试题-贵州-2014_三年中考化学贵州省2011-2013年中考化学命题点示例 第十单元 酸和碱(pdf版).rar
 立即下载
立即下载


如果您无法下载资料,请参考说明:
1、部分资料下载需要金币,请确保您的账户上有足够的金币
2、已购买过的文档,再次下载不重复扣费
3、资料包下载后请先用软件解压,在使用对应软件打开
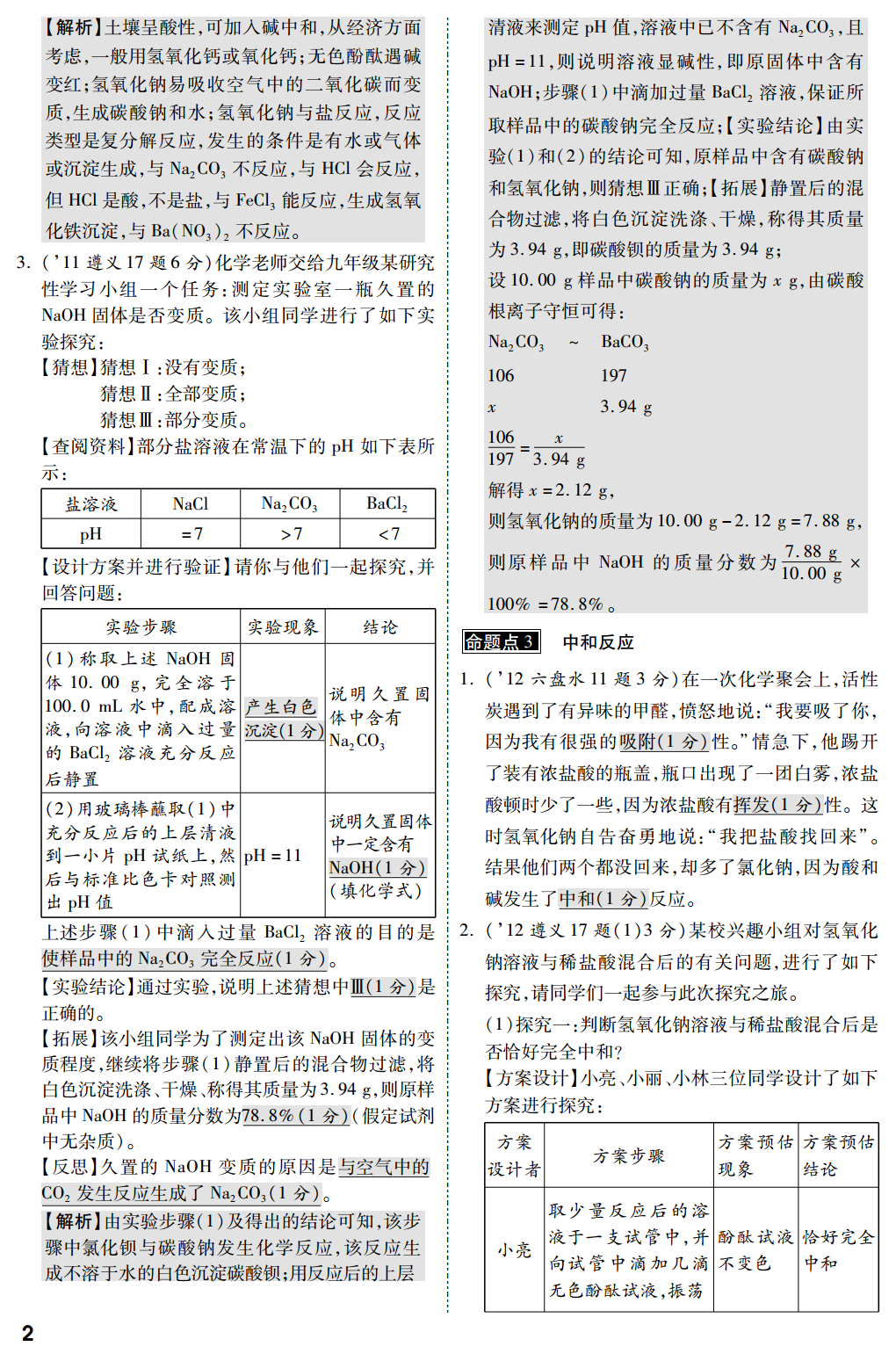
第十单元酸和碱命题点1常见酸的性质及用途注意不能将水加入浓硫酸中;溶解时要用玻璃棒不断搅动,缓慢注入,以免液体沸腾,液滴飞1.(’13铜仁26题7分)使用浓硫酸时要十分小心,溅出来。浓硫酸有强烈的腐蚀性(1分)!所以,不要将浓硫酸沾到皮肤或衣服上。为了加深记忆,小丽同命题点2常见碱的性质及用途学用如图形象地总结了硫酸能与5类物质发生反1.(’13六盘水6题2分)下列物质中,前者是碱,后应。请你根据要求完成下列问题:者是氧化物的是(B)(1)将紫色石蕊溶液滴入稀硫酸A.纯碱干冰B.熟石灰生石灰溶液中,紫色石蕊溶液遇稀硫酸C.烧碱小苏打D.酒精水变成红色(1分)。【解析】碱是指电离时产生的阴离子全部是氢氧(2)稀硫酸能够除铁锈(铁锈的根离子的化合物,氧化物是指由两种元素组成主要成分Fe2O3),除锈后溶液颜且其中一种是氧元素的化合物。纯碱的成分是色的变化情况是无色变成黄色Na2CO3,由金属离子和酸根离子构成,属于盐,(1分),写出反应的化学方程式第1题图干冰就是固体CO2,属于氧化物,A错误;熟石灰Fe2O3+3H2SO4Fe2(SO4)3+主要成分是Ca(OH)2,生石灰主要成分是CaO,3HO(1分)。2属于氧化物,B正确;烧碱是氢氧化钠的俗称,成(3)为了验证反应⑤能够发生,应选择的物质是分为NaOH,属于碱,小苏打是碳酸氢钠的俗称,(C(1分))主要成分是NaHCO3,属于盐,C错误;酒精的成A.NaCl溶液B.NaOH溶液分为C2H5OH,是含有碳元素的化合物,属于有C.Ba(NO3)2溶液D.MgCl2溶液机物,水的化学式为HO,属于氧化物,D错误。2(4)用废铁屑与废硫酸(H2SO4的质量分数为20%)2.(’12铜仁26题(1)(2)4分)某化学活动小组以反应可制取硫酸亚铁,写出由废铁屑中铁制取硫酸“酸碱盐的性质”为主题进行探究性学习,请你作亚铁的化学反应方程式Fe+H2SO4FeSO4+为该小组成员一起来解决下列问题:H2↑(1分);若得到的硫酸亚铁溶液中含少量硫(1)小红同学从某一欠收农田里取回一份土壤样酸铜,请你选择合适的物质除去硫酸铜,写出其化品,如果检测结果呈酸性,从经济和可行方面考学反应方程式Fe+CuSOCu+FeSO(1分)。44虑,那么要改良此土壤的酸性,应向农田里施加【解析】浓硫酸具有很强的腐蚀性;(1)将紫色石Ca(OH)2(或CaO)(1分)(填化学式)。蕊溶液滴入稀硫酸溶液中,紫色石蕊溶液遇稀硫(2)小红同学用如图所示总结了NaOH的四条化学酸变成红色;(2)稀硫酸能够除铁锈,反应的化学性质(即NaOH与四类物质能够发生化学反应)。方程式为Fe2O3+3H2SO4Fe2(SO4)3+3HO,除锈后生成的Fe(SO)溶液为黄色;2243(3)反应⑤是硫酸与某些盐反应,A、C、D属于盐,但是能和硫酸发生复分解反应的只有Ba(NO3)2溶液;(4)由废铁屑中铁制取硫酸亚铁的化学反第2题图Ⅰ.为了验证反应①,小红将无色酚酞试液滴入应方程式为Fe+H2SO4FeSO4+H2↑;硫酸NaOH溶液中,溶液由无色变成红色(1分)。亚铁溶液中含少量硫酸铜,可以加入过量的铁粉Ⅱ.依据反应④说明NaOH必须密封保存,否则在空气除去,反应的化学方程式为Fe+CuSOCu4中要变质,其化学反应方程式为CO2+2NaOH+FeSO4。NaCO+HO(1分)。2.(’12铜仁23题3分)简述在实验室如何稀释浓232硫酸。Ⅲ.为了验证反应③能够发生,你选择的物质是将浓硫酸沿烧杯壁(或玻璃棒)缓慢地注入水中,C(1分)。并用玻璃棒不断搅拌(3分)A.Na2CO3B.HCl【解析】因浓硫酸溶于水会放出大量的热,特别C.FeCl3D.Ba(NO)21书【解析】土壤呈酸性,可加入碱中和,从经济方面清液来测定pH值,溶液中已不含有Na2CO3,且考虑,一般用氢氧化钙或氧化钙;无色酚酞遇碱pH=11,则说明溶液显碱性,即原固体中含有变红;氢氧化钠易吸收空气中的二氧化碳而变NaOH;步骤(1)中滴加过量BaCl溶液,保证所2质,生成碳酸钠和水;氢氧化钠与盐反应,反应取样品中的碳酸钠完全反应;【实验结论】由实类型是复分解反应,发生的条件是有水或气体验(1)和(2)的结论可知,原样品中含有碳酸钠或沉淀生成,与Na2CO3不反应,与HCl会反应,和氢氧化钠,

努力****凌芹
 实名认证
实名认证
 内容提供者
内容提供者
最近下载


















