


如果您无法下载资料,请参考说明:
1、部分资料下载需要金币,请确保您的账户上有足够的金币
2、已购买过的文档,再次下载不重复扣费
3、资料包下载后请先用软件解压,在使用对应软件打开
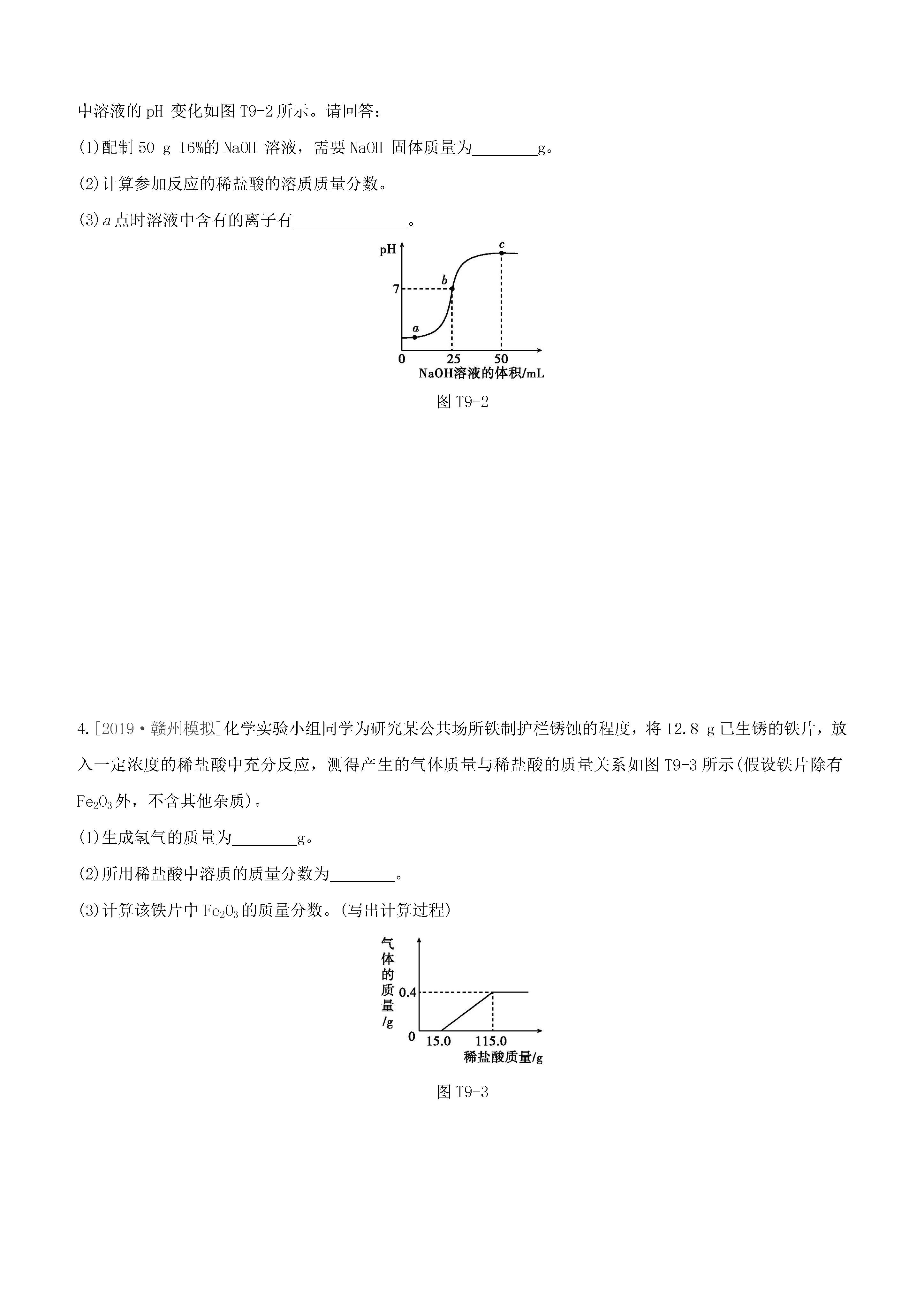
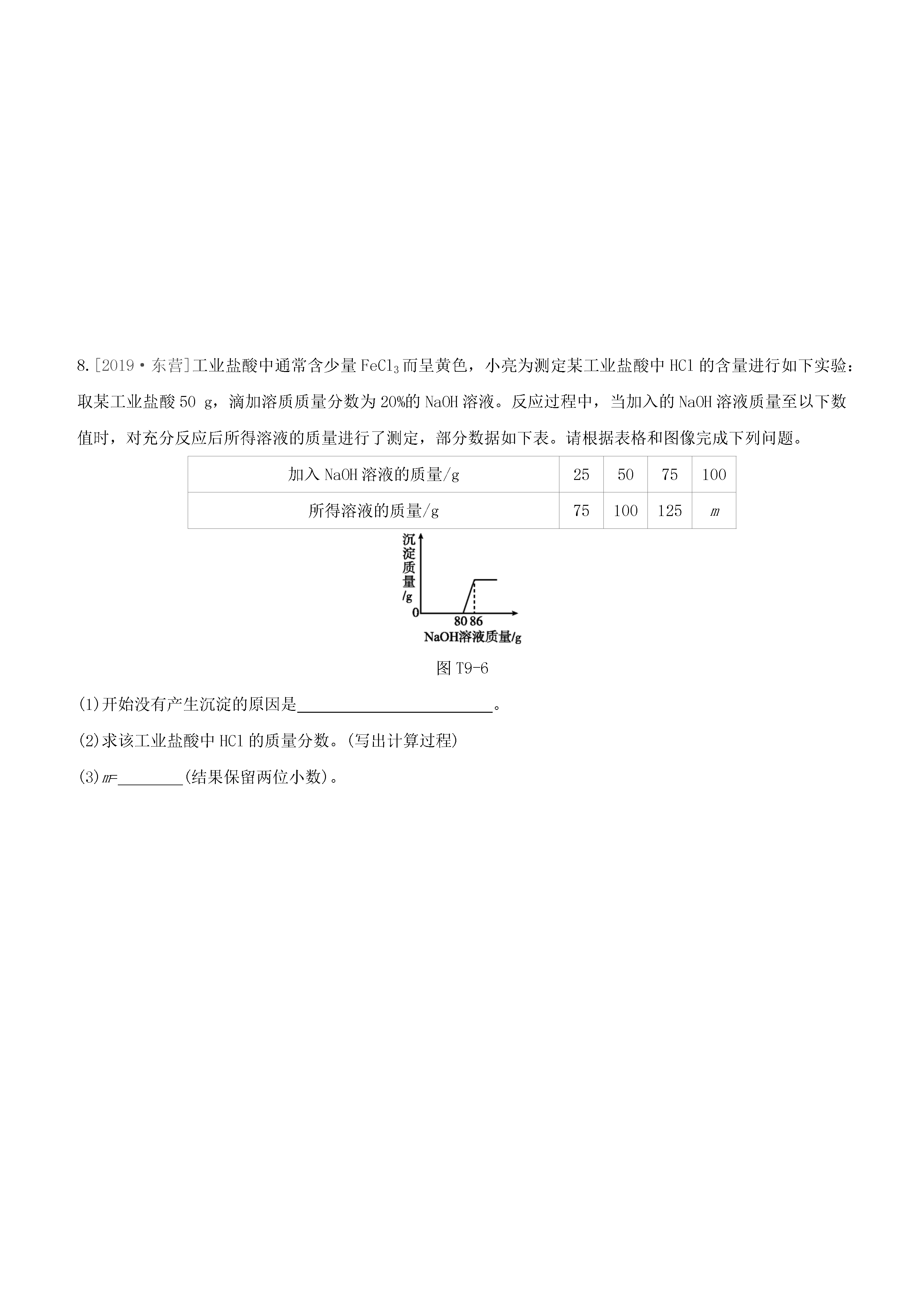
题型突破(九)计算题1.[2017·江西]学习小组测定某工业废水(含有H2SO4、HNO3,不含固体杂质)中H2SO4的含量。取100g废水于烧杯中,加入100gBaCl2溶液,恰好完全反应,经过滤得到176.7g溶液(可溶性杂质不参加反应,过滤后滤液的损失忽略不计)。求:(1)充分反应后生成沉淀的质量为g。(2)该工业废水中硫酸的质量分数为多少?(写出计算过程)(3)为避免工业废水污染环境,排放前应对废水进行中和处理,需加入的物质是。2.[2019·赣州模拟]某氢氧化钠样品中混有氯化钠,为测定样品中氢氧化钠的质量分数,称取5g样品,加入27g水完全溶解后,缓慢加入稀盐酸,同时测定溶液的pH。当pH=7时,刚好用去10%的稀盐酸36.5g。试计算:(1)将100g质量分数为38%的浓盐酸稀释成10%的稀盐酸,需加水的质量为g。(2)样品中氢氧化钠的质量分数。(3)反应后所得溶液中溶质的质量分数。3.[2019·江西模拟]向盛有36.5g稀盐酸的烧杯中逐滴加入16%的NaOH溶液(密度为1g·mL-1),测得烧杯中溶液的pH变化如图T9-2所示。请回答:(1)配制50g16%的NaOH溶液,需要NaOH固体质量为g。(2)计算参加反应的稀盐酸的溶质质量分数。(3)a点时溶液中含有的离子有。图T9-24.[2019·赣州模拟]化学实验小组同学为研究某公共场所铁制护栏锈蚀的程度,将12.8g已生锈的铁片,放入一定浓度的稀盐酸中充分反应,测得产生的气体质量与稀盐酸的质量关系如图T9-3所示(假设铁片除有Fe2O3外,不含其他杂质)。(1)生成氢气的质量为g。(2)所用稀盐酸中溶质的质量分数为。(3)计算该铁片中Fe2O3的质量分数。(写出计算过程)图T9-35.[2019·郴州]往80g含有硝酸铜和硝酸银的混合溶液中加入一定量的镁粉,加入的镁粉的质量与溶液质量变化如图T9-4所示。试分析计算:(1)a→b段表示镁粉与混合溶液中的(填化学式)反应。(2)原混合溶液中硝酸铜的质量分数是多少?(写出计算过程,精确到0.1%)图T9-46.[2019·绍兴]为了探究氢氧化钡溶液和硫酸钠溶液反应后所得滤液X的成分,同学们做了以下实验:取50g滤液于烧杯中,先向烧杯中滴加溶质质量分数为6%的硫酸镁溶液20g,接着向烧杯中滴加稀硫酸。加入溶液的质量与烧杯内沉淀的质量关系如图T9-5所示。图T9-5(1)滤液X的pH(填“大于”“小于”或“等于”)7。(2)CD段发生反应的化学方程式为。(3)滤液X中含有的溶质是。(4)滴加入30g稀硫酸时,烧杯中沉淀的质量m2的值为多少?(写出计算过程)7.[2019·九江模拟改编]某样品仅含NaCl和MgCl2,为探究样品中MgCl2的质量分数,某研究性小组取了19g样品,加入138.8g水使其完全溶解后,再将120g一定溶质质量分数的NaOH溶液不断加入到该溶液中,充分反应后,测得相关数据如下表。实验次数1234加入NaOH溶液质量/g30303030共生成沉淀的质量/g2.95.8m5.8求:(1)表中m的值为(填序号)。A.大于5.8B.小于5.8C.等于5.8D.大于或等于5.8(2)样品中MgCl2的质量。(写出计算过程)(3)计算第二次实验后溶液中溶质的质量分数。(保留一位小数)8.[2019·东营]工业盐酸中通常含少量FeCl3而呈黄色,小亮为测定某工业盐酸中HCl的含量进行如下实验:取某工业盐酸50g,滴加溶质质量分数为20%的NaOH溶液。反应过程中,当加入的NaOH溶液质量至以下数值时,对充分反应后所得溶液的质量进行了测定,部分数据如下表。请根据表格和图像完成下列问题。加入NaOH溶液的质量/g255075100所得溶液的质量/g75100125m图T9-6(1)开始没有产生沉淀的原因是。(2)求该工业盐酸中HCl的质量分数。(写出计算过程)(3)m=(结果保留两位小数)。9.[2019·衢州]小科为测定某石灰石样品(主要成分为碳酸钙,其他成分不与稀盐酸反应)中碳酸钙的含量,利用气密性良好的图T9-8中甲装置进行实验:①称取石灰石样品6g,加入锥形瓶中,塞紧瓶塞,从左侧持续缓慢鼓入空气;②一段时间后打开分液漏斗活塞,注入足量的稀盐酸,开始计时;③待装置D总质量不再增加时停止鼓入空气。实验过程中测得装置D增加的质量随时间变化图像如图乙(碱石灰能吸收二氧化碳和水)。图T9-8(1)根据图乙,运用化学方程式计算该石灰石样品中碳酸钙的

白真****ng
 实名认证
实名认证
 内容提供者
内容提供者
最近下载


















