



如果您无法下载资料,请参考说明:
1、部分资料下载需要金币,请确保您的账户上有足够的金币
2、已购买过的文档,再次下载不重复扣费
3、资料包下载后请先用软件解压,在使用对应软件打开
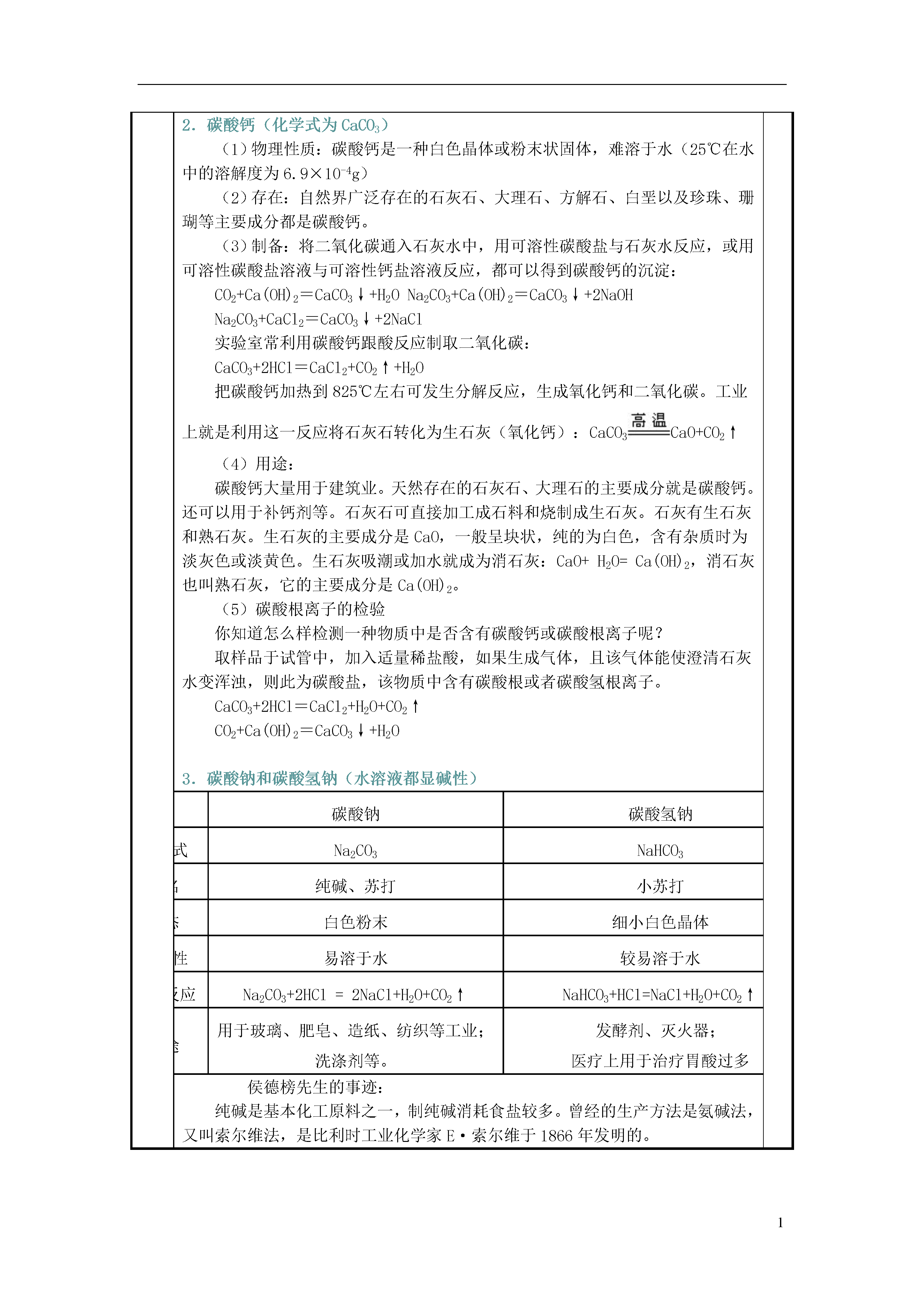
1盐的性质学案主题新课讲解课时数量(全程或具体时间)第()课时授课时段教学目标教学内容重要的盐个性化学习问题解决见教案教学重点、难点盐的化学性质和复分解反应考点分析盐的有关化学方程式和运用复分解反应的条件来判断化学方程式的书写教学过程学生活动教师活动一、盐的分类根据盐的组成不同,如按盐组成中的阳离子或阴离子的名称,一般有如下的分类:钠盐:NaCl、Na2CO3、Na2SO4、Na2S等。钾盐:K2CO3、KNO3、KCl等。硫酸盐:CuSO4、K2SO4、(NH4)2SO4等。碳酸盐:Na2CO3、K2CO3、(NH4)2CO3等。盐的分类方法还有很多种,例如:酸式盐、碱式盐和正盐;含氧酸盐和无氧酸盐;强酸弱碱盐、强碱弱酸盐、强酸强碱盐和弱酸弱碱盐等。二、生活中常见的盐1.氯化钠(重要的调味品,食盐的主要成分是NaCl)(1)物理性质:白色晶体,易溶于水,有咸味。(2)在人的正常生理过程中的作用:人体中的氯化钠都是以离子的形式存在于体液中,钠离子对于维持细胞内外正常水分分布和促进细胞内外物质的交换起主要作用;氯离子是胃液的主要成分,具有促生盐酸、帮助消化和增进食欲的作用。人体正常每人每天约需3g~5g食盐。但长期食用过多食盐不利于人体健康。(3)存在:海水、盐湖、盐井、盐矿(4)用途:①医疗上的生理盐水(质量分数为0.9%)②用来制备Na2CO3、NaOH、Cl2、HCl等物质;③食品的调味剂,腌渍蔬菜等;④公路积雪可以用氯化钠消除;⑤农业上利用氯化钠溶液来选种。粗盐的提纯:(1)溶解-------使用的仪器:烧杯、玻璃棒、药匙玻璃棒的作用:加快溶解速率,不能提高物质的溶解度操作要点:搅拌时玻璃棒不能接触烧杯壁(2)过滤------使用的仪器:漏斗、铁架台(带铁圈)、玻璃棒、烧杯玻璃棒的作用:引流操作要点:一贴、二低、三靠(3)蒸发-------使用的仪器:蒸发皿、铁架台(带铁圈)、玻璃棒、酒精灯、坩埚钳玻璃棒的作用:防止液体局部过热而引起液滴飞溅操作要点:当蒸发皿中出现较多固体时,即停止加热,利用余热使液体全部挥发。*如果有转移操作:最后在转移固体时,玻璃棒起到转移的作用。2.碳酸钙(化学式为CaCO3)(1)物理性质:碳酸钙是一种白色晶体或粉末状固体,难溶于水(25℃在水中的溶解度为6.9×10-4g)(2)存在:自然界广泛存在的石灰石、大理石、方解石、白垩以及珍珠、珊瑚等主要成分都是碳酸钙。(3)制备:将二氧化碳通入石灰水中,用可溶性碳酸盐与石灰水反应,或用可溶性碳酸盐溶液与可溶性钙盐溶液反应,都可以得到碳酸钙的沉淀:CO2+Ca(OH)2=CaCO3↓+H2ONa2CO3+Ca(OH)2=CaCO3↓+2NaOHNa2CO3+CaCl2=CaCO3↓+2NaCl实验室常利用碳酸钙跟酸反应制取二氧化碳:CaCO3+2HCl=CaCl2+CO2↑+H2O把碳酸钙加热到825℃左右可发生分解反应,生成氧化钙和二氧化碳。工业上就是利用这一反应将石灰石转化为生石灰(氧化钙):CaCO3CaO+CO2↑(4)用途:碳酸钙大量用于建筑业。天然存在的石灰石、大理石的主要成分就是碳酸钙。还可以用于补钙剂等。石灰石可直接加工成石料和烧制成生石灰。石灰有生石灰和熟石灰。生石灰的主要成分是CaO,一般呈块状,纯的为白色,含有杂质时为淡灰色或淡黄色。生石灰吸潮或加水就成为消石灰:CaO+H2O=Ca(OH)2,消石灰也叫熟石灰,它的主要成分是Ca(OH)2。(5)碳酸根离子的检验你知道怎么样检测一种物质中是否含有碳酸钙或碳酸根离子呢?取样品于试管中,加入适量稀盐酸,如果生成气体,且该气体能使澄清石灰水变浑浊,则此为碳酸盐,该物质中含有碳酸根或者碳酸氢根离子。CaCO3+2HCl=CaCl2+H2O+CO2↑CO2+Ca(OH)2=CaCO3↓+H2O3.碳酸钠和碳酸氢钠(水溶液都显碱性)碳酸钠碳酸氢钠化学式Na2CO3NaHCO3俗名纯碱、苏打小苏打色态白色粉末细小白色晶体溶解性易溶于水较易溶于水与酸反应Na2CO3+2HCl=2NaCl+H2O+CO2↑NaHCO3+HCl=NaCl+H2O+CO2↑用途用于玻璃、肥皂、造纸、纺织等工业;洗涤剂等。发酵剂、灭火器;医疗上用于治疗胃酸过多侯德榜先生的事迹:纯碱是基本化工原料之一,制纯碱消耗食盐较多。曾经的生产方法是氨碱法,又叫索尔维法,是比利时工业化学家E·索尔维于1866年发明的。氨碱法是把氨气溶于食盐水后,通入二氧化碳,生成碳酸氢钠。分离后加热分解,即得到纯碱(碳酸钠):NaCl+NH3·H2O+CO2=NaHCO3↓(晶体析出)+NH4Cl2NaHCO3Na2CO3+H2O+CO2↑反应生成的氯化铵可与熟石灰(Ca(OH)2)作用,生成氨气而回收,剩下残渣氯化钙。而由

是你****平呀
 实名认证
实名认证
 内容提供者
内容提供者
最近下载


















