

如果您无法下载资料,请参考说明:
1、部分资料下载需要金币,请确保您的账户上有足够的金币
2、已购买过的文档,再次下载不重复扣费
3、资料包下载后请先用软件解压,在使用对应软件打开
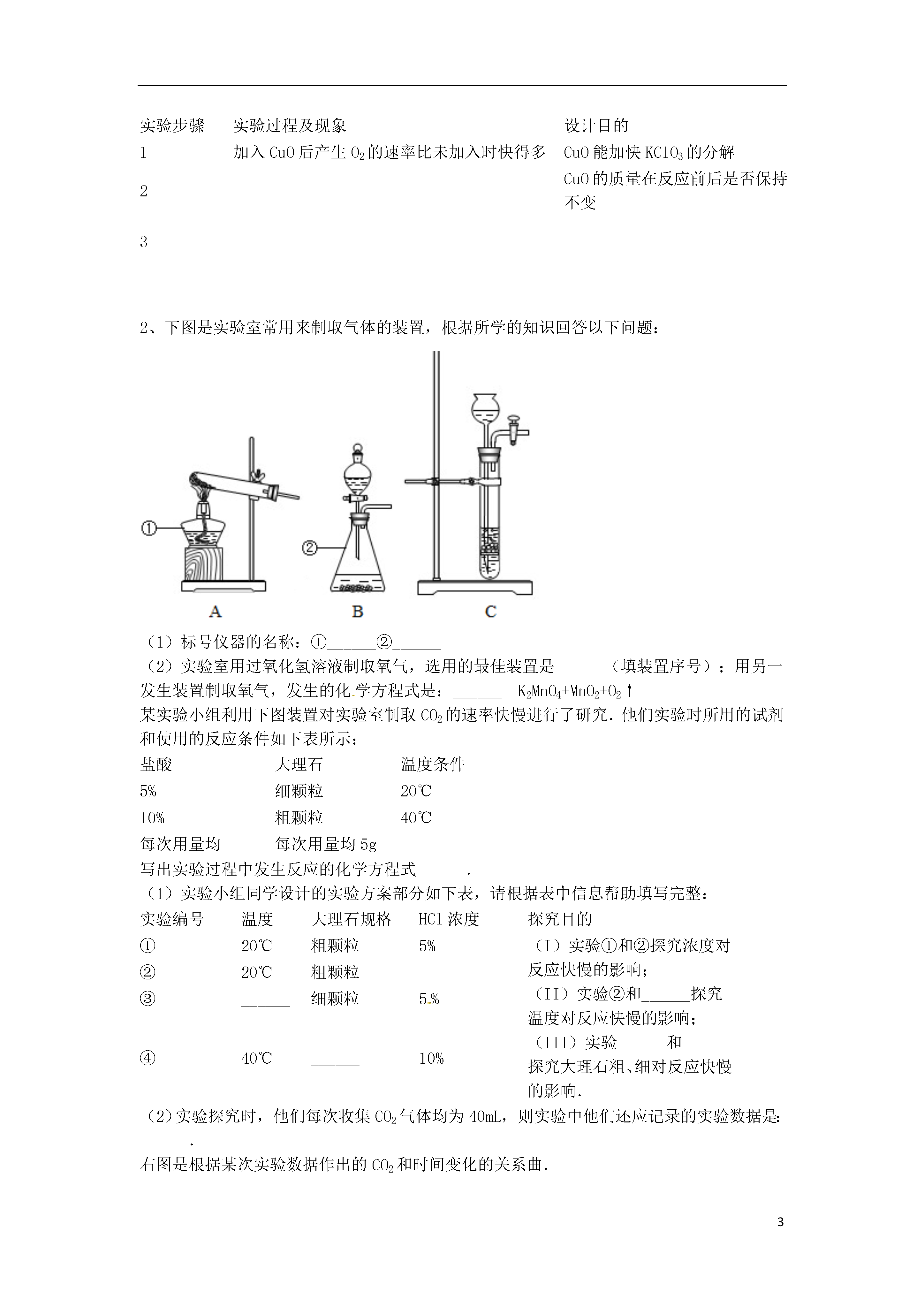
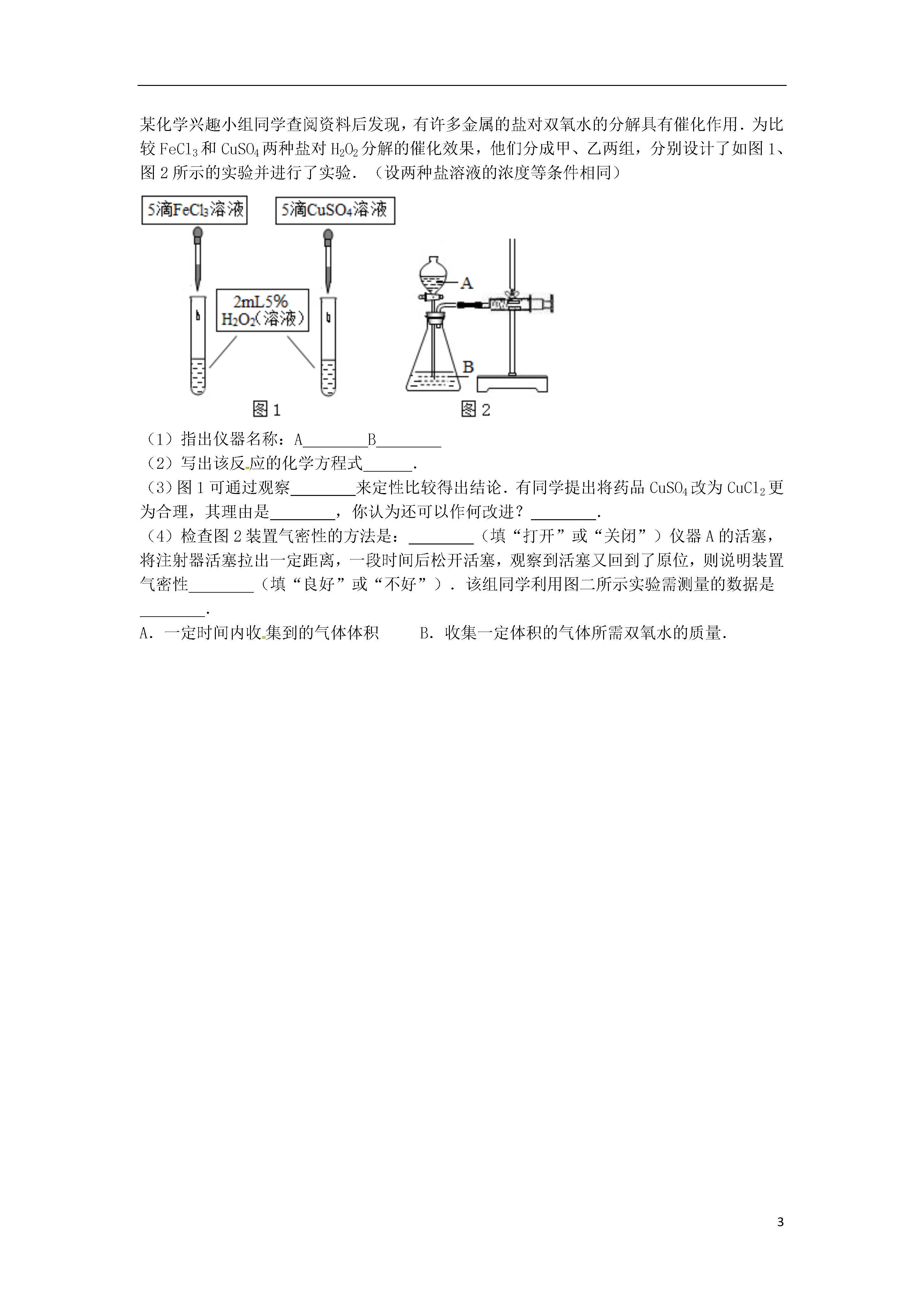
3影响化学反应速率的因素探究41、某研究性学习小组欲证明氧化铜也能作为氯酸钾分解反应的催化剂,他们进行了如下实验:①称取1.0gCuSO4粉末加入10mL蒸馏水完全溶解;②将足量的NaOH溶液与上述溶液充分反应,生成蓝色沉淀,过滤后洗涤沉淀;③将所得沉淀转移到坩埚(一种可用于加热固体物质的容器)中,均匀缓慢加热至完全变为黑色的氧化铜,研细备用;④按下表中的质量将固体混合好后,在相同条件下加热,并与MnO2的催化效果做比较,实验时间均以生成50mL气体为准(见图甲),其他可能影响实验的因素均忽略.编号KClO3质量(g)其他物质质量(g)待测数据12.0不加任何物质…22.0CuO0.5…32.0MnO20.5…回答下列问题:(1)上述实验步骤中需要使用玻璃棒的是______(填序号).(2)写出步骤③的化学方程式______.(3)表格中的“待测数据”是指______.(4)若实验过程中50mL量气管中液面的位置如图乙所示,A与B刻度间相差1mL,刻度A的读数为20,则此时量气管中收集到的气体体积为______.(5)如果要进一步探究CuO在反应中是否起到催化作用,请完成后续实验.实验步骤实验过程及现象设计目的1加入CuO后产生O2的速率比未加入时快得多CuO能加快KClO3的分解2CuO的质量在反应前后是否保持不变3下图是实验室常用来制取气体的装置,根据所学的知识回答以下问题:(1)标号仪器的名称:①______②______(2)实验室用过氧化氢溶液制取氧气,选用的最佳装置是______(填装置序号);用另一发生装置制取氧气,发生的化学方程式是:______K2MnO4+MnO2+O2↑某实验小组利用下图装置对实验室制取CO2的速率快慢进行了研究.他们实验时所用的试剂和使用的反应条件如下表所示:盐酸大理石温度条件5%细颗粒20℃10%粗颗粒40℃每次用量均每次用量均5g写出实验过程中发生反应的化学方程式______.(1)实验小组同学设计的实验方案部分如下表,请根据表中信息帮助填写完整:实验编号温度大理石规格HCl浓度探究目的①20℃粗颗粒5%(I)实验①和②探究浓度对反应快慢的影响;(II)实验②和______探究温度对反应快慢的影响;(III)实验______和______探究大理石粗、细对反应快慢的影响.②20℃粗颗粒______③______细颗粒5%④40℃______10%实验探究时,他们每次收集CO2气体均为40mL,则实验中他们还应记录的实验数据是:______.右图是根据某次实验数据作出的CO2和时间变化的关系曲.请分析在80秒以后,产生CO2逐渐减慢的可能原因:______.4、金属活动性顺序在工农业生产和科学研究中有重要应用.请回答下列问题:(1)完成金属活动性顺序表:KCaNaMgA1ZnFeSnPb(H)Cu______AgPtAu.(2)现有两种金属,分别是金属甲和金属铁.请用以下药品检验它们的金属活动性顺序,应选用的是_____(填序号).A.浓度为10%的盐酸B.浓度为98%的硫酸C.粉状10g金属甲D.10g铁片E.片状5g金属甲F.10g片状金属甲(3)某研究小组拟用定量的方法测量A1和Fe分别与酸反应的快慢,设计了下图所示的装置(实验中采用表面积相同的铝丝和铁丝).①实验时,为了除去铝丝和铁丝表面的氧化物,其操作是______.②检查图示装置气密性的方法是______.③实验测得铝丝产生气体的速率(v)与时间(t)的关系如图所示,则t1~t2时间内反应速率逐渐加快的主要原因是______.(4)该研究小组若要探究铜、锌、银的金属活动性顺序,请你设计一个实验探究.实验步骤实验现象实验结论某化学兴趣小组同学查阅资料后发现,有许多金属的盐对双氧水的分解具有催化作用.为比较FeCl3和CuSO4两种盐对H2O2分解的催化效果,他们分成甲、乙两组,分别设计了如图1、图2所示的实验并进行了实验.(设两种盐溶液的浓度等条件相同)(1)指出仪器名称:AB(2)写出该反应的化学方程式.(3)图1可通过观察来定性比较得出结论.有同学提出将药品CuSO4改为CuCl2更为合理,其理由是,你认为还可以作何改进?.(4)检查图2装置气密性的方法是:(填“打开”或“关闭”)仪器A的活塞,将注射器活塞拉出一定距离,一段时间后松开活塞,观察到活塞又回到了原位,则说明装置气密性(填“良好”或“不好”).该组同学利用图二所示实验需测量的数据是.A.一定时间内收集到的气体体积B.收集一定体积的气体所需双氧水的质量.

是你****韵呀
 实名认证
实名认证
 内容提供者
内容提供者
最近下载


















