



如果您无法下载资料,请参考说明:
1、部分资料下载需要金币,请确保您的账户上有足够的金币
2、已购买过的文档,再次下载不重复扣费
3、资料包下载后请先用软件解压,在使用对应软件打开
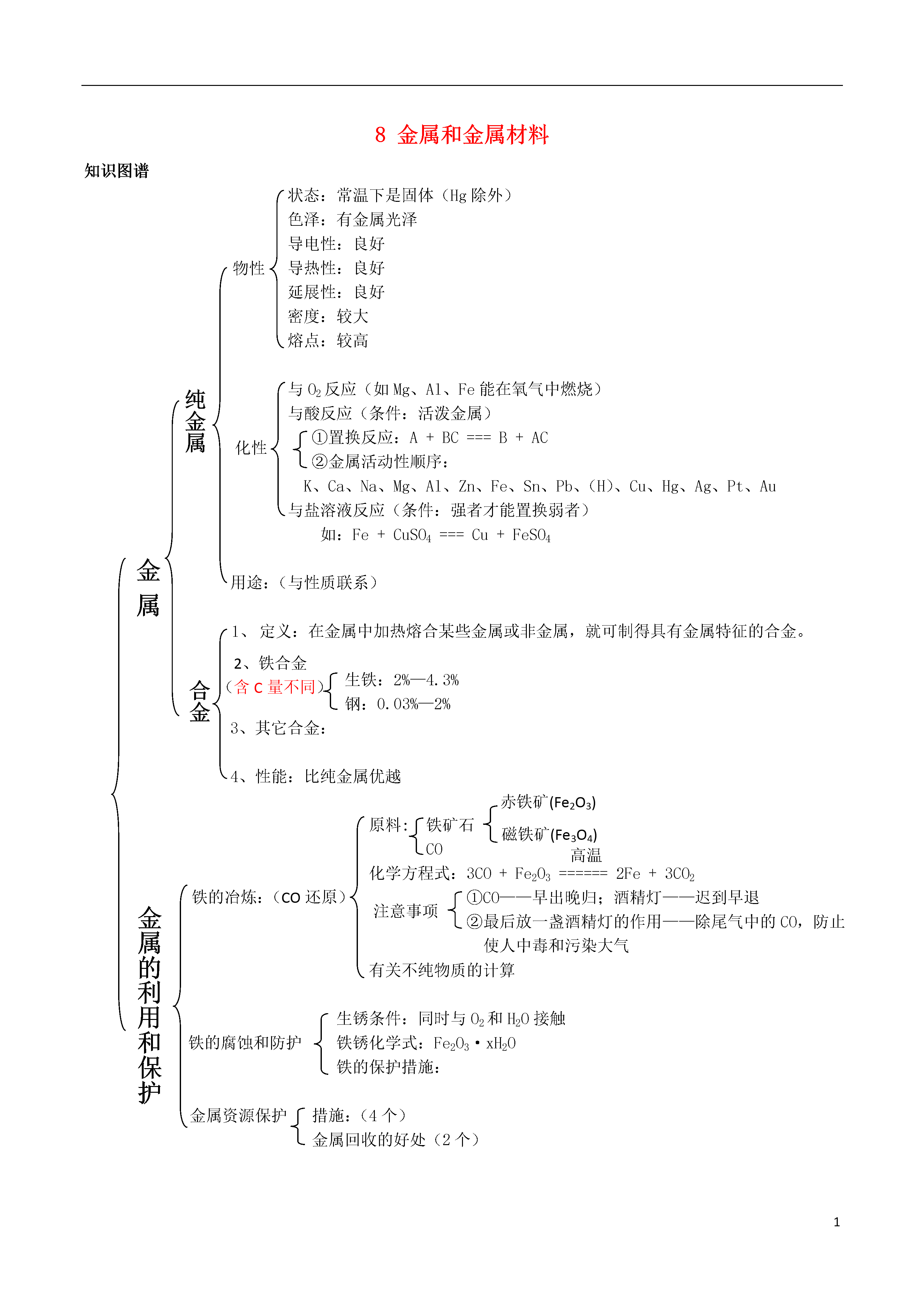
18金属和金属材料知识图谱状态:常温下是固体(Hg除外)色泽:有金属光泽物性导电性:良好导热性:良好延展性:良好密度:较大熔点:较高纯金属与O2反应(如Mg、Al、Fe能在氧气中燃烧)与酸反应(条件:活泼金属)化性①置换反应:A+BC===B+AC②金属活动性顺序:K、Ca、Na、Mg、Al、Zn、Fe、Sn、Pb、(H)、Cu、Hg、Ag、Pt、Au金属材料与盐溶液反应(条件:强者才能置换弱者)如:Fe+CuSO4===Cu+FeSO4用途:(与性质联系)定义:在金属中加热熔合某些金属或非金属,就可制得具有金属特征的合金。2、铁合金(含C量不同)合金生铁:2%—4.3%钢:0.03%—2%3、其它合金:赤铁矿(Fe2O3)4、性能:比纯金属优越磁铁矿(Fe3O4)原料:铁矿石高温CO铁的冶炼:(CO还原)化学方程式:3CO+Fe2O3======2Fe+3CO2注意事项金属的利用和保护①CO——早出晚归;酒精灯——迟到早退②最后放一盏酒精灯的作用——除尾气中的CO,防止使人中毒和污染大气有关不纯物质的计算铁的腐蚀和防护生锈条件:同时与O2和H2O接触铁锈化学式:Fe2O3·xH2O铁的保护措施:金属资源保护措施:(4个)金属回收的好处(2个)1.金属与氧气反应(1)常温下能反应:镁、铝;2Mg+O2=2MgO4Al+3O2=2Al2O3(2)点燃或加热条件下能反应:Fe、Cu;3Fe+2O2Fe3O42Cu+O22CuO(3)高温下也不反应:金、银。(4)与氧气反应情况金属与氧气反应情况镁在空气中常温就能缓慢氧化。点燃时剧烈燃烧。生成白色固体。铝在空气中常温就能缓慢氧化,表面形成致密的氧化铝薄膜。在氧气中点燃时剧烈燃烧。生成白色固体。铁在干燥的空气中不易与氧气反应,但是在潮湿的空气中易与氧气、水等反应生成铁锈,主要成分为氧化铁。铁在空气中不能燃烧,在氧气中能剧烈燃烧。生成一种黑色固体。铜在干燥的空气中不易与氧气反应,但是在潮湿的空气中易与氧气、水、二氧化碳等反应生成铜绿,主要成分是碱式碳酸铜。铜在空气中加热时表面会生成黑色的氧化铜。金在常温与高温时都不与氧气反应。备注:①金属与氧气反应的难易和剧烈程度首先与金属本身的性质有关,其次还与金属粉碎的程度、与氧气的接触面积、氧气的浓度、温度等因素有关;②铝具有抗腐蚀性不是因为它不活泼,而是因为它比较活泼,会与氧气反应生成一层致密的氧化铝薄膜;③根据金属与氧气反应的条件,可以判断金属的活动性强弱,条件分为三种:常温条件下、加热、高温。条件越容易说明金属活动性越强。2.金属与盐酸、稀硫酸反应(1)金属与盐酸反应:活泼金属+酸→盐+H2↑金属与酸反应与金属活动性有关,金属活动性越强,与酸反应越剧烈,金属活动性越弱,与酸反应越慢,甚至不反应,故这四种金属的活动性顺序为Mg>Zn>Fe>Cu。(2)金属与稀硫酸反应:①Mg+H2SO4=MgSO4+H2↑;②Fe+H2SO4=FeSO4+H2↑;③Zn+H2SO4=ZnSO4+H2↑。备注:①实验室制取氢气选用块状锌粒和稀硫酸,其原因之一是反应速率适中;②若用m表示参加反应的金属质量,M表示金属的相对原子质量,则金属与足量的盐酸或稀硫酸反应生成氢气的质量=m×金属的化合价数M;③化合价相同的等质量金属完全反应放出氢气的质量与金属的相对原子质量成反比。3.置换反应(1)定义:由一种单质与一种化合物反应,生成另一种单质和另一种化合物的反应。(2)表达式:单质+化合物→新单质+新化合物通式:A+BC→AC+B特点:一单换一单(3)已学过反应类型:备注:①置换反应前后物质的类别:①单质(A和B):可以是金属,也可以是非金属(碳或氢气);②化合物(BC和AC):可以是酸或金属化合物(溶液),也可以是氧化物;②条件:判断一个反应是否是置换反应,必须同时符合两个条件:反应物是一种单质和一种化合物,生成物是另一种单质和另一种化合物;③规律:置换反应中因反应物和生成物都有单质,参加反应的单质和生成物的单质中元素的化合价一定有变化。4.金属活动性:A1>Cu>Ag5.金属活动性顺序(1)规律:(2)在金属活动性顺序里:①金属的位置越靠前,它的活动性越强;②位于氢前面的金属能置换出盐酸、稀硫酸中的氢;③位于前面的金属一般能把位于它后面的金属从它们的盐溶液里置换出来。(K、Ca、Na除外)。(3)反应一定要在水溶液中进行,不溶于水的金属化合物一般不与金属反应。如Mg和AgCl不反应。因为AgCl不溶于水。(4)由于K、Ca、Na的活动性较强,若将它们放入某金

努力****冰心
 实名认证
实名认证
 内容提供者
内容提供者
最近下载


















