


如果您无法下载资料,请参考说明:
1、部分资料下载需要金币,请确保您的账户上有足够的金币
2、已购买过的文档,再次下载不重复扣费
3、资料包下载后请先用软件解压,在使用对应软件打开
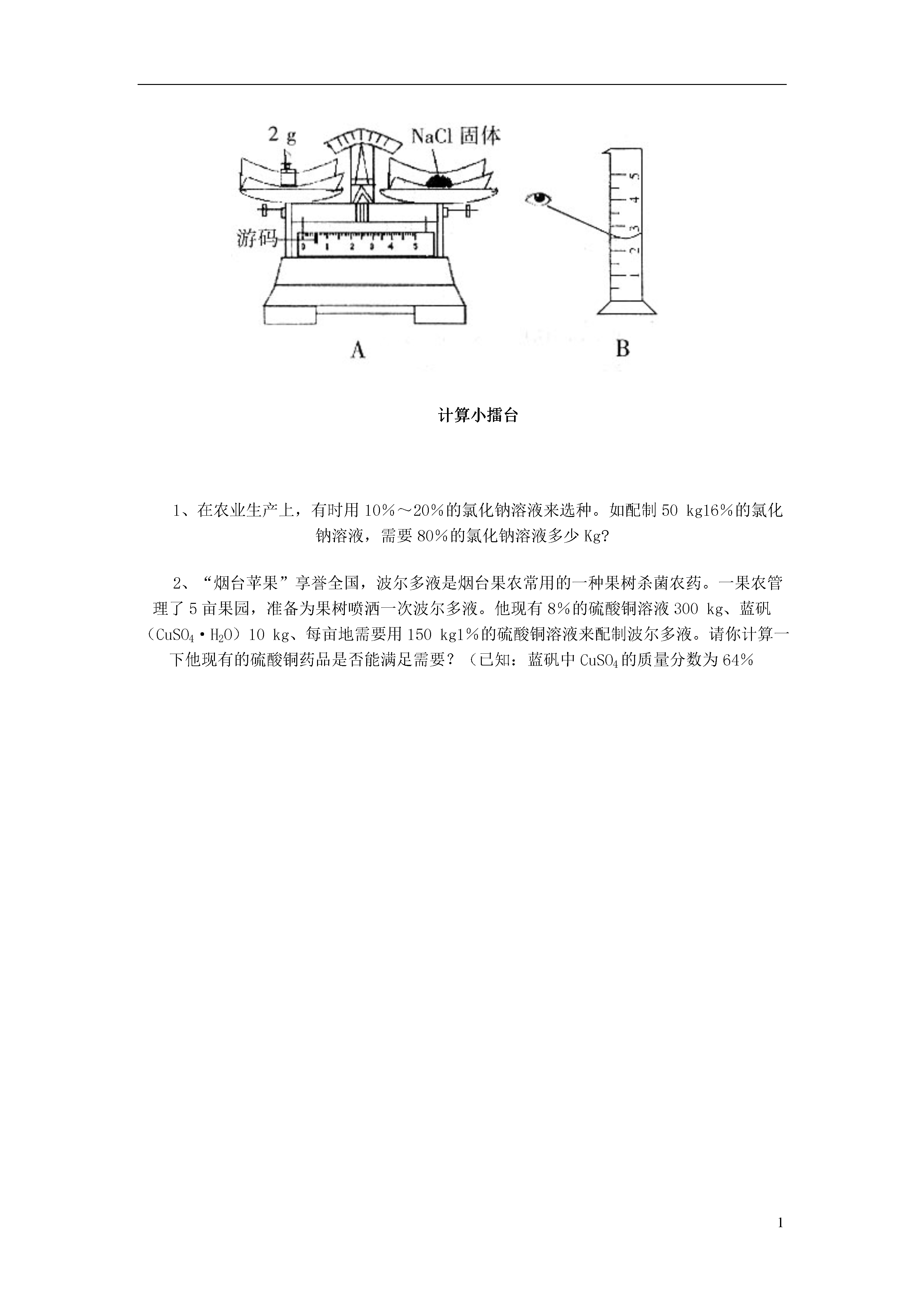
1《第9单元课题3溶质的质量分数》检测题趣味导读你知道溶质质量后分数为5%的意思吗?14°的含义吗?别着急。让我从酿酒开始。我国有悠久的酿酒历史,其中五粮液等在国际上享有盛誉。某五粮液白酒的商标上注有“53°”字样,它表示该酒在53℃的条件下酿制的,还是该酒的着火点是53℃,或者100g该酒中含有53g酒精,再或者100mL该酒中含有53mL酒精。你是不是想知道答案呢?请跟我来吧!智能点拨例1预防“非典”(SARS),家庭、学校经常使用过氧乙酸(CH3COOOH)作消毒剂,它是一种具有腐蚀性、强烈刺激性气味的无色液体,易分解产生氧气,有杀菌、漂白作用。它的相对分子质量是。市售过氧乙酸溶液的质量分数为20%,若要配制0.1%的该消毒液2000g,需20%的过氧乙酸溶液质量为。答案:76;10g。关键点:(1)CH3COOOH的相对分子质量==12×2+16×3+1×4=76(2)设需20%的过氧乙酸的质量为x则20%x=0.1%×2000gx=10g例2溶液与人类的生活息息相关,溶液的配制是日常生活和化学实验中的常见操作。下表示硫酸溶液和氨水的密度与其溶质的质量分数对照表(20℃)溶液中溶质的质量分数/%412162428硫酸溶液的密度/(g/mL)1.021.081.111.171.20氨水的密度/(g/mL)0.980.950.940.910.90请仔细分析回答下列问题:(1)20℃时,随着溶液中溶质的质量分数逐渐增大,硫酸溶液的密度逐渐(填增大、减或不变);氨水的密度逐渐(填增大、减或不变)。(2)取12%的硫酸溶液100g配制成6%的溶液,向100g12%的硫酸溶液中加水的质量应100g(填大于、小于或等于)。(3)向100g24%的氨水中加入100g水,摇匀,溶液体积是mL(保留到0.1)。答案:(1)增大;减小(2)等于(3)210.5方法点:①从表中的数据可知,溶液中溶质的质量分数与溶液密度之间的关系,你发现了什么规律?②设加溶剂的质量为x,12%×100g=6%×(100g+x)x=100g。③稀释后氨水的体积为:(100g+100g)÷0.95g/mL=210.5mL随堂反馈1、下列操作会引起所配制的食盐溶液溶质质量分数降低的是()A、用托盘天平称量6.2g食盐固体,误将砝码放在左盘并使用游码B、称量时,两盘分别垫上大小质量相同的纸C、用量筒量水时,俯视凹液面的最低处读数D、将配好的溶液转移到试剂瓶时,不慎洒出2、在用固体氯化钠配制一定量一定溶质质量分数的氯化钠溶液的实验中,必须用到的一组仪器是()A、托盘天平、药匙、烧杯、玻璃棒、酒精灯B、量筒、烧杯、玻璃棒、药匙、酒精灯C、量筒、托盘天平、玻璃棒、药匙、烧杯D、烧杯、药匙、漏斗、玻璃棒3、汽车电瓶是一种铅蓄电池,它在充电、放电时发生的化学反应为:PbO2+Pb+2H2SO42PbSO4+2H2O铅蓄电池在使用一段时间后,常常需要补充“电瓶水”(即30%的硫酸溶液)。当铅蓄电池里剩余3.4千g20%的硫酸溶液时,应该加入Kg98%的浓硫酸,才能恰好配成30%的硫酸溶液。4、注射用链霉素试验针的药液配制方法如下:(1)把1.0g的链霉素溶于水制成4.0mL溶液①。(2)取0.1mL溶液①,加水稀释至1.0mL,得溶液②。(3)取0.1mL溶液②,加水稀释至1.0mL,得溶液③。(4)取0.1mL溶液③,加水稀释至1.0mL,即得试验针药液④。试求最终得到得试验针药液中溶质的质量分数。(由于整个过程中药液很稀,其密度可近似看做是1g/cm3)火眼金睛1、t℃时,有两瓶硝酸钾溶液,一瓶为饱和溶液(溶质的质量分数为40%),另一瓶为10%的溶液,下列实验操作无法区分这两种溶液的是()A、加一定量的水B、加入少量硝酸钾晶体C、降低温度D、t℃时,蒸发少量水2、人体的胃液含有少量的盐酸,下列图象正确的反应人喝水与胃液的溶质的质量分数的关系的变化的是()3、4岁的大雄耳朵有点痛,需要服用扑热息痛糖浆或滴剂(二者的作用相同),而家里只有扑热息痛滴剂。对于一个4岁的儿童来说,服用糖浆的安全用量为6mL(见下图)。则服用多少mL的滴剂等于服用了6mL的糖浆()A、3mLB、6mLC、9mLD、12mL4、海水淡化可采用膜分离技术。如右图所示,对淡化膜右侧的海水加压,水分子可以透过淡化膜进入左侧水池,而海水中的各种离子不能捅咕淡化膜,从而得到淡水。对加压后右侧海水成分变化进行分析,正确的是()A、溶质质量增加B、溶剂质量减少C、溶液质量不变D

和裕****az
 实名认证
实名认证
 内容提供者
内容提供者
最近下载


















