

如果您无法下载资料,请参考说明:
1、部分资料下载需要金币,请确保您的账户上有足够的金币
2、已购买过的文档,再次下载不重复扣费
3、资料包下载后请先用软件解压,在使用对应软件打开
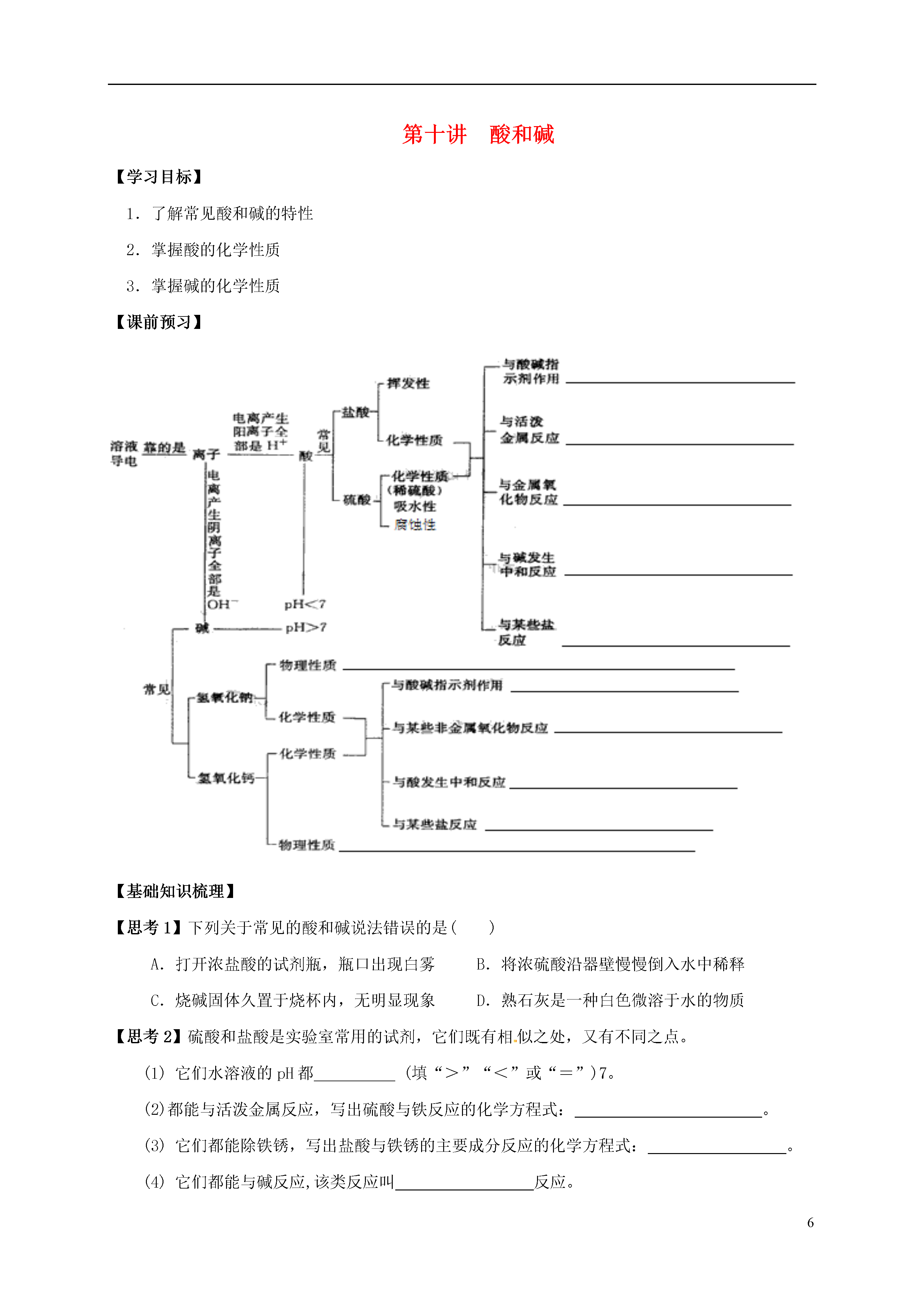
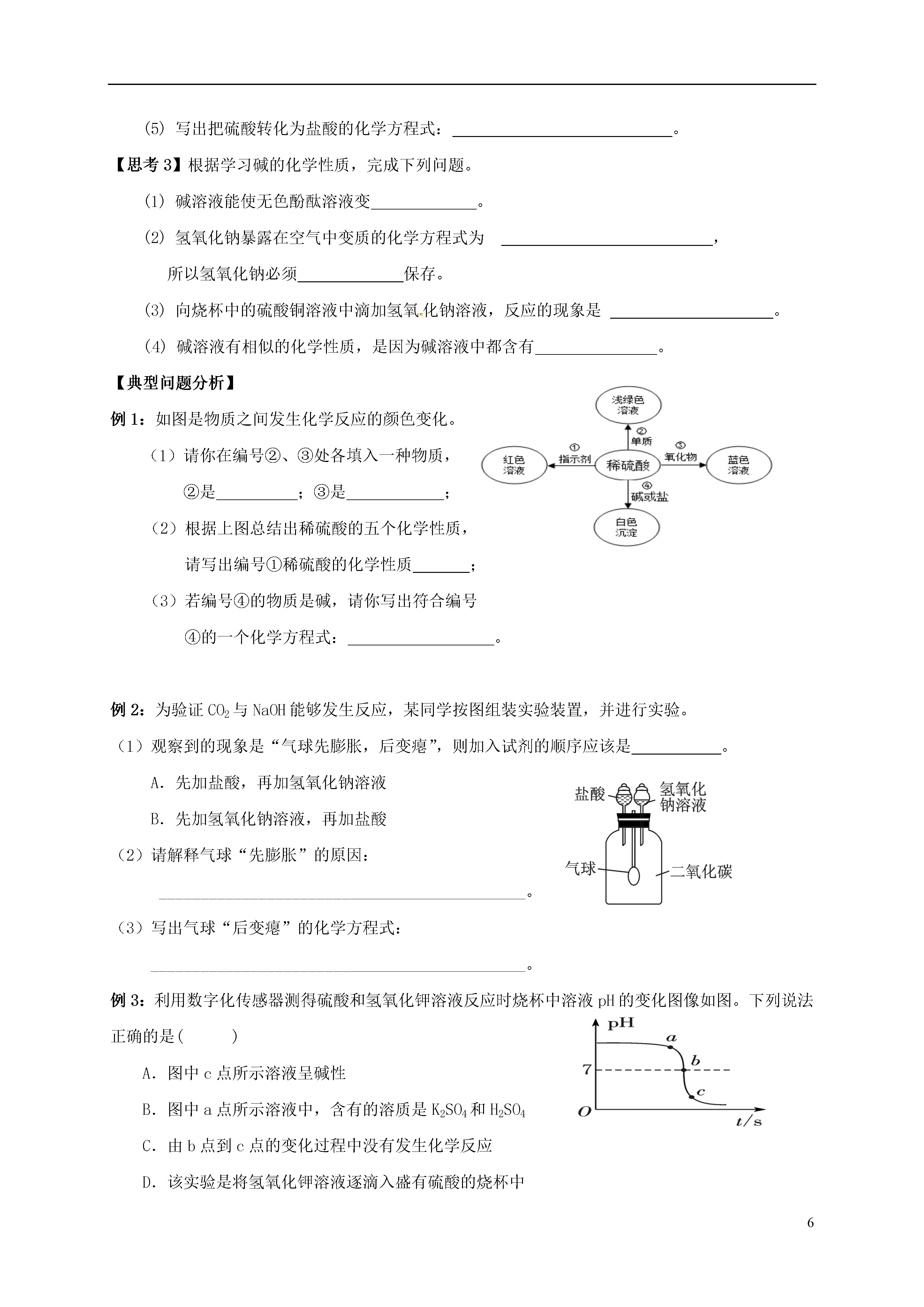
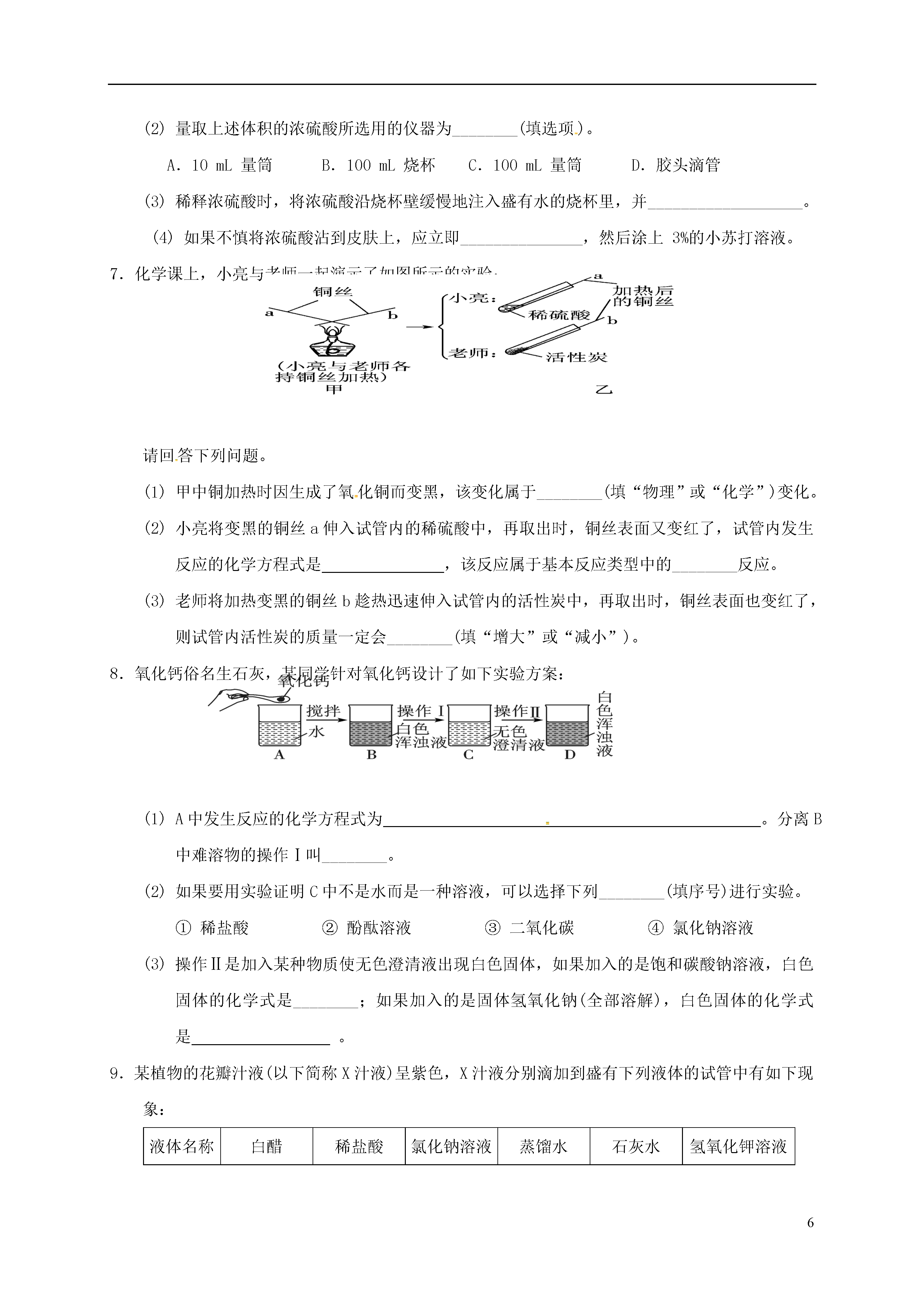
6第十讲酸和碱【学习目标】1.了解常见酸和碱的特性2.掌握酸的化学性质3.掌握碱的化学性质【课前预习】【基础知识梳理】【思考1】下列关于常见的酸和碱说法错误的是()A.打开浓盐酸的试剂瓶,瓶口出现白雾B.将浓硫酸沿器壁慢慢倒入水中稀释C.烧碱固体久置于烧杯内,无明显现象D.熟石灰是一种白色微溶于水的物质【思考2】硫酸和盐酸是实验室常用的试剂,它们既有相似之处,又有不同之点。(1)它们水溶液的pH都(填“>”“<”或“=”)7。(2)都能与活泼金属反应,写出硫酸与铁反应的化学方程式:。(3)它们都能除铁锈,写出盐酸与铁锈的主要成分反应的化学方程式:。(4)它们都能与碱反应,该类反应叫反应。(5)写出把硫酸转化为盐酸的化学方程式:。【思考3】根据学习碱的化学性质,完成下列问题。(1)碱溶液能使无色酚酞溶液变。(2)氢氧化钠暴露在空气中变质的化学方程式为,所以氢氧化钠必须保存。(3)向烧杯中的硫酸铜溶液中滴加氢氧化钠溶液,反应的现象是。(4)碱溶液有相似的化学性质,是因为碱溶液中都含有。【典型问题分析】例1:如图是物质之间发生化学反应的颜色变化。(1)请你在编号②、③处各填入一种物质,②是;③是;(2)根据上图总结出稀硫酸的五个化学性质,请写出编号①稀硫酸的化学性质;(3)若编号④的物质是碱,请你写出符合编号④的一个化学方程式:。例2:为验证CO2与NaOH能够发生反应,某同学按图组装实验装置,并进行实验。(1)观察到的现象是“气球先膨胀,后变瘪”,则加入试剂的顺序应该是。A.先加盐酸,再加氢氧化钠溶液B.先加氢氧化钠溶液,再加盐酸(2)请解释气球“先膨胀”的原因:_____________________________________________。(3)写出气球“后变瘪”的化学方程式:______________________________________________。例3:利用数字化传感器测得硫酸和氢氧化钾溶液反应时烧杯中溶液pH的变化图像如图。下列说法正确的是()A.图中c点所示溶液呈碱性B.图中a点所示溶液中,含有的溶质是K2SO4和H2SO4C.由b点到c点的变化过程中没有发生化学反应D.该实验是将氢氧化钾溶液逐滴入盛有硫酸的烧杯中【课堂小结】【课后作业】1.物质存放在烧杯中一段时间后,质量变大且变质的是()①浓盐酸②浓硫酸③烧碱④生石灰⑤澄清石灰水A.③④⑤B.②③④⑤C.①②③④⑤D.④⑤2.下列物质常用于改良酸性土壤的是()A.熟石灰B.烧碱C.食盐D.大理石3.向一定质量的甲中逐渐加入乙至过量,此过程中溶液的溶质总质量与加入乙的质量之间的关系,能用如图曲线表示的是()选项甲乙A稀硫酸氢氧化钠溶液B稀盐酸碳酸钙粉末C稀盐酸锌粒D硝酸银溶液铜粉4.下列食物的近似pH如下,其中酸性最强的是()A.柠檬汁:2.2~2.4B.番茄汁:4.0~4.4C.牛奶:6.3~6.6D.鸡蛋清:7.6~8.05.厕所清洁剂的主要成分是盐酸,炉具清洁剂的主要成分是氢氧化钠。关于这两种清洁剂的叙述正确的是()A.测得厕所清洁剂的pH=13B.测得炉具清洁剂的pH=1C.厕所清洁剂能使紫色石蕊溶液变蓝D.炉具清洁剂能使无色酚酞溶液变红6.硫酸是工农业生产中使用非常广泛的一种试剂,实验室用质量分数为98%的浓硫酸(密度为1.84g/cm3)配制49g质量分数为20%的硫酸。(1)经计算,所用水的质量为________g,所需98%的浓硫酸的体积约为________mL。(2)量取上述体积的浓硫酸所选用的仪器为________(填选项)。A.10mL量筒B.100mL烧杯C.100mL量筒D.胶头滴管(3)稀释浓硫酸时,将浓硫酸沿烧杯壁缓慢地注入盛有水的烧杯里,并___________________。(4)如果不慎将浓硫酸沾到皮肤上,应立即_______________,然后涂上3%的小苏打溶液。7.化学课上,小亮与老师一起演示了如图所示的实验:请回答下列问题。(1)甲中铜加热时因生成了氧化铜而变黑,该变化属于________(填“物理”或“化学”)变化。(2)小亮将变黑的铜丝a伸入试管内的稀硫酸中,再取出时,铜丝表面又变红了,试管内发生反应的化学方程式是,该反应属于基本反应类型中的________反应。(3)老师将加热变黑的铜丝b趁热迅速伸入试管内的活性炭中,再取出时,铜丝表面也变红了,则试管内活性炭的质量一定会________(填“增大”或“减小”)。8.氧化钙俗名生石灰,某同学针对氧化钙设计了如下实验方案:(1)A中发生反应的化学方程式为。分离

一吃****春晓
 实名认证
实名认证
 内容提供者
内容提供者
最近下载


















