试题-安徽-2015_安徽省2015中考化学考点拓展(打包14套).rar
安徽省2015中考化学考点拓展 基本实验操作.doc
预览
安徽省2015中考化学考点拓展 工业流程(框图)题.doc
预览
安徽省2015中考化学考点拓展 常见气体的制取.doc
预览
安徽省2015中考化学考点拓展 影响因素的探究.doc
预览
安徽省2015中考化学考点拓展 溶解度及溶解度曲线.doc
预览
安徽省2015中考化学考点拓展 物质性质的探究.doc
预览
安徽省2015中考化学考点拓展 物质成分的探究.doc
预览
安徽省2015中考化学考点拓展 特殊现象的探究.doc
预览
安徽省2015中考化学考点拓展 计算题.doc
预览
河南省2015中考化学考点拓展 常见气体的制备.doc
预览
河南省2015中考化学考点拓展 溶解度曲线及其应用.doc
预览
河南省2015中考化学考点拓展 物质的转化与推断.doc
预览
河南省2015中考化学考点拓展 综合应用题.doc
预览
河南省2015中考化学考点拓展 质量守恒定律的应用.doc
预览
如果您无法下载资料,请参考说明:
1、部分资料下载需要金币,请确保您的账户上有足够的金币
2、已购买过的文档,再次下载不重复扣费
3、资料包下载后请先用软件解压,在使用对应软件打开
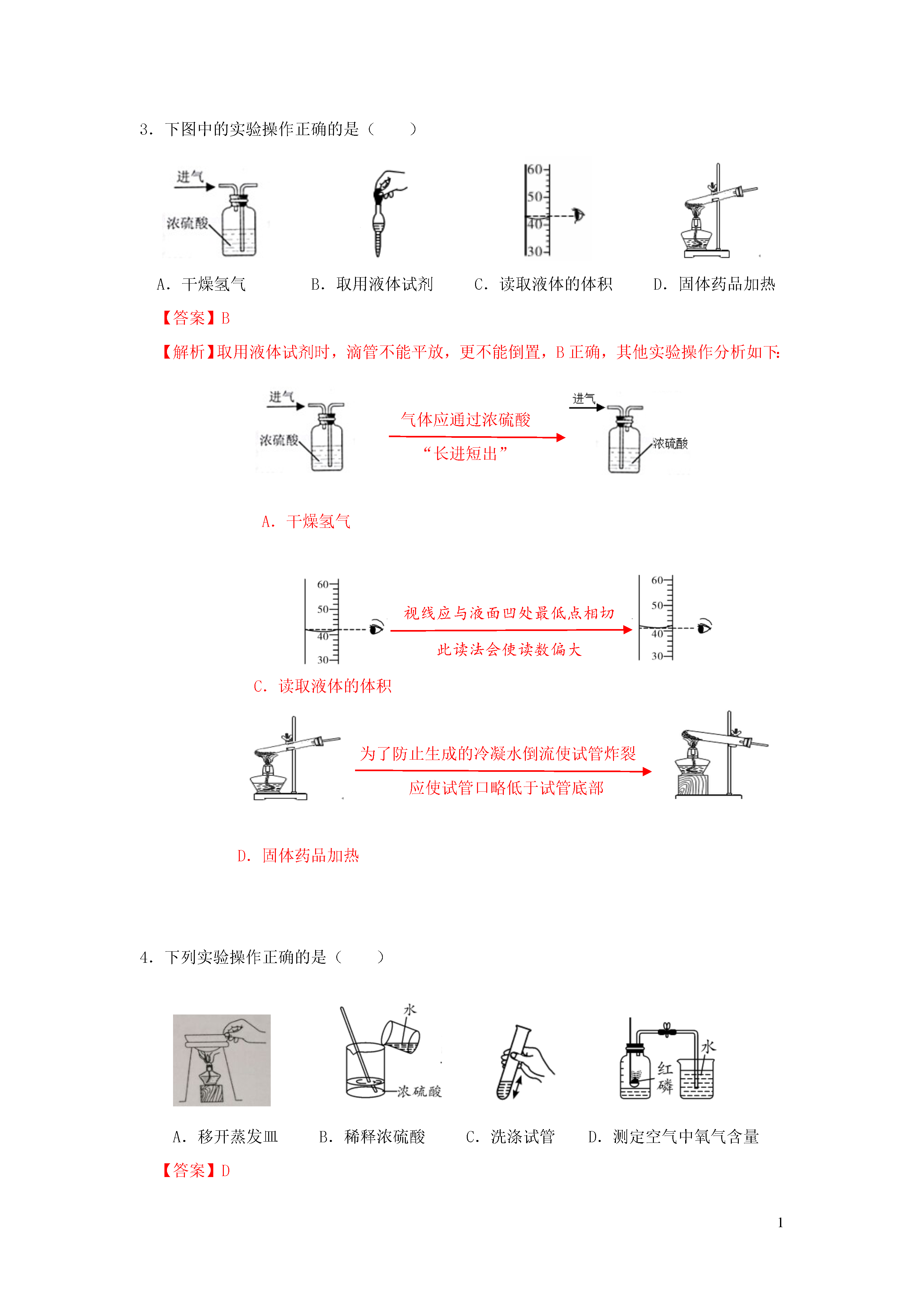
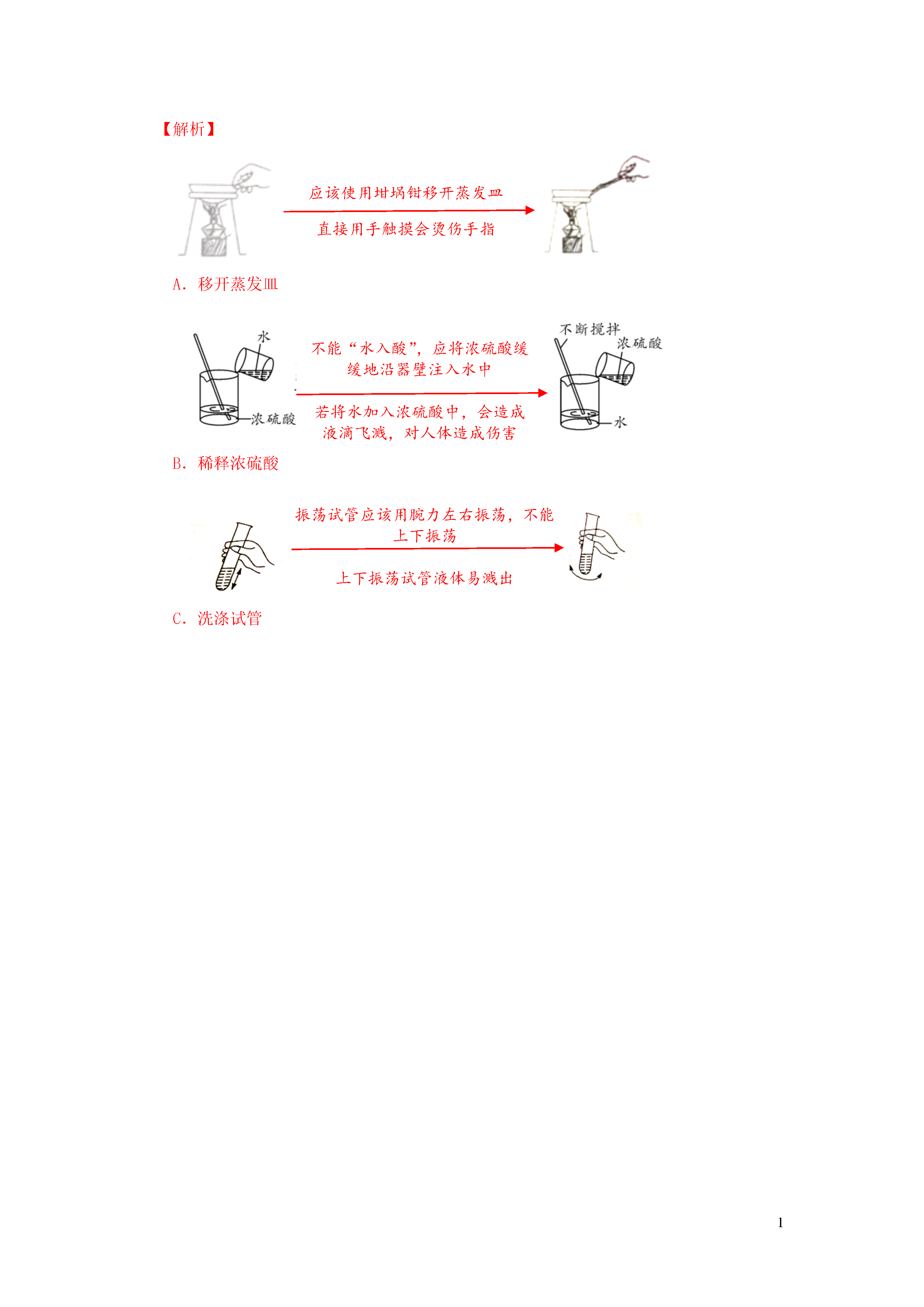
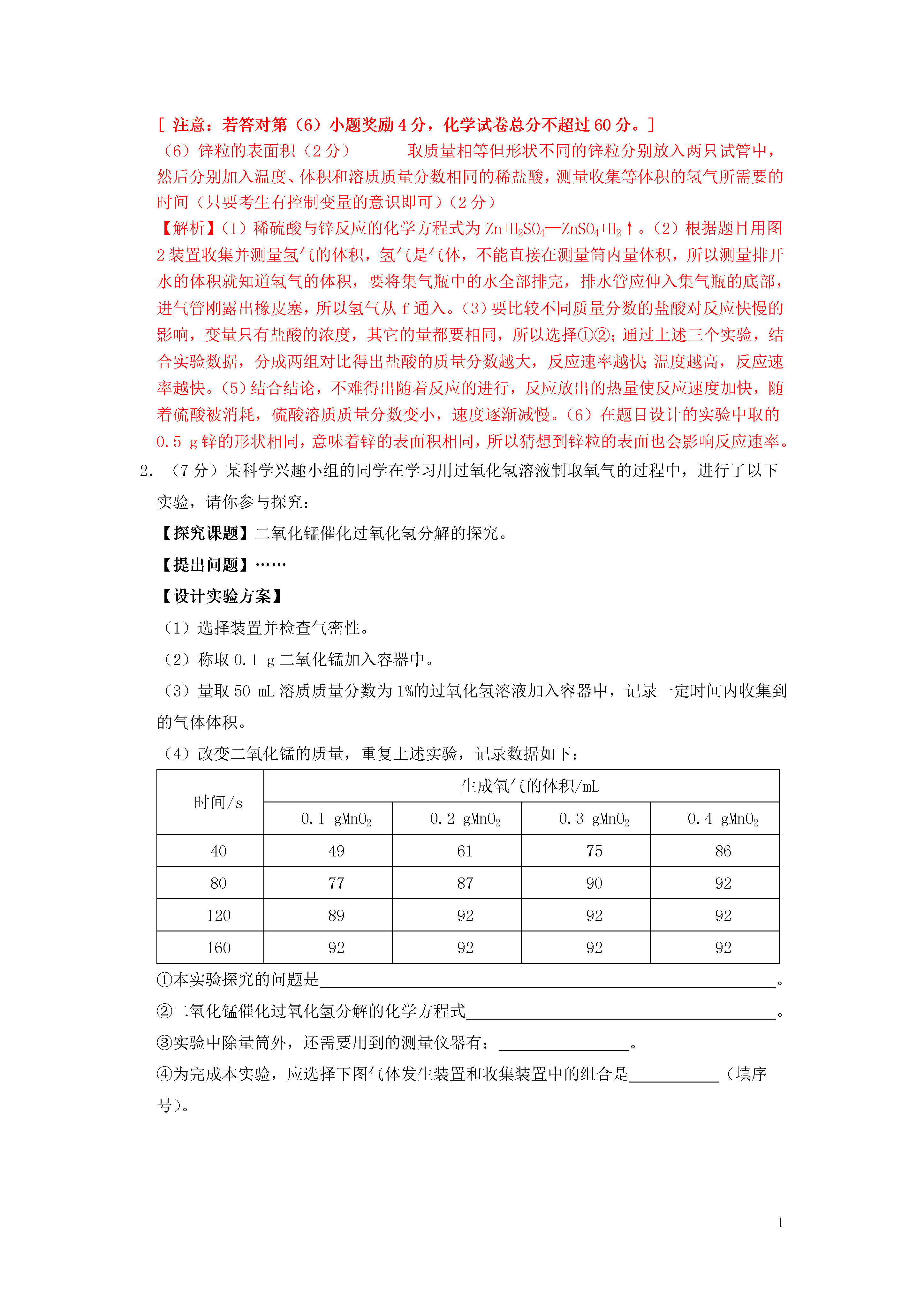
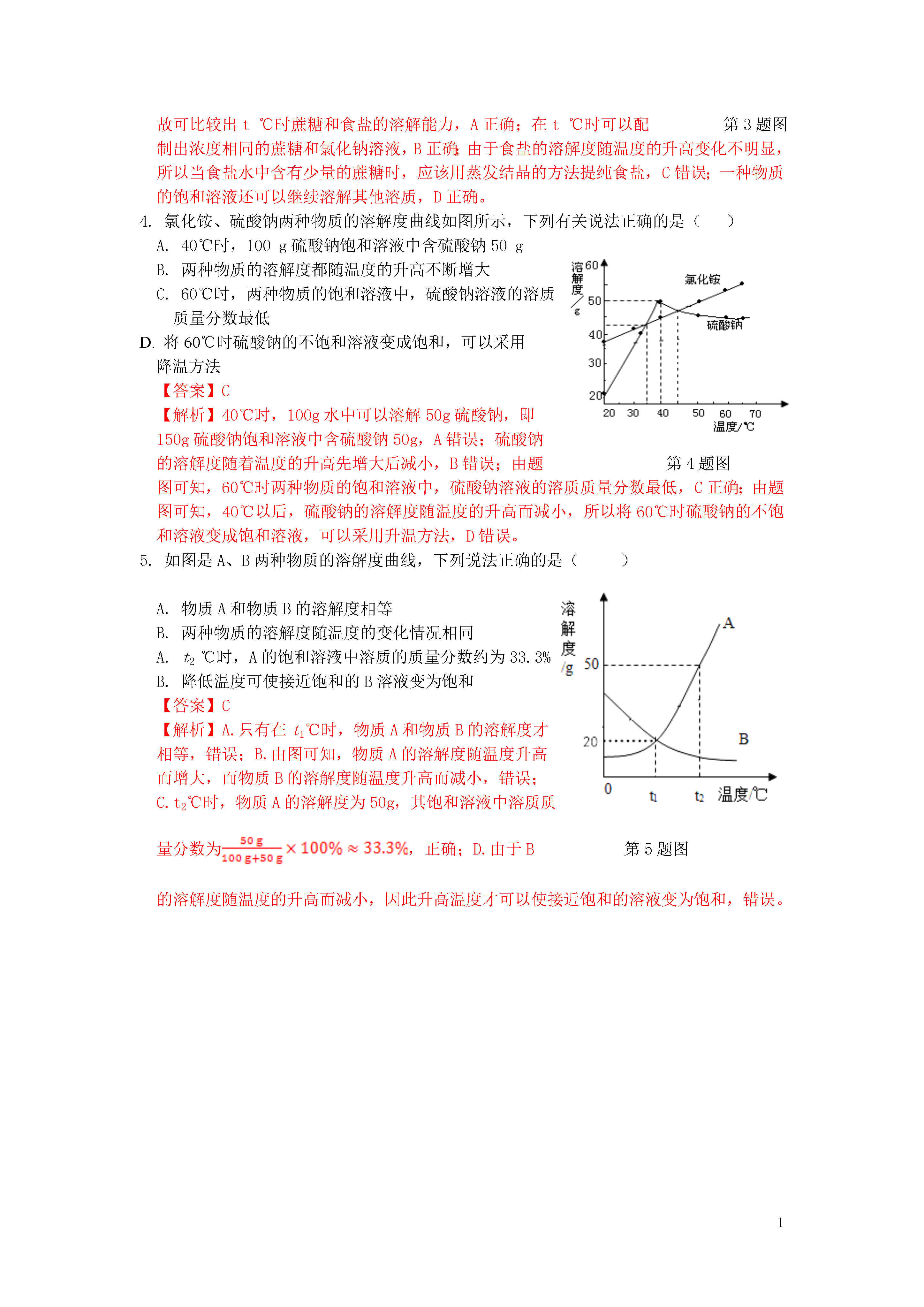
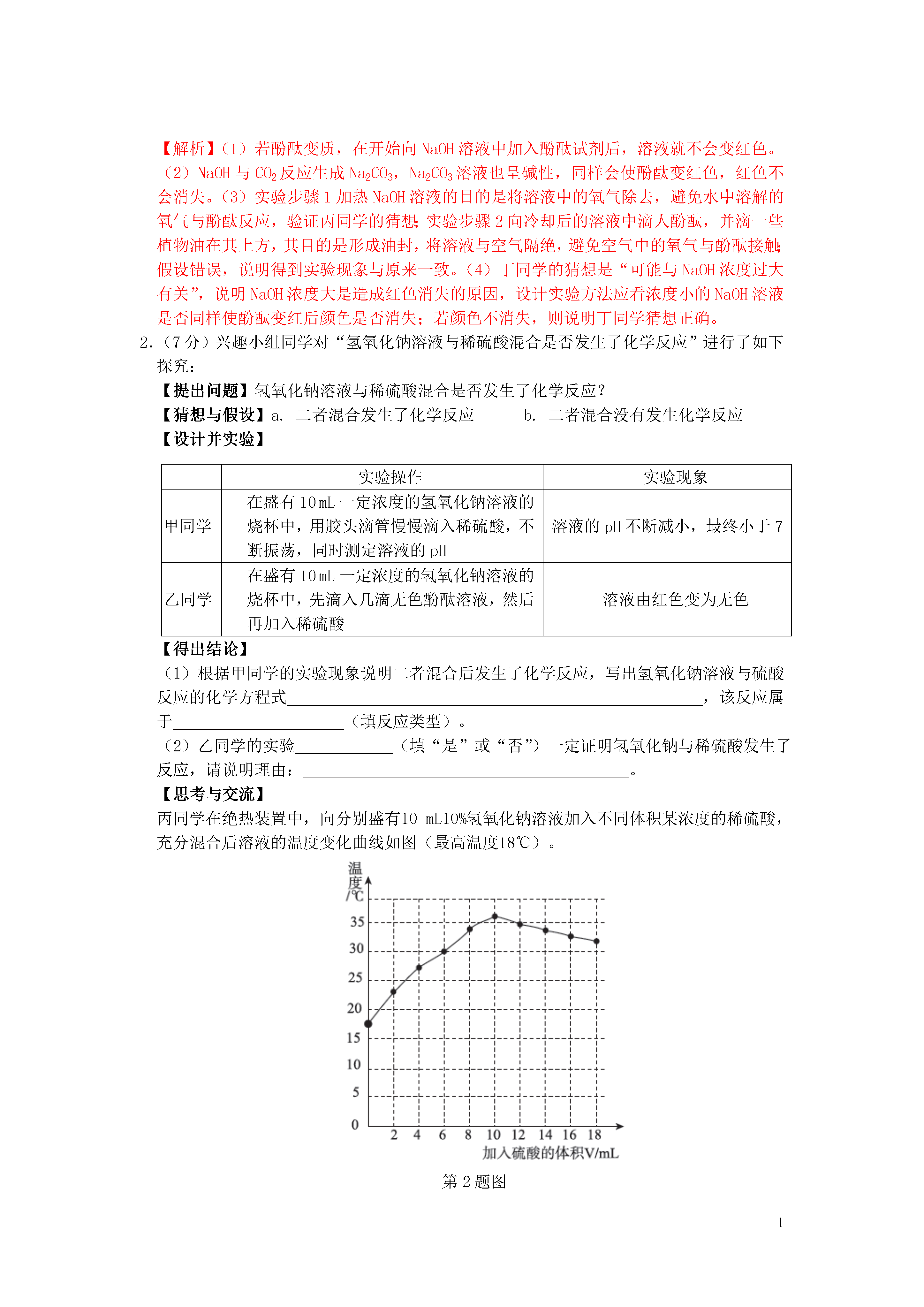
1基本实验操作1.下列实验操作错误的是()A.闻药品气味B.熄灭酒精灯C.称量固体质量D.氧气的验满【答案】C【解析】称量固体时,应遵循“左物右码”的原则,取用砝码时应用镊子而不能直接用手,否则易腐蚀砝码,C错误。2.下列实验操作正确的是()A.收集二氧化碳B.加热液体C.铁丝在氧气中燃烧D.塞紧橡皮塞【答案】C【解析】二氧化碳的密度比空气大,收集方法时是长进短出短进长出容易引入杂质,导致收集气体不纯A.收集二氧化碳试管中液体的体积应少于试管容积的1/3容易使液体飞溅,造成危险B.加热液体应该左手拿试管,右手拿橡皮塞,把橡皮塞慢慢转动塞进试管口不能放在桌上往下压,易将试管压碎D.塞紧橡皮塞3.下图中的实验操作正确的是()A.干燥氢气B.取用液体试剂C.读取液体的体积D.固体药品加热【答案】B【解析】取用液体试剂时,滴管不能平放,更不能倒置,B正确,其他实验操作分析如下:气体应通过浓硫酸“长进短出”A.干燥氢气视线应与液面凹处最低点相切此读法会使读数偏大C.读取液体的体积为了防止生成的冷凝水倒流使试管炸裂应使试管口略低于试管底部D.固体药品加热4.下列实验操作正确的是()A.移开蒸发皿B.稀释浓硫酸C.洗涤试管D.测定空气中氧气含量【答案】D【解析】应该使用坩埚钳移开蒸发皿直接用手触摸会烫伤手指A.移开蒸发皿不能“水入酸”,应将浓硫酸缓缓地沿器壁注入水中若将水加入浓硫酸中,会造成液滴飞溅,对人体造成伤害B.稀释浓硫酸振荡试管应该用腕力左右振荡,不能上下振荡上下振荡试管液体易溅出C.洗涤试管1工业流程(框图)题1.(6分)近年来有人提出了利用海水(含氯化钠)处理含二氧化硫的废气,该方法的流程如图所示。第1题图(1)写出氯化钠的一种用途。(2)根据流程图,写出②中吸收SO2的反应的化学方程式。(3)若要测定海水电解后所得溶液的pH,其方法是。(4)反应③中氢气在氯气中燃烧生成氯化氢气体,通过此反应,你对燃烧有什么新的认识?。(5)用海水处理二氧化硫的现实意义是。【答案】(1)作调味品(合理即可)(1分)(2)SO2+NaOH═NaHSO3(2分)(3)用玻璃棒蘸取少量电解后的溶液,滴在pH试纸上,将试纸显示的颜色与标准比色卡对照,读出溶液的pH(1分)(4)燃烧不一定要有氧气参与(1分)(5)吸收二氧化硫,减少酸雨的形成(合理即可)(1分)【解析】(1)氯化钠在生活和生产中有很多用途,如生活中氯化钠可作调味品,医疗上可用于配制生理盐水,农业上用氯化钠溶液来选种等等。(2)根据反应②,二氧化硫与氢氧化钠反应生成NaHSO3。(3)测定溶液pH的方法是用玻璃棒蘸取少量待测液,滴在pH试纸上,将试纸显示的颜色与标准比色卡对照,读出溶液的pH。(4)氢气在氯气中燃烧没有氧气参加,说明燃烧不一定需要氧气参与。(5)二氧化硫是大气污染物之一,会引起酸雨的形成,用海水处理二氧化硫可减少大气污染。2.(7分)有一种工业废水,已知其中含有大量硫酸亚铁,少量硫酸铜和硫酸钠。现设计一种既经济又合理的方法回收金属铜和硫酸亚铁晶体,其主要流程如图所示:第2题图(1)写出工业废水中加入铁粉后发生的反应的化学方程式,加入铁粉后进行过滤,用到的玻璃仪器有烧杯、漏斗和。(2)加入稀硫酸并进行操作Ⅰ的目的是。A.分离出铜和增加滤液①B.除去过量的铁粉和分离出铜C.除去过量的铁粉和增加滤液①实验室稀释浓硫酸的具体操作为。(4)操作Ⅱ是蒸发浓缩、、过滤,过滤后所得滤液的一种用途:。【答案】(1)Fe+CuSO4═FeSO4+Cu(2分)玻璃棒(1分)(2)B(1分)(3)将浓硫酸沿烧杯壁缓缓注入水中,并用玻璃棒不断进行搅拌(1分)(4)降温结晶(或冷却结晶)(1分)制备钠盐(其他合理答案均可)(1分)【解析】(1)根据实验目的要收集铜和硫酸亚铁,所以应加入过量的铁来置换出铜,铁和硫酸铜反应生成了铜和硫酸亚铁,可以写出该反应的化学方程式为Fe+CuSO4═FeSO4+Cu;过滤用到的玻璃仪器有烧杯、漏斗、玻璃棒。(2)由于加入过量的铁,所以为了将铁转化为硫酸亚铁,应该加入稀硫酸来将多余的铁反应掉,同时可得到较纯的铜,故该实验的目的是除去过量的铁粉和分离出铜。(3)稀释浓硫酸的具体操作为将浓硫酸沿烧杯壁缓缓注入水中,并用玻璃棒不断进行搅拌。(4)用滤液①和硫酸亚铁溶液得到硫酸亚铁晶体的操作为先蒸发浓缩然后降温使硫酸亚铁从溶液中结晶出来,然后过滤使硫酸亚铁晶体和液体进行分离。操作Ⅱ后所得滤液中主要含有的溶质为硫酸钠、过量的硫酸和没有结晶完全的硫酸亚铁,其可用于制备钠

雨巷****珺琦
 实名认证
实名认证
 内容提供者
内容提供者
最近下载