

如果您无法下载资料,请参考说明:
1、部分资料下载需要金币,请确保您的账户上有足够的金币
2、已购买过的文档,再次下载不重复扣费
3、资料包下载后请先用软件解压,在使用对应软件打开
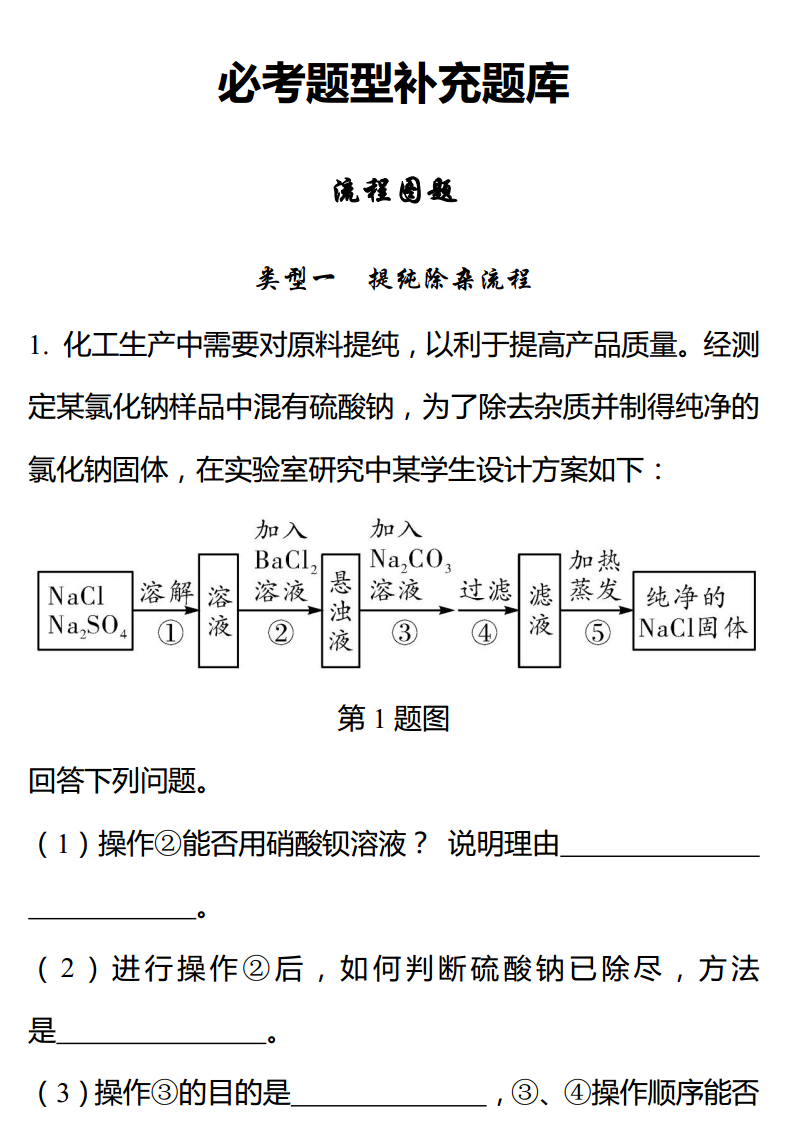
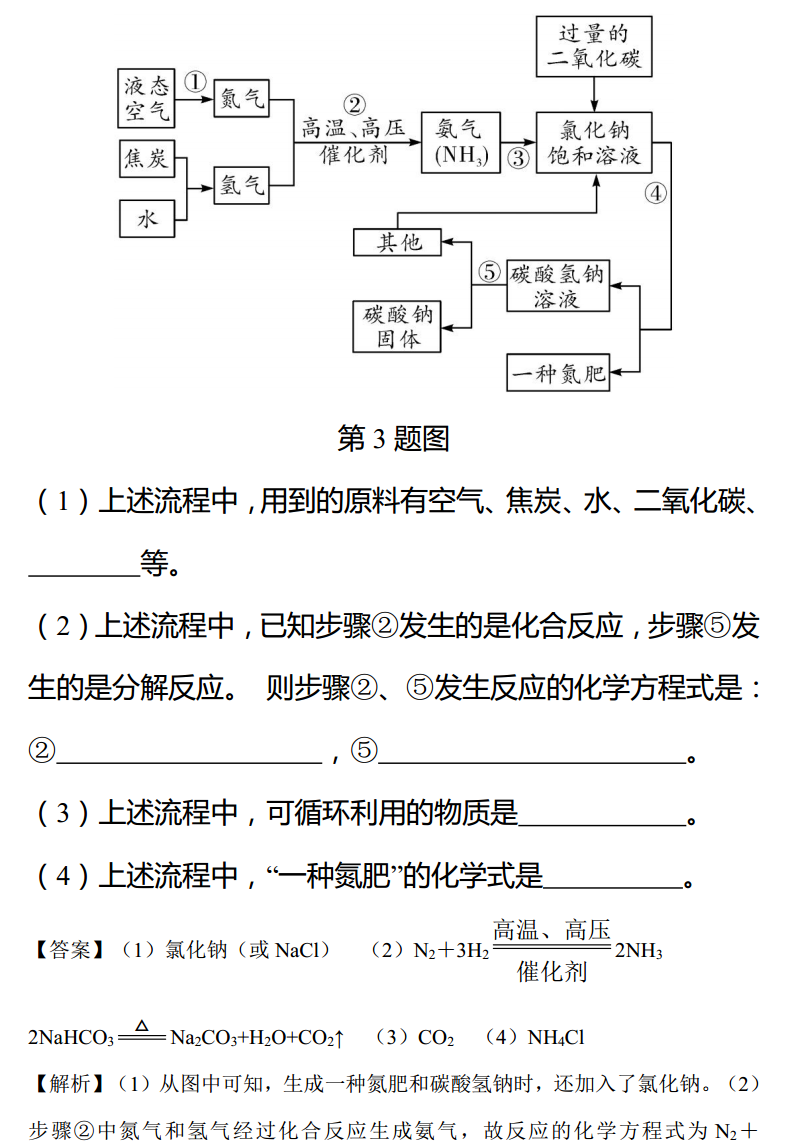
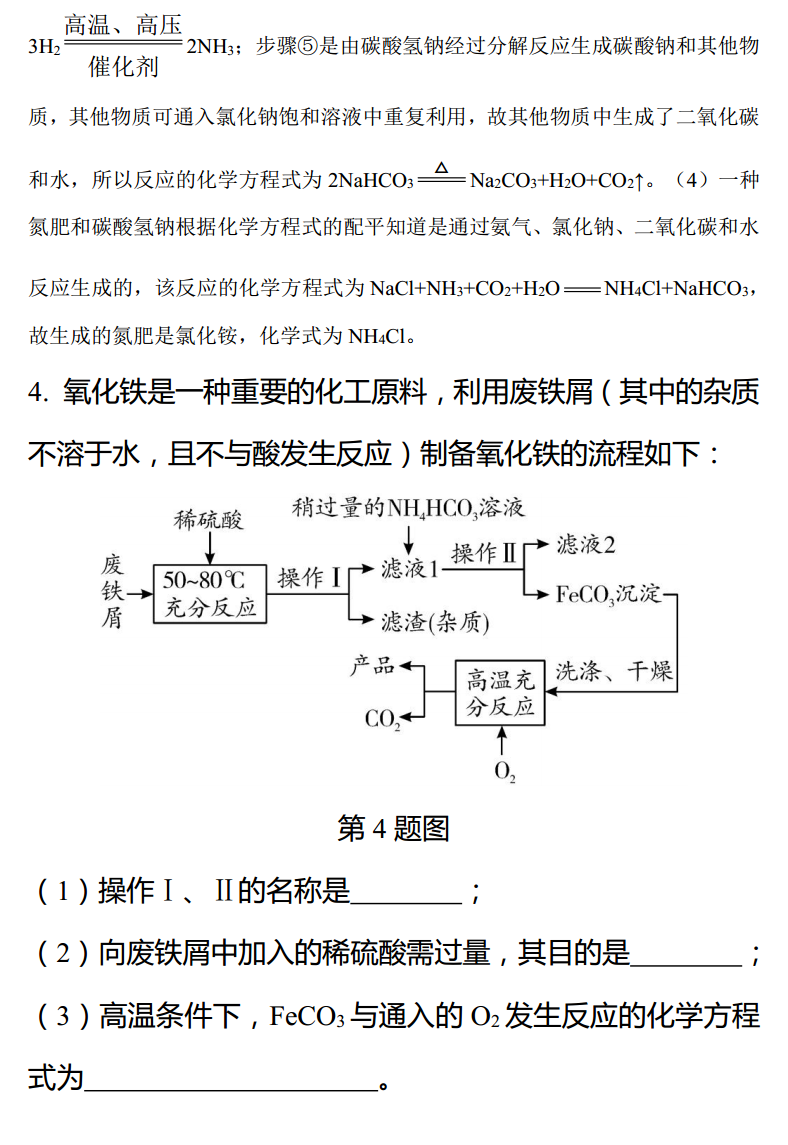
必考题型补充题库流程图题类型一提纯除杂流程1.化工生产中需要对原料提纯,以利于提高产品质量。经测定某氯化钠样品中混有硫酸钠,为了除去杂质并制得纯净的氯化钠固体,在实验室研究中某学生设计方案如下:第1题图回答下列问题。(1)操作②能否用硝酸钡溶液?说明理由。(2)进行操作②后,如何判断硫酸钠已除尽,方法是。(3)操作③的目的是,③、④操作顺序能否交换,其理由是。(4)此设计方案是否严密,说明理由。【答案】(1)不能,会引入新的杂质硝酸钠无法除去(2)取上层清液于试管中,滴加氯化钡溶液,看是否有沉淀生成(3)使钡离子完全沉淀不能,交换后得不到滤液(4)不严密,过量的碳酸钠没有除去【解析】(1)硝酸钡溶液和硫酸钠反应生成硫酸钡沉淀和硝酸钠,新的杂质硝酸钠会引入,所以不能用硝酸钡溶液。(2)氯化钡和硫酸钠溶液反应会生成硫酸钡沉淀和氯化钠,所以判断硫酸钠是否除尽,方法是取上层清液于试管中,滴加氯化钡溶液,看是否有沉淀生成。(3)碳酸钠和氯化钡反应生成碳酸钡沉淀和氯化钠,所以操作③的目的是使钡离子完全沉淀;③、④操作顺序不能交换,其理由是得不到滤液。(4)最后新引入的碳酸钠没有除去,所以此设计方案不严密。2.氯化钾固体样品中混有少量碳酸钾和硫酸钾两种杂质。为了获得纯净的氯化钾,将样品溶解。按如图所示步骤进行提纯,已知试剂Ⅰ为氯化钡溶液。B、C为固体难溶物,每个步骤加稍过量的试剂。第2题图(1)固体难溶物B含有碳酸钡和。(2)检验步骤①已除去杂质的方法(操作、现象、结论)是。(3)试剂Ⅱ中溶质的化学式,试剂Ⅲ的名称是。(4)由E获得氯化钾晶体的分离操作名是。【答案】(1)硫酸钡(或BaSO4)(2)取少量A溶液(反应后所得上清液),加氯化钡溶液,如果没有白色沉淀生成,则说明杂质已被除去(其他合理答案即可)(3)K2CO3盐酸(4)蒸发结晶类型二生产流程3.侯德榜是我国著名的化学家,为纯碱和氮肥工业技术的发展作出了杰出的贡献。他发明的侯氏制碱法大大提高了原料的利用率。其工业流程大致如下:第3题图(1)上述流程中,用到的原料有空气、焦炭、水、二氧化碳、等。(2)上述流程中,已知步骤②发生的是化合反应,步骤⑤发生的是分解反应。则步骤②、⑤发生反应的化学方程式是:②,⑤。(3)上述流程中,可循环利用的物质是。(4)上述流程中,“一种氮肥”的化学式是。高温、高压【答案】(1)氯化钠(或NaCl)(2)N2+3H22NH3催化剂2NaHCO3Na2CO3+H2O+CO2↑(3)CO2(4)NH4Cl【解析】(1)从图中可知,生成一种氮肥和碳酸氢钠时,还加入了氯化钠。(2)步骤②中氮气和氢气经过化合反应生成氨气,故反应的化学方程式为N2+高温、高压3H22NH3;步骤⑤是由碳酸氢钠经过分解反应生成碳酸钠和其他物催化剂质,其他物质可通入氯化钠饱和溶液中重复利用,故其他物质中生成了二氧化碳和水,所以反应的化学方程式为2NaHCO3Na2CO3+H2O+CO2↑。(4)一种氮肥和碳酸氢钠根据化学方程式的配平知道是通过氨气、氯化钠、二氧化碳和水反应生成的,该反应的化学方程式为NaCl+NH3+CO2+H2ONH4Cl+NaHCO3,故生成的氮肥是氯化铵,化学式为NH4Cl。4.氧化铁是一种重要的化工原料,利用废铁屑(其中的杂质不溶于水,且不与酸发生反应)制备氧化铁的流程如下:第4题图(1)操作Ⅰ、Ⅱ的名称是;(2)向废铁屑中加入的稀硫酸需过量,其目的是;(3)高温条件下,FeCO3与通入的O2发生反应的化学方程式为。高温【答案】(1)过滤(2)将废铁屑中铁完全反应(3)4FeCO3+O22Fe2O3+4CO2【解析】(1)依据操作Ⅰ、Ⅱ后得到的都是固体和液体,可推出,这两步操作都是过滤;(2)过量的稀硫酸有利于废铁屑中铁完全反应;(3)高温条件下,FeCO3与通入的O2发生反应,生成Fe2O3和CO2,该反应的化学方程式是4FeCO3高温+O22Fe2O3+4CO2。类型三废气、废液处理流程5.某工厂产生的废水中含有硫酸锌和少量的硫酸铜以及污泥,为了变废为宝,利用废水制取七水硫酸锌(ZnSO4·7H2O),其工艺流程图如下:第5题图回答下列问题:(1)步骤①的操作名称。(2)步骤②需加入过量的物质是,目的是。(3)步骤③需加入的溶液是。(4)步骤④的操作是蒸发浓缩,,过滤。【答案】(1)过滤(2)锌除去少量的硫酸铜杂质(3)

戊午****jj
 实名认证
实名认证
 内容提供者
内容提供者
最近下载


















