


如果您无法下载资料,请参考说明:
1、部分资料下载需要金币,请确保您的账户上有足够的金币
2、已购买过的文档,再次下载不重复扣费
3、资料包下载后请先用软件解压,在使用对应软件打开
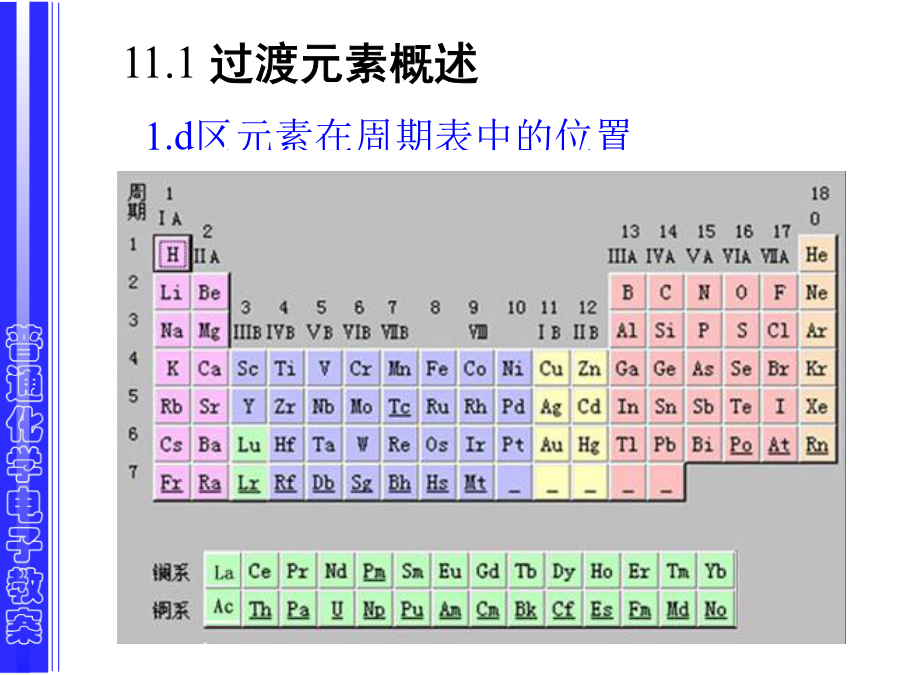
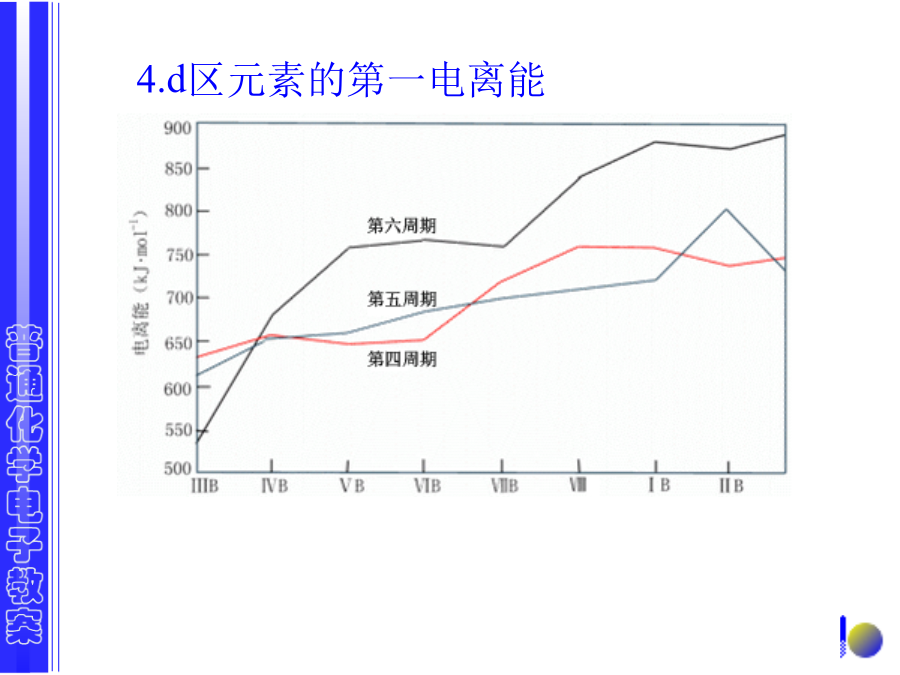
第十一章过渡元素11.1过渡元素概述3.d区元素的原子半径总趋势:同周期左右由小大,幅度不大。 同副族不规律。5过渡元素的物理性质熔点变化示意图过渡元素的氧化态过渡元素离子的颜色§11.2过渡元素的单质表11-1d区元素在地壳中的存在形式和丰度钛铬分族(VIB):Cr,Mo,W,Sg锰分族(VIIB):MnTcReBh 价电子构型:(n-1)d5ns2与氧、卤素等非金属反应:锰的存在与制备:Ⅷ族FeCoNi铁系 RuRhPd OsIrPt铁、钴、镍的单质3.与非金属反应铜族元素(ⅠB):Cu,Ag,Au 价电子构型:(n-1)d10ns11.物理性质2.化学性质(2)与X2作用硫脲所以不可用铜器盛氨水。与氧化性酸作用锌族元素的单质熔点低: Zn:419℃,Cd:321℃,Hg:-39℃。 汞是室温下惟一的液态金属。 易形成合金 黄铜:Cu-Zn 汞齐:Na-Hg,Au-Hg,Ag-Hg 用于提取贵金属。单质的化学性质与S的作用与酸反应思考: 1.已知:EӨ(Zn2+/Zn)=-0.7621V,室温下锌不能从水中置换出H2,为什么?日常生活中如何利用锌的这一性质? 2.锌是否可以从碱液中置换出氢气? 试计算pH=14时,E(H+/H2)=?,EӨ([Zn(OH)4]2-/Zn)=?§11.3过渡元素的化合物11.3.1铬的化合物铬元素的电势图1000~1300℃(2)以K2Cr2O7为原料制备其他含铬化合物(3)Cr(Ⅵ)含氧酸及其离子在溶液中的转化(4)Cr(Ⅵ)的难溶盐O2.铬(Ⅲ)的化合物[Cr(H2O)6]3+[Cr(OH)(H2O)5]2++H+蓝色(5)Cr(Ⅲ)的配位性(6)Cr(Ⅲ),Cr(Ⅵ)的鉴定小结:11.3.2锰的化合物锰的重要化合物性质表水溶液中锰的各种离子及其性质锰元素电势图:1.锰(Ⅶ)的化合物②不稳定性2.锰(Ⅵ)的化合物制取低氧化值锰化合物的原料4.锰(Ⅱ)的化合物Mn2+的还原性弱小结:除Fe以外,最高氧化值都没有达到3d和4s电子数的总和。铁的重要化合物钴(Ⅱ)和镍(Ⅱ)的重要化合物Fe氧化性:Fe(Ⅲ)<Co(Ⅲ)<Ni(Ⅲ)铁、钴、镍的氧化物和氢氧化物2铁、钴、镍的氢氧化物氯化羟钴(碱式氯化钴)3.铁、钴、镍的盐(NH4)2Fe(SO4)2·6H2O(Mohr盐)淡绿色, CoSO4·7H2O淡紫色,CoCl2·6H2O粉红色, NiCl2·6H2O草绿色,NiSO4·7H2O暗绿色。 Ni(NO3)2·6H2O青绿色。(1)水溶液中水解Fe3+水解最终产物:Fe(OH)3粉红色红保存Fe2+溶液应加入Fe(4)FeCl3有明显的共价性,易潮解3.Fe(Ⅱ),Co(Ⅱ),Ni(Ⅱ)的硫化物1)铁的配合物K4[Fe(CN)6]黄血盐,黄色; K3[Fe(CN)6]赤血盐,晶体为红色。Prussian’s蓝[KFeⅢ(CN)6FeⅡ]x的结构为:用于鉴定S2-。Fe(Ⅲ)的配合物比Fe(Ⅱ)的配合物稳定, 相应电对的标准电极电势低于E(Fe3+/Fe2+)。 [Fe(phen)3]2+[Fe(phen)3]3+ 深红色蓝色2)钴的配合物Co(Ⅱ)的配合物分为两类,一类是粉红色的八面体配合物,另一类是蓝色的四面体配合物。蓝色四异硫氰合钴(Ⅱ)配离子蓝色Ni离子的鉴定小结:1.铜的化合物几种常见的铜的化合物:(1)铜(Ⅰ)的化合物CuCl>CuBr>CuI>CuSCN>CuCN>Cu2SCu(Ⅰ)配合物的配位数多为2,配体浓度 增大时,也可能形成配位数为3或4的配 合物。Cu(Ⅰ)配合物吸收CO和烯烃:Cu(Ⅰ)的沉淀物不易歧化(2)铜(Ⅱ)的化合物浅蓝I-CuSO4·5H2O的结构与性质Cu(Ⅱ)的配合物:多为4配位 Cu(Ⅱ)配合物不如Cu(Ⅰ)配合物稳定。 [CuCl4]2-[CuCl2]-2.银和金的化合物几种银和金的常见化合物热稳定性差具有颜色,显色机理为电荷迁移。 AgClAgBrAgIAg2OAg2CrO4Ag2S 白浅黄黄褐砖红黑(2)Ag(Ⅰ)离子的反应鉴定S2O32-:(3)Ag+的重要反应7(4)Ag+的鉴定思考: 已知:EӨ(I2/I-)=0.535V, EӨ(Ag+/Ag)=0.799V, 在Ag+溶液中加入I-时,为何不能把I-氧化为I2?11.3.5锌族元素的化合物ZnO既溶于酸又溶于碱。稀酸溶性硫化物(4)配合物(5)Zn2+的鉴定(碱性条件)Hg(Ⅰ)的化合物: Hg2Cl2,Hg2(NO3)2, 氯化亚汞(甘汞)硝酸亚汞 难溶于水易溶于水与S2-的反应Hg2+0.9083VHg22+0.7955VHg氨基氯化汞加有利于平衡右移4反之:可利用HgCl2鉴定Sn2+HgS:=1.6×10-52(4)汞的配合物

邻家****文章
 实名认证
实名认证
 内容提供者
内容提供者
最近下载
201651206021+莫武林+浅析在互联网时代下酒店的营销策略——以湛江民大喜来登酒店为例.doc
201651206021+莫武林+浅析在互联网时代下酒店的营销策略——以湛江民大喜来登酒店为例.doc
用于空间热电转换的耐高温涡轮发电机转子及其装配方法.pdf
用于空间热电转换的耐高温涡轮发电机转子及其装配方法.pdf
用于空间热电转换的耐高温涡轮发电机转子及其装配方法.pdf
用于空间热电转换的耐高温涡轮发电机转子及其装配方法.pdf
用于空间热电转换的耐高温涡轮发电机转子及其装配方法.pdf
用于空间热电转换的耐高温涡轮发电机转子及其装配方法.pdf
论《离骚》诠释史中的“香草”意蕴.docx
论《离骚》诠释史中的“香草”意蕴.docx


















