

如果您无法下载资料,请参考说明:
1、部分资料下载需要金币,请确保您的账户上有足够的金币
2、已购买过的文档,再次下载不重复扣费
3、资料包下载后请先用软件解压,在使用对应软件打开
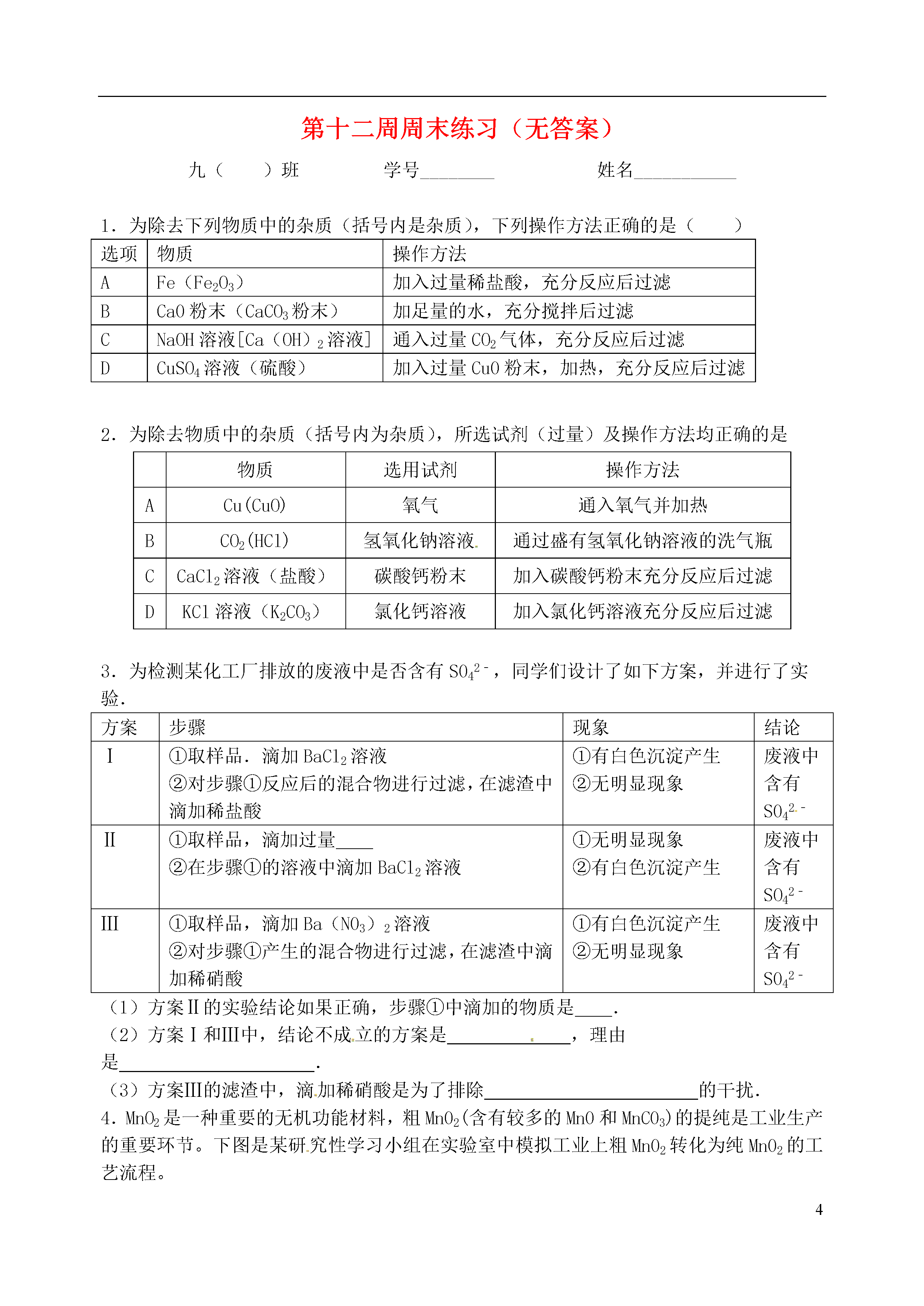
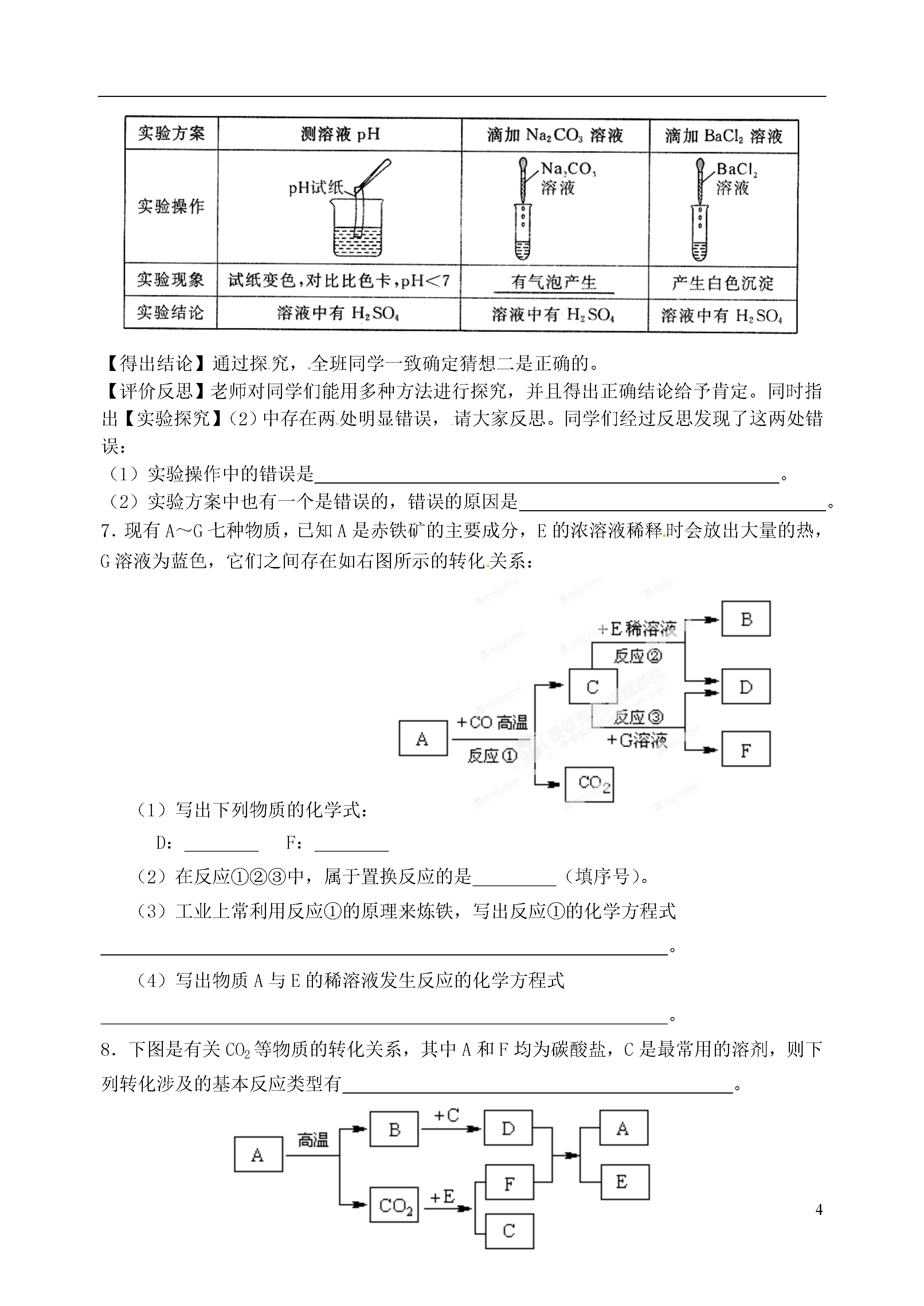
4第十二周周末练习(无答案)九()班学号________姓名___________1.为除去下列物质中的杂质(括号内是杂质),下列操作方法正确的是()选项物质操作方法AFe(Fe2O3)加入过量稀盐酸,充分反应后过滤BCa0粉末(CaCO3粉末)加足量的水,充分搅拌后过滤CNaOH溶液[Ca(OH)2溶液]通入过量CO2气体,充分反应后过滤DCuSO4溶液(硫酸)加入过量Cu0粉末,加热,充分反应后过滤2.为除去物质中的杂质(括号内为杂质),所选试剂(过量)及操作方法均正确的是物质选用试剂操作方法ACu(CuO)氧气通入氧气并加热BCO2(HCl)氢氧化钠溶液通过盛有氢氧化钠溶液的洗气瓶CCaCl2溶液(盐酸)碳酸钙粉末加入碳酸钙粉末充分反应后过滤DKCl溶液(K2CO3)氯化钙溶液加入氯化钙溶液充分反应后过滤3.为检测某化工厂排放的废液中是否含有S042﹣,同学们设计了如下方案,并进行了实验.方案步骤现象结论Ⅰ①取样品.滴加BaCl2溶液②对步骤①反应后的混合物进行过滤,在滤渣中滴加稀盐酸①有白色沉淀产生②无明显现象废液中含有S042﹣Ⅱ①取样品,滴加过量②在步骤①的溶液中滴加BaCl2溶液①无明显现象②有白色沉淀产生废液中含有SO42﹣Ⅲ①取样品,滴加Ba(N03)2溶液②对步骤①产生的混合物进行过滤,在滤渣中滴加稀硝酸①有白色沉淀产生②无明显现象废液中含有S042﹣(1)方案Ⅱ的实验结论如果正确,步骤①中滴加的物质是.(2)方案Ⅰ和Ⅲ中,结论不成立的方案是,理由是.(3)方案Ⅲ的滤渣中,滴加稀硝酸是为了排除的干扰.4.MnO2是一种重要的无机功能材料,粗Mn02(含有较多的Mn0和MnC03)的提纯是工业生产的重要环节。下图是某研究性学习小组在实验室中模拟工业上粗Mn02转化为纯Mn02的工艺流程。请回答下列问题:(1)操作A的名称是。(2)NaCl03中氯元素的化合价为价。(3)蒸发所需的仪器有铁架台(带铁圈)、蒸发皿、酒精灯和。(4)写出加稀H2SO4时产生C02的化学方程式。(5)该流程中可以循环利用的物质是H2SO4和。5.某工厂用电解饱和食盐水的方法生产氯气、烧碱、氢气等化工产品(反应的化学方程式:2NaCl+2H2O2NaOH+H2↑+Cl2↑),这种工业称为“氯碱工业”。某研究性学习小组对该厂生产的烧碱样品进行如下探究。Ⅰ.定性探究【提出问题】烧碱样品中可能含有哪些杂质?【猜想】猜想一:可能含有Na2C03,作出此猜想的依据是(用化学方程式表示)。猜想二:可能含有NaCl,作出此猜想的依据是(用简洁的文字表述)。【设计实验】实验步骤实验现象解释或结论①取适量烧碱样品置于试管中,加水溶解,并用手触摸试管外壁。试管外壁发热原因是②向①所得的溶液中逐滴加入稀硝酸至过量(学科网精校)一开始无明显现象,一段时间后产生能使澄清石灰水变浑浊的气体。样品中含有的杂质是③向②所得的溶液中滴加几滴硝酸银溶液产生白色沉淀样品中还含有的杂质是【交流与讨论】小明同学提出:“上述实验中稀硝酸也可以用稀盐酸代替”。你认为他的观点(填“正确”或“不正确”)。Ⅱ.定量探究【提出问题】烧碱样品中氢氧化钠的质量分数是多少呢?【设计实验】小婉同学设计探究方案后进行实验并测得数据如下:请你利用小婉同学测得的数据计算烧碱样品中氢氧化钠的质量分数(请列出计算过程)。【交流与反思】小强同学认为小婉同学设计的探究方案不够严密,其理由是:(1)探究方案中未考虑氢氧化钠的吸水性。(2)探究方案中因缺少(填操作名称),导致测得的氢氧化钠的质量分数偏小。6.某化学课堂围绕“酸碱中和反应”,将学生分成若干小组,在老师引导下开展探究活动。以下是教学片段,请你参与学习并帮助填写空格(包括表中空格)。【演示实验】将一定量的稀H2SO4加入到盛有NaOH溶液的小烧杯中。【学生板演】该反应的化学方程式。【提出问题】实验中未观察到明显现象,部分同学产生了疑问:反应后溶液中溶质是什么呢?【假设猜想】针对疑问,太家纷纷提出猜想。甲组同学的猜想如下:猜想一:只有Na2SO4猜想二:有Na2SO4和H2SO4猜想三:有Na2SO4和NaOH猜想四:有Na2SO4、H2SO4和NaOH乙组同学对以上猜想提出质疑,认为有一种猜想是不合理的。不合理的猜想是。【实验探究】(1)丙组同学取烧杯中的溶液少量于试管中,滴加几滴CuSO4溶液,无明显变化,溶液中一定没有。(2)为了验证其余猜想,各学习小组利用烧杯中的溶液,并选用老师提供的pH试纸、铜片、BaC12溶液、Na2CO3溶液,进行如下三个方案的探究。【得出结论】通过探究,全班同

玉军****la
 实名认证
实名认证
 内容提供者
内容提供者
最近下载


















