



如果您无法下载资料,请参考说明:
1、部分资料下载需要金币,请确保您的账户上有足够的金币
2、已购买过的文档,再次下载不重复扣费
3、资料包下载后请先用软件解压,在使用对应软件打开
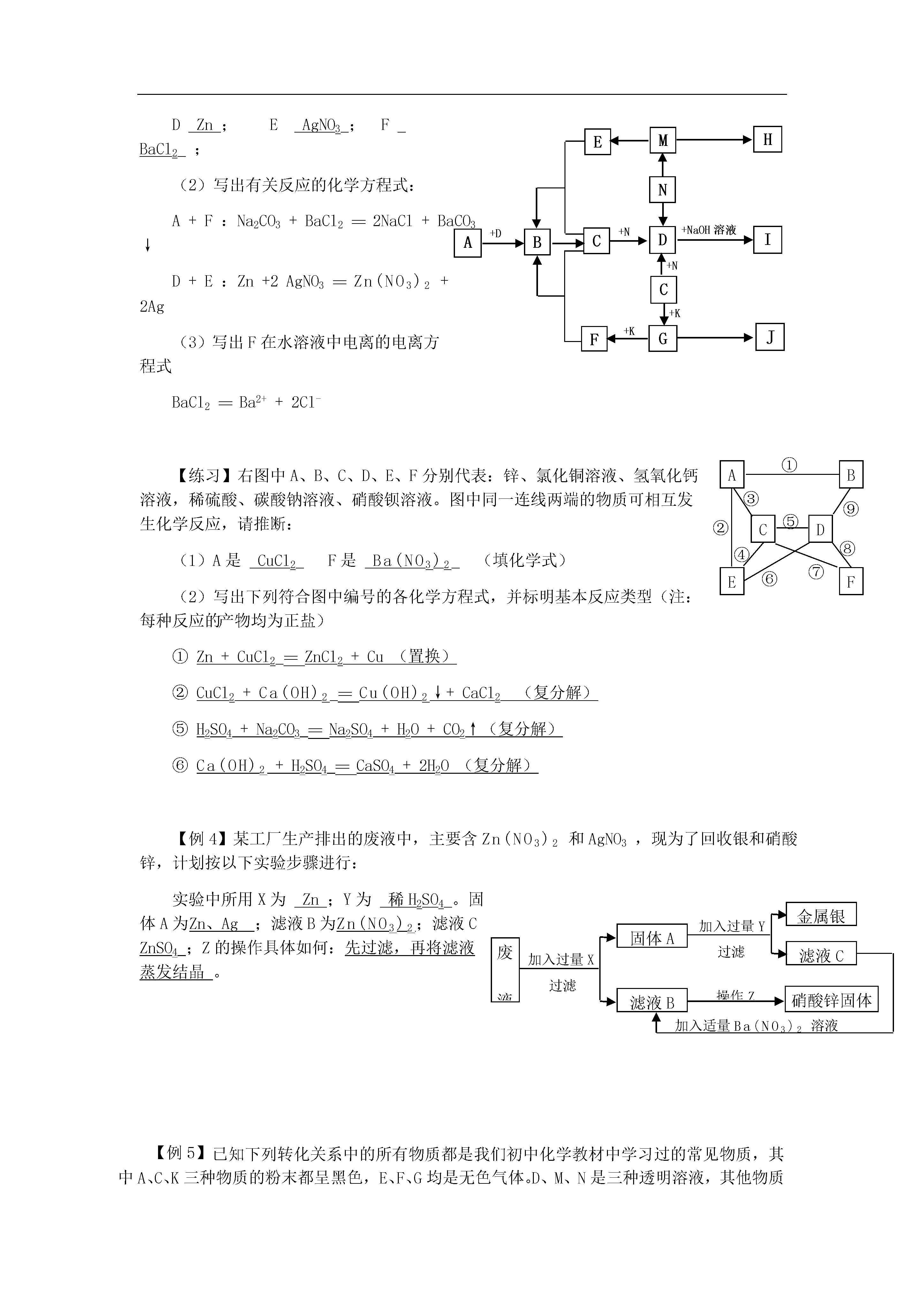
第十九课时无机物之间基本反应规律【练习1】用化学方程式表示下列变化:⑴以铜为例表示:“金属碱性氧化物碱盐”的衍生过程。⑵以碳为例表示:“非金属酸性氧化物酸盐”的衍生过程。【练习2】用化学方程式表示各类物质相互反应:⑴酸性氧化物+碱盐+水⑵碱性氧化物+酸盐+水⑶碱+酸盐+水⑷碱+盐新碱+新盐⑸酸+盐新酸+新盐⑹盐+盐新盐+新盐⑺金属+酸盐+氢气⑻金属+盐金属+盐【练习3】各写一个化学方程式,表示下列种类物质的制取方法:⑴用活动金属制取不活动金属⑵用碱性氧化物制取盐⑶用可溶性碱制不溶性碱⑷用可溶性盐制可溶性碱⑸用不溶性碱制可溶性盐⑹用可溶性盐制不溶性盐【练习4】某工厂排放的澄清废液中,加入BaCl2溶液产生白色沉淀,再加入足量的稀硝酸,沉淀部分溶解并放出使澄清石灰水变浑浊的气体,下列结论正确的是()A.废液中一定有Ag+B.废液中一定有CO32-C.废液中一定有SO42-D.废液中一定有H2SO4【例1】现有盐酸、氢氧化钙、碳酸钠三种溶液,请你从中选择两种溶液,用化学方法进行鉴别。要求:①选择试剂时,同类物质在鉴别中只能使用一次;②每一次鉴别一步完成;③有微溶物生成的,不按沉淀处理。请回答:(1)你认为鉴别方法最多的两种溶液是(2)鉴别上述两种溶液,你所选择的试剂分别是(1)可能的两种溶液(2)各种鉴别方法中所加试剂(写具体物质也可)HCl、Na2CO3①指示剂②活泼金属③CuO或Fe2O3④酸(HCl、H2SO4等)⑤难溶碱或Ca(OH)2、Ba(OH)2⑥碳酸盐HCl、Ca(OH)2①指示剂②活泼金属③CO2或CuO、Fe2O3④难溶碱⑤碳酸盐Na2CO3、Ca(OH)2①CO2②酸(HCl、H2SO4等)③Ca(OH)2、Ba(OH)2等④可溶性碳酸盐或可溶性钙盐、钡盐等【例2】有一包白色固体,可能含有碳酸钠、硫酸铜、氯化钙、硫酸钠、氯化钠等物质中的一种或几种,现取部分该固体溶于水,可得到澄清的无色溶液,向其中滴入氯化钡溶液,产生白色沉淀,再加入足量的稀硝酸,沉淀部分溶解。请回答:(1)该固体中一定含有_Na2CO3、Na2SO4,一定不含有CuSO4、CaCl2;可能含有NaCl。(2)写出反应的化学方程式Na2CO3+BaCl2==2NaCl+BaCO3↓Na2SO4+BaCl2==2NaCl+BaSO4↓BaCO3+2HNO3==Ba(NO3)2+H2O+CO2↑(3)请你设计一个实验,证明白色固体中可能含有的物质是否存在。①取少量固体样品溶于水中;②向溶液中加入足量的Ba(NO3)2溶液,产生白色沉淀;③过滤得到滤液;④向液中加入AgNO3溶液,若有白色沉淀产生,说明原白色固体中含有NaCl;若无沉淀产生,说明原混合物中不含NaCl。【练习】有一包粉末,可能由NaCl、Na2SO4、Na2CO3、FeCl3、MgCl2中的一种或几种组成。现做如下实验:①取少量粉末,加水溶解得到无色透明溶液;②取①所得溶液少许加入氢氧化钠溶液,看不到明显现象;③另取少量粉末滴加稀盐酸,也看不到明显现象。试回答:⑴由实验①可知,原粉末中一定没有______;由实验②可说明原粉末中没有_______;实验③证明原粉末中没有______。⑵根据上述实验,可得出原粉末中可能有的物质是_________。为了确定原粉末是纯净物还是混合物,继续做如下实验:④取①所得溶液少许,滴加溶液A,有白色沉淀生成;⑤继续滴加溶液A,直至再无白色沉淀生成,静置。取上层清液少许,滴加溶液B,无明显现象。⑶由实验④可知原粉末中一定有_____;由实验⑤可知原粉末中一定没有______。试写出④、⑤两实验所用溶液A、B中溶质的化学式:A______,B_____;实验④中反应的化学方程式为_____。[答案]⑴FeCl3;MgCl2;Na2CO3⑵NaCl、Na2SO4⑶Na2SO4;NaCl;Ba(NO3)2;AgNO3;Na2SO4+Ba(NO3)2==BaSO4↓+2NaNO3。【例2】只有氯化钡溶液和简单的仪器装置,鉴别稀硫酸和碳酸钠溶液(任意编号为甲、乙溶液)操作如下:(1)分别取少量甲、乙溶液于两支试管中,各滴加氯化钡溶液,两支试管中都产生白色沉淀。下面还要进行怎样的操作,才能把它们鉴别出来。请将鉴别的步骤、现象及最终结论,填写在相应的横线上:(2)分别过滤,得到两种白色固体和两种无色溶液。(3)将所得固体分别置于两支试管中,若取溶液甲滴入两支试管,观察到一支试管中产生无色气体,另一支试管中无明显现象。证明甲是稀硫酸、乙是碳酸钠溶液。若取溶液甲滴入两支试管中,均无明显现象。证明甲是碳酸钠溶液、乙是稀硫酸。【例3】有A、B、

是向****23
 实名认证
实名认证
 内容提供者
内容提供者
最近下载


















