学案-江苏-2016_江苏省铜山区清华中学九年级化学全册《第7章 应用广泛的酸、碱、盐》导学案(无答案)(新版)沪教版.doc
 立即下载
立即下载

如果您无法下载资料,请参考说明:
1、部分资料下载需要金币,请确保您的账户上有足够的金币
2、已购买过的文档,再次下载不重复扣费
3、资料包下载后请先用软件解压,在使用对应软件打开
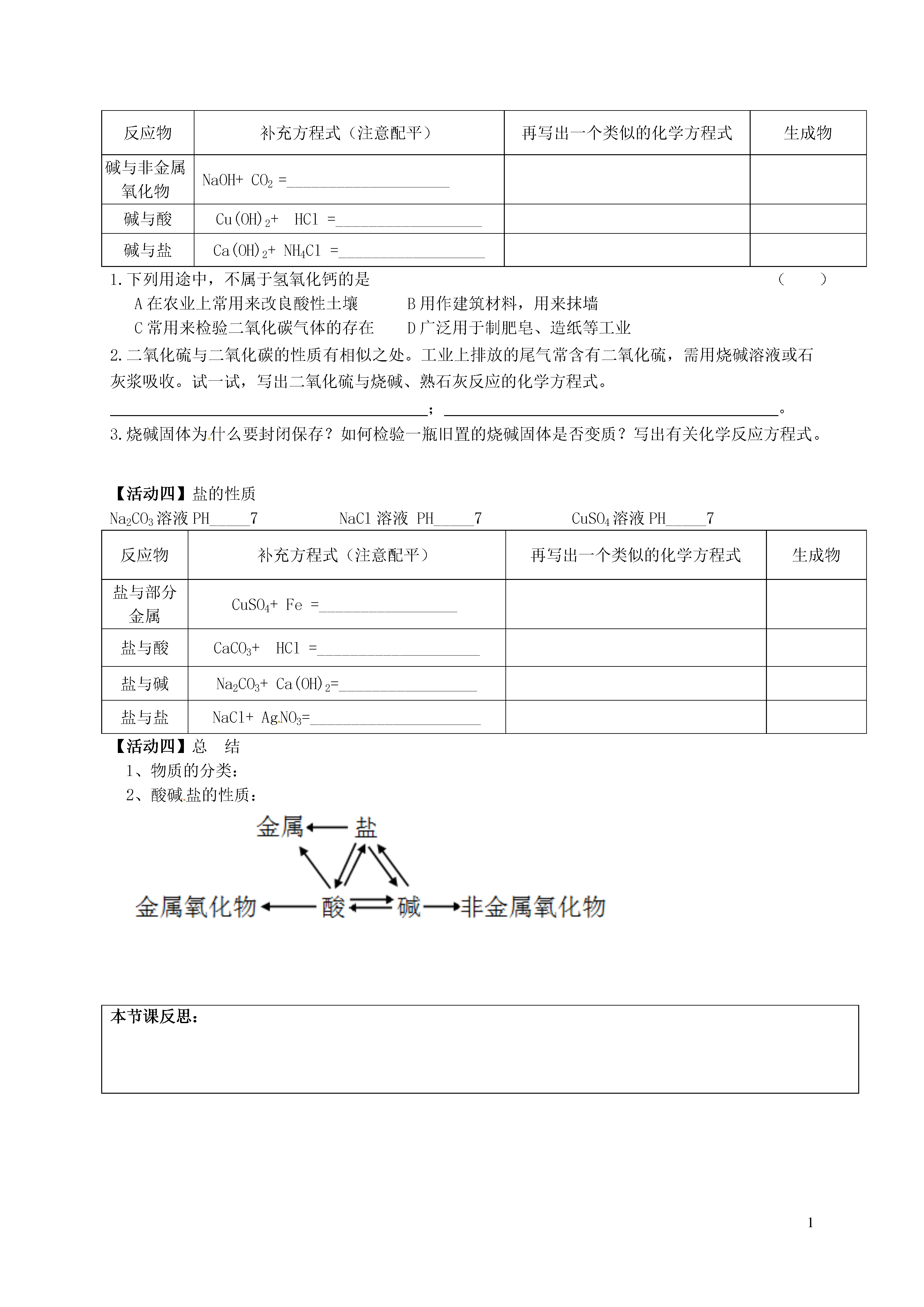
1第7章应用广泛的酸、碱、盐【学习目标】1.掌握物质的分类方法,对常见物质进行分类。2.掌握酸碱盐的化学性质及应用。3.掌握典型化学反应方程式的书写及应用。【学习重点】酸碱盐的化学性质及应用【学习难点】典型化学反应方程式的书写及应用导学过程【活动一】找出酸碱盐在下列各类物质中,找出酸、碱、盐,分别写在相应的横线上SO2NaOHCuHClNaClCaCO3ZnNH4NO3Fe2O3Na2CO3FeHNO3CuSO4AgNO3CuOCa(OH)2H2SO4CO2酸:__________________________________________________________________碱:_______________________________________________________________盐:__________________________________________________________________【活动二】酸的通性1.酸溶液PH_____7,能使紫色石蕊试液变_______,无色酚酞试液遇到酸___________。反应物补充方程式(注意配平)再写一个类似的化学方程式生成物酸与部分活泼金属HCl+Fe=_____________________酸与金属氧化物HCl+Fe2O3=___________________酸与碱H2SO4+Ba(OH)2=_________________酸与盐HCl+AgNO3=____________________2.下列关于盐酸的用途中,不能用稀硫酸代替的是()A、制氢气B、除铁锈C、制二氧化碳D、溶解氧化铜3.归纳是学习的重要方法,小红在复习盐酸的性质时,归纳出盐酸的五条化学性质(连线表示相互反应).(1)为了验证性质①,小红将紫色石蕊试液滴加到盐酸溶液中,溶液变。(2)图中A所表示的物质类别是;(3)盐酸的性质③决定了盐酸可用于清除铁锈(主要成分Fe2O3),该反应的化学方程式是;(4)为了验证性质⑤,可选用的物质是(填一种即可);(5)镁和锌可以用来验证盐酸的性质②,小红要探究镁和锌与盐酸反应的快慢,需要控制不变(相同)的量是(填序号);A.两种金属的形状B.盐酸的质量分数C.反应容器的大小D.温度.【活动三】碱的通性1.总结碱的化学性质:碱溶液PH_____7,使紫色石蕊试液变_____,无色酚酞试液遇到碱___________。反应物补充方程式(注意配平)再写出一个类似的化学方程式生成物碱与非金属氧化物NaOH+CO2=____________________碱与酸Cu(OH)2+HCl=__________________碱与盐Ca(OH)2+NH4Cl=__________________1.下列用途中,不属于氢氧化钙的是()A在农业上常用来改良酸性土壤B用作建筑材料,用来抹墙C常用来检验二氧化碳气体的存在D广泛用于制肥皂、造纸等工业2.二氧化硫与二氧化碳的性质有相似之处。工业上排放的尾气常含有二氧化硫,需用烧碱溶液或石灰浆吸收。试一试,写出二氧化硫与烧碱、熟石灰反应的化学方程式。;。3.烧碱固体为什么要封闭保存?如何检验一瓶旧置的烧碱固体是否变质?写出有关化学反应方程式。【活动四】盐的性质Na2CO3溶液PH_____7NaCl溶液PH_____7CuSO4溶液PH_____7反应物补充方程式(注意配平)再写出一个类似的化学方程式生成物盐与部分金属CuSO4+Fe=_________________盐与酸CaCO3+HCl=____________________盐与碱Na2CO3+Ca(OH)2=_________________盐与盐NaCl+AgNO3=_____________________【活动四】总结1、物质的分类:2、酸碱盐的性质:本节课反思:

白凡****12
 实名认证
实名认证
 内容提供者
内容提供者
最近下载


















