


如果您无法下载资料,请参考说明:
1、部分资料下载需要金币,请确保您的账户上有足够的金币
2、已购买过的文档,再次下载不重复扣费
3、资料包下载后请先用软件解压,在使用对应软件打开
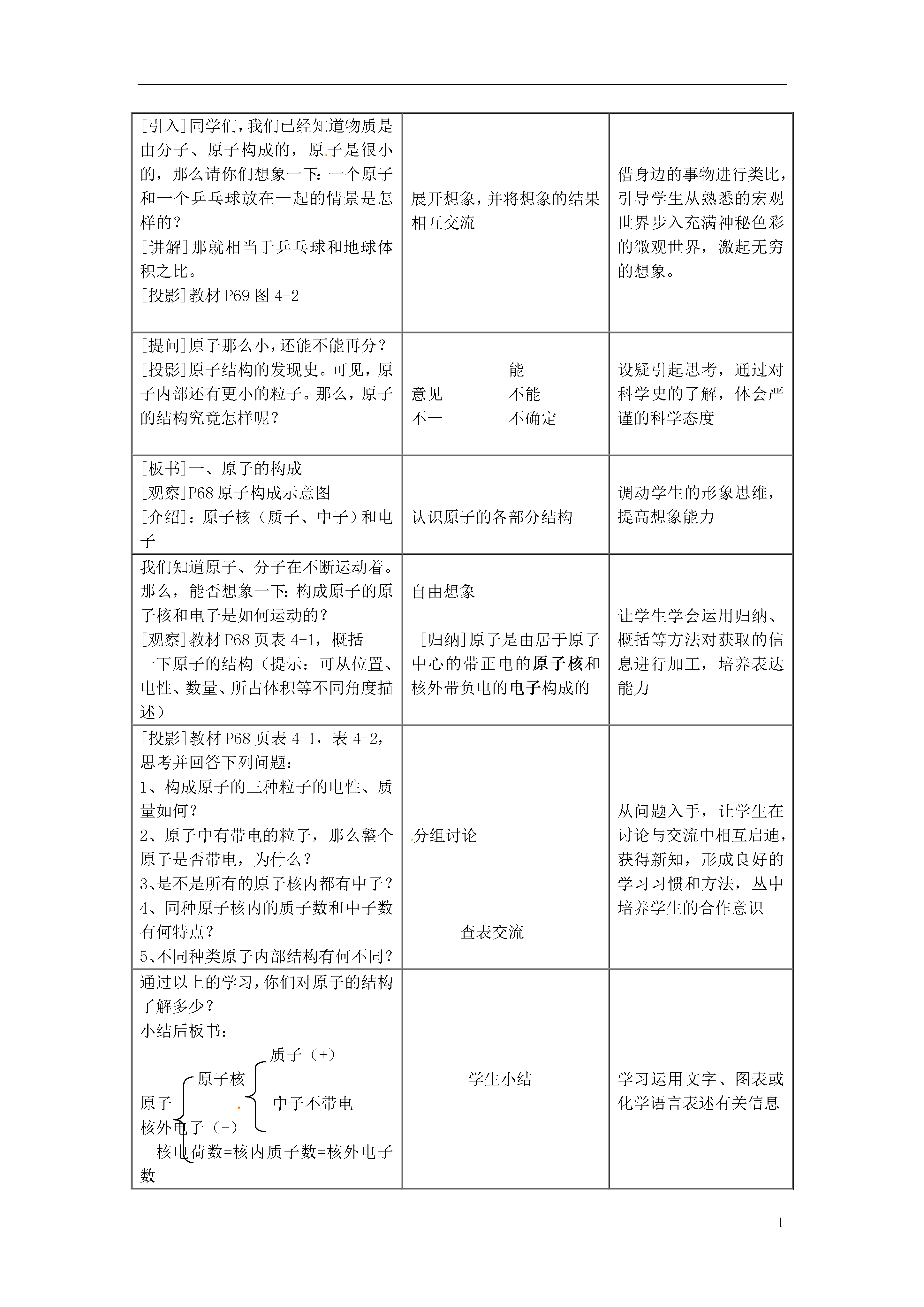
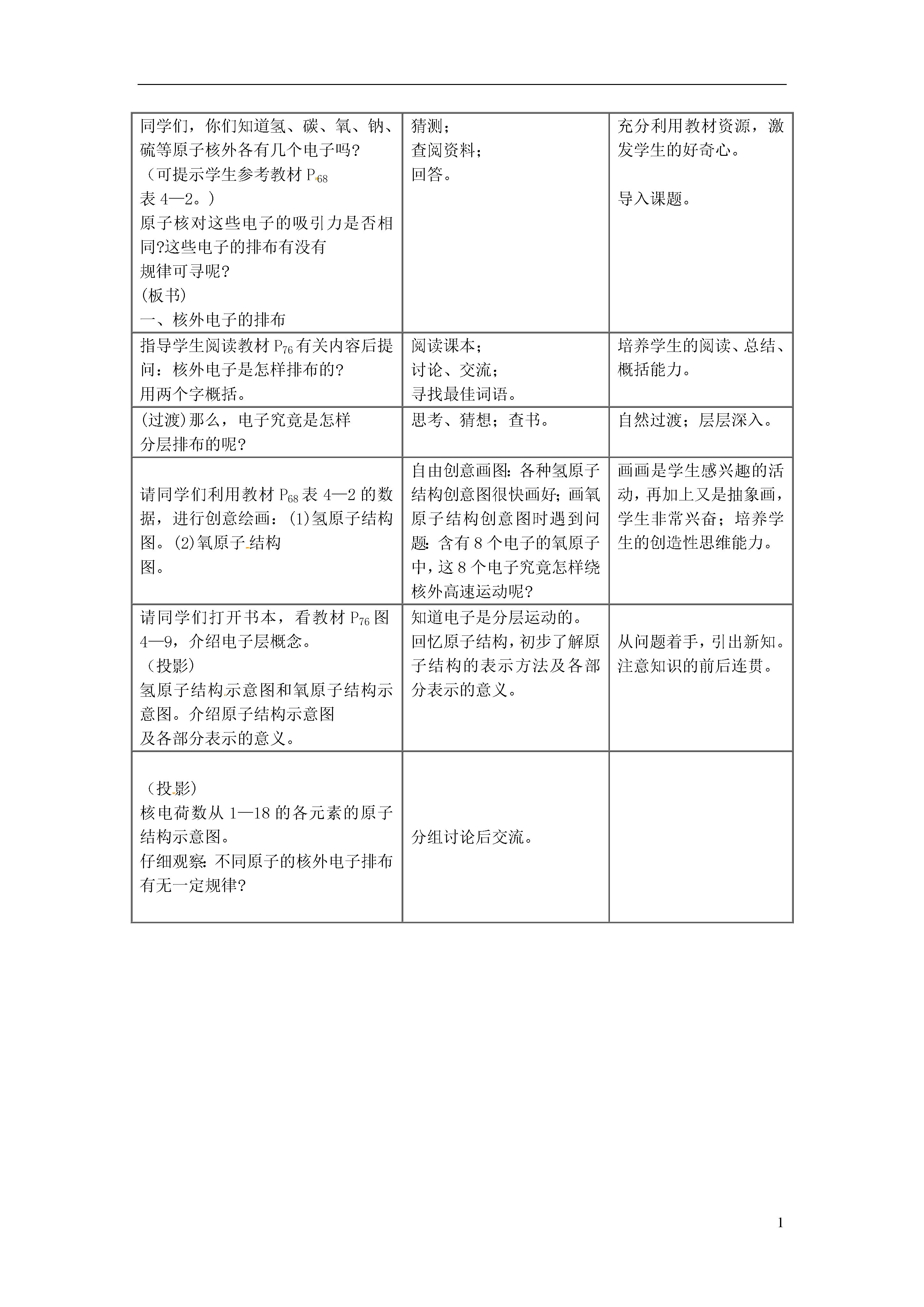
1原子的结构设计要素设计内容教学内容分析教学目标知识与技能1、了解原子是由质子、中子和电子构成的2、初步了解原子核外的电子是分层排布的;3、了解原子结构的表示方法;4、了解原子结构与元素化学性质的关系;5了解离子的形成过程,认识离子是构成物质的一种粒子。6、初步了解相对原子质量的概念,并会查相对原子质量表过程与方法1、充分利用教材提供的图表等资料,借助模型,多媒体等教学手段,化抽象为直观,初步学会运用类比、想象、归纳、概括等方法获取的信息2、通过讨论与交流,启发学生的思维,逐步养成良好的学习习惯和学习方法情感态度价值观1、激发学生对微观世界的探究欲和学习化学的兴趣2、对学生进行世界的物质性、物质的可分性的辨证唯物主义观点的教育学情分析教学分析教学重点原子的内部结构、相对原子质量、离子的形成教学难点难点对“原子不显电性”的理解、核外电子排布的概念解决办法利用原子结构示意图引导学生。教学资源教材、原子结构示意图板书设计课题1原子的构成一、原子的构成1.原子的构成质子(+)原子核原子中子不带电核外电子(-)2.核电荷数=核内质子数=核外电子数3.不同种类的原子,其核内的质子数不同,核外的电子数也不同。二、核外电子的排布1.排布规律:分层。2.原子结构示意图:3.决定元素的化学性质:最外层电子数。4.离子的形成(1)定义:带电荷的原子。(2)形成过程:三、相对原子质量1.概念以一种碳原子质量的1/12为标准,其他原子的质量跟它相比较所得到的比,作为这种原子的相对原子质量(符号为Ar)。2.计算①计算一种原子的相对原子质量。②计算一种原子的真实质量。③计算作为标准的碳原子的质量。教学过程教师活动学生活动设计意图[引入]同学们,我们已经知道物质是由分子、原子构成的,原子是很小的,那么请你们想象一下:一个原子和一个乒乓球放在一起的情景是怎样的?[讲解]那就相当于乒乓球和地球体积之比。[投影]教材P69图4-2展开想象,并将想象的结果相互交流借身边的事物进行类比,引导学生从熟悉的宏观世界步入充满神秘色彩的微观世界,激起无穷的想象。[提问]原子那么小,还能不能再分?[投影]原子结构的发现史。可见,原子内部还有更小的粒子。那么,原子的结构究竟怎样呢?能意见不能不一不确定设疑引起思考,通过对科学史的了解,体会严谨的科学态度[板书]一、原子的构成[观察]P68原子构成示意图[介绍]:原子核(质子、中子)和电子认识原子的各部分结构调动学生的形象思维,提高想象能力我们知道原子、分子在不断运动着。那么,能否想象一下:构成原子的原子核和电子是如何运动的?[观察]教材P68页表4-1,概括一下原子的结构(提示:可从位置、电性、数量、所占体积等不同角度描述)自由想象[归纳]原子是由居于原子中心的带正电的原子核和核外带负电的电子构成的让学生学会运用归纳、概括等方法对获取的信息进行加工,培养表达能力[投影]教材P68页表4-1,表4-2,思考并回答下列问题:1、构成原子的三种粒子的电性、质量如何?2、原子中有带电的粒子,那么整个原子是否带电,为什么?3、是不是所有的原子核内都有中子?4、同种原子核内的质子数和中子数有何特点?5、不同种类原子内部结构有何不同?分组讨论查表交流从问题入手,让学生在讨论与交流中相互启迪,获得新知,形成良好的学习习惯和方法,丛中培养学生的合作意识通过以上的学习,你们对原子的结构了解多少?小结后板书:质子(+)原子核原子中子不带电核外电子(-)核电荷数=核内质子数=核外电子数学生小结学习运用文字、图表或化学语言表述有关信息同学们,你们知道氢、碳、氧、钠、硫等原子核外各有几个电子吗?(可提示学生参考教材P68表4—2。)原子核对这些电子的吸引力是否相同?这些电子的排布有没有规律可寻呢?(板书)一、核外电子的排布猜测;查阅资料;回答。充分利用教材资源,激发学生的好奇心。导入课题。指导学生阅读教材P76有关内容后提问:核外电子是怎样排布的?用两个字概括。阅读课本;讨论、交流;寻找最佳词语。培养学生的阅读、总结、概括能力。(过渡)那么,电子究竟是怎样分层排布的呢?思考、猜想;查书。自然过渡;层层深入。请同学们利用教材P68表4—2的数据,进行创意绘画:(1)氢原子结构图。(2)氧原子结构图。自由创意画图:各种氢原子结构创意图很快画好;画氧原子结构创意图时遇到问题:含有8个电子的氧原子中,这8个电子究竟怎样绕核外高速运动呢?画画是学生感兴趣的活动,再加

子璇****君淑
 实名认证
实名认证
 内容提供者
内容提供者
最近下载
一种胃肠道超声检查助显剂及其制备方法.pdf
201651206021+莫武林+浅析在互联网时代下酒店的营销策略——以湛江民大喜来登酒店为例.doc
201651206021+莫武林+浅析在互联网时代下酒店的营销策略——以湛江民大喜来登酒店为例.doc
用于空间热电转换的耐高温涡轮发电机转子及其装配方法.pdf
用于空间热电转换的耐高温涡轮发电机转子及其装配方法.pdf
用于空间热电转换的耐高温涡轮发电机转子及其装配方法.pdf
用于空间热电转换的耐高温涡轮发电机转子及其装配方法.pdf
用于空间热电转换的耐高温涡轮发电机转子及其装配方法.pdf
用于空间热电转换的耐高温涡轮发电机转子及其装配方法.pdf
论《离骚》诠释史中的“香草”意蕴.docx


















