

如果您无法下载资料,请参考说明:
1、部分资料下载需要金币,请确保您的账户上有足够的金币
2、已购买过的文档,再次下载不重复扣费
3、资料包下载后请先用软件解压,在使用对应软件打开
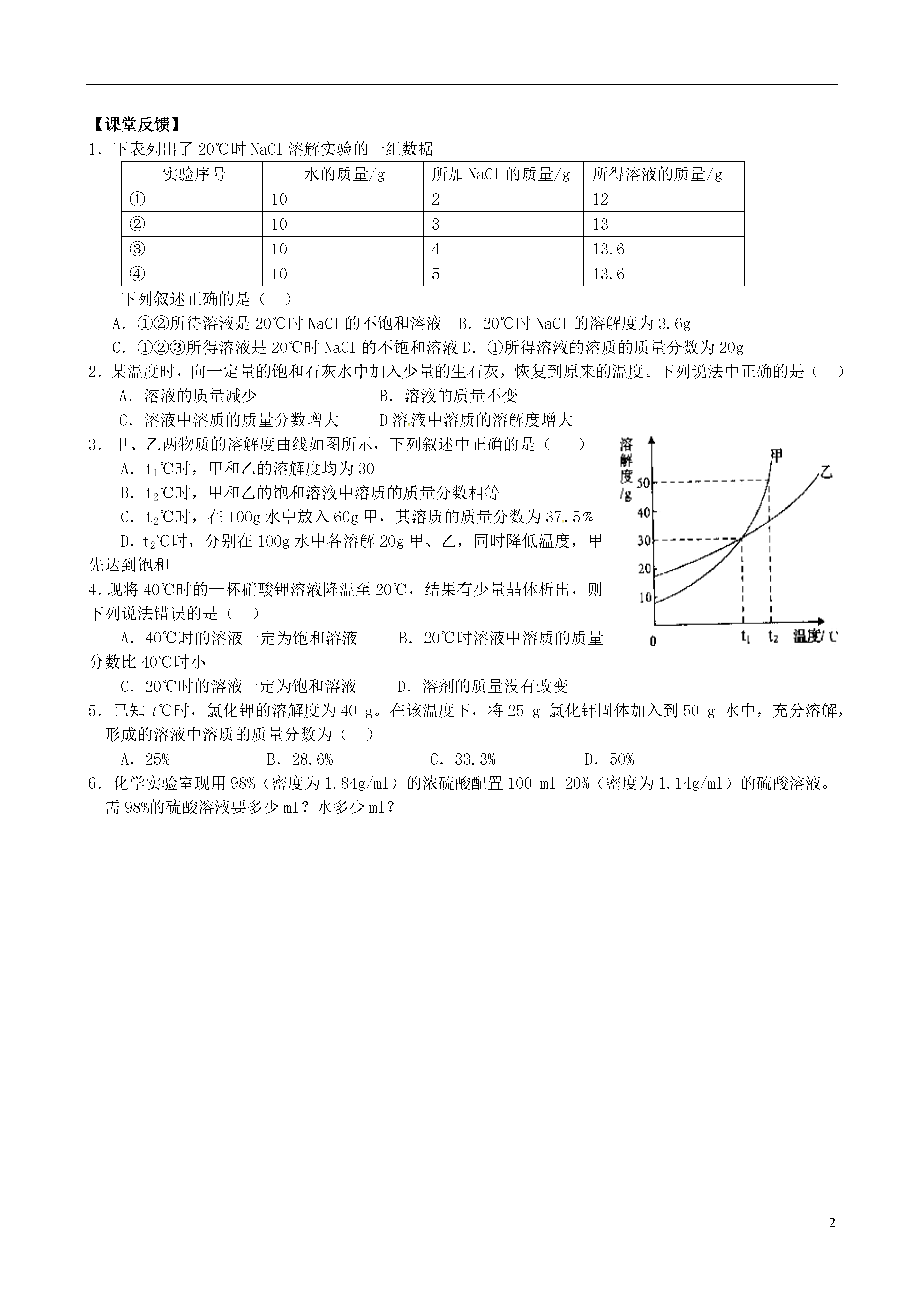
2江苏省如皋市石庄初中九年级化学下册《溶质的质量分数(第1课时)》教案新人教版1、感受溶液的浓与稀2、感知溶质的质量分数,并掌握溶质质量分数的计算方法3、感知溶质的质量分数、溶质质量、溶液质量、溶剂质量之间的关系4、初步学会有关溶液稀释的计算【活动过程】活动一:感受溶液的浓与稀甲组:取装有10mL水的烧杯乙组:取装有10mL水的烧杯操作步骤溶液的浓与稀判断依据加入0.5g硫酸铜,搅拌,得溶液①再加2g硫酸铜,搅拌,得溶液②操作步骤溶液的浓与稀判断依据加入0.5g氯化钠,搅拌,得溶液③再加2g氯化钠,搅拌,得溶液④[结论]甲乙两组交流后作出自己的结论:1、对于有色溶液来说,可根据溶液颜色的________来比较溶液的浓稀;2、对于无色溶液来说,可根据溶液中溶质质量与溶液质量的___________来比较溶液的浓稀。活动二:感知溶质的质量分数,并掌握溶质质量分数的计算方法。在生活中我们常常需要准确知道一定量溶液中究竟含有多少溶质。如在施用农药时,就应该准确的知道一定量的药液里所含农药的量。如果农药过浓,会毒害农作物;如果药液过稀,又不能有效杀虫灭菌。因此我们需要准确知道溶液的组成。溶液组成的表示方法有多种,化学中常用溶质的质量分数(即溶质质量与溶液质量的比值)来表示溶液的组成。1、用溶质的质量分数表示下列溶液的组成。已知20℃SNaCl=36.0g,SKNO3=31.6g;60℃SNaCl=37.3g,SKNO3=110g配得4种溶液溶液a60℃时,20gKNO3完全溶于80克水中溶液b20℃时,15.8gNaCl完全溶于50克水中溶液c60℃时,20gNaCl加入到50克水中,充分溶解溶液d20℃时,20gKNO3加入到50克水中,充分溶解(1)、根据你的计算结果判断上述4种溶液溶质质量分数由大到小的顺序是:﹥﹥﹥.2、20℃SNaCl=36.0g,则该温度下,氯化钠溶液中溶质的质量分数不可能的是()A.30%B.26.2%C.25%D.20%活动三、感知溶质的质量分数、溶质质量、溶液质量、溶剂质量之间的关系溶液编号溶质质量(克)溶剂质量(克)溶液质量(克)溶质质量分数11910021502503321846733%54824%总结:由上表可知,只要知道“溶液的质量”“溶质的质量”“溶剂的质量”以及“溶质的质量分数”四个量中的任意_____个量,我们就可以求出另外两个。活动四体验溶液稀释的计算。现有20%的NaCl的溶液,若要变为5%的溶液。可以通过哪些途径实现?⑴分析:浓溶液+水→稀溶液,请把溶液中各个量的变化情况填写再下表中。原浓溶液加xg水后的稀溶液变化情况(填变多、变少、或不变)溶质质量溶剂质量溶液质量溶质的质量分数⑵找出浓溶液+水→稀溶液过程中的等量关系:A浓%H2OA稀%m浓溶液m水m稀溶液m浓溶液×A浓%m稀溶液×A稀%判断:V浓溶液+V水=V稀溶液?为什么?2.[例题1]化学实验室现有98%的浓硫酸,但在实验中常需要用较稀的硫酸溶液。要把50g质量分数为98%的浓硫酸稀释为质量分数为20%的硫酸溶液,需要多少克水?98%H2O20%____________________________________________【课堂反馈】1.下表列出了20℃时NaCl溶解实验的一组数据实验序号水的质量/g所加NaCl的质量/g所得溶液的质量/g①10212②10313③10413.6④10513.6下列叙述正确的是()A.①②所待溶液是20℃时NaCl的不饱和溶液B.20℃时NaCl的溶解度为3.6gC.①②③所得溶液是20℃时NaCl的不饱和溶液D.①所得溶液的溶质的质量分数为20g2.某温度时,向一定量的饱和石灰水中加入少量的生石灰,恢复到原来的温度。下列说法中正确的是()A.溶液的质量减少B.溶液的质量不变C.溶液中溶质的质量分数增大D溶液中溶质的溶解度增大3.甲、乙两物质的溶解度曲线如图所示,下列叙述中正确的是()A.t1℃时,甲和乙的溶解度均为30B.t2℃时,甲和乙的饱和溶液中溶质的质量分数相等C.t2℃时,在100g水中放入60g甲,其溶质的质量分数为37.5﹪D.t2℃时,分别在100g水中各溶解20g甲、乙,同时降低温度,甲先达到饱和4.现将40℃时的一杯硝酸钾溶液降温至20℃,结果有少量晶体析出,则下列说法错误的是()A.40℃时的溶液一定为饱和溶液B.20℃时溶液中溶质的质量分数比40℃时小C.20℃时的溶液一定为饱和溶液D.溶剂的质量没有改变5.已知t℃时,氯化钾的溶解度为40g。在该温度下,将25g氯化钾固体加入到50g水中,充分溶解

明轩****la
 实名认证
实名认证
 内容提供者
内容提供者
最近下载
最新上传
2024年安徽省六安市金寨县二级建造师考试水利水电工程管理与实务考前冲刺试卷及答案.docx
2024年安徽省六安市金寨县二级建造师考试水利水电工程管理与实务考前冲刺试卷完整版.docx
2025年高考河南省化学真题试卷(网络收集版).pdf
2025年高考江苏卷物理真题(网络收集版).pdf
2025年高考山东地理真题(网络收集版).pdf
2025年高考山东卷物理真题(网络收集版).pdf
2025高考广西卷物理真题及答案(网络收集版).pdf
2025年高考安徽卷化学真题及答案(网络收集版).pdf
2025年黑吉辽蒙化学高考真题试卷及答案-黑龙江卷(网络收集版).pdf
2025年高考云南省物理真题及答案(网络收集版).pdf


















