素材-全国-2018_(湖南专用)2019年中考化学复习 专题三 水与常见的溶液(讲解部分)素材(pdf).pdf
 立即下载
立即下载


如果您无法下载资料,请参考说明:
1、部分资料下载需要金币,请确保您的账户上有足够的金币
2、已购买过的文档,再次下载不重复扣费
3、资料包下载后请先用软件解压,在使用对应软件打开
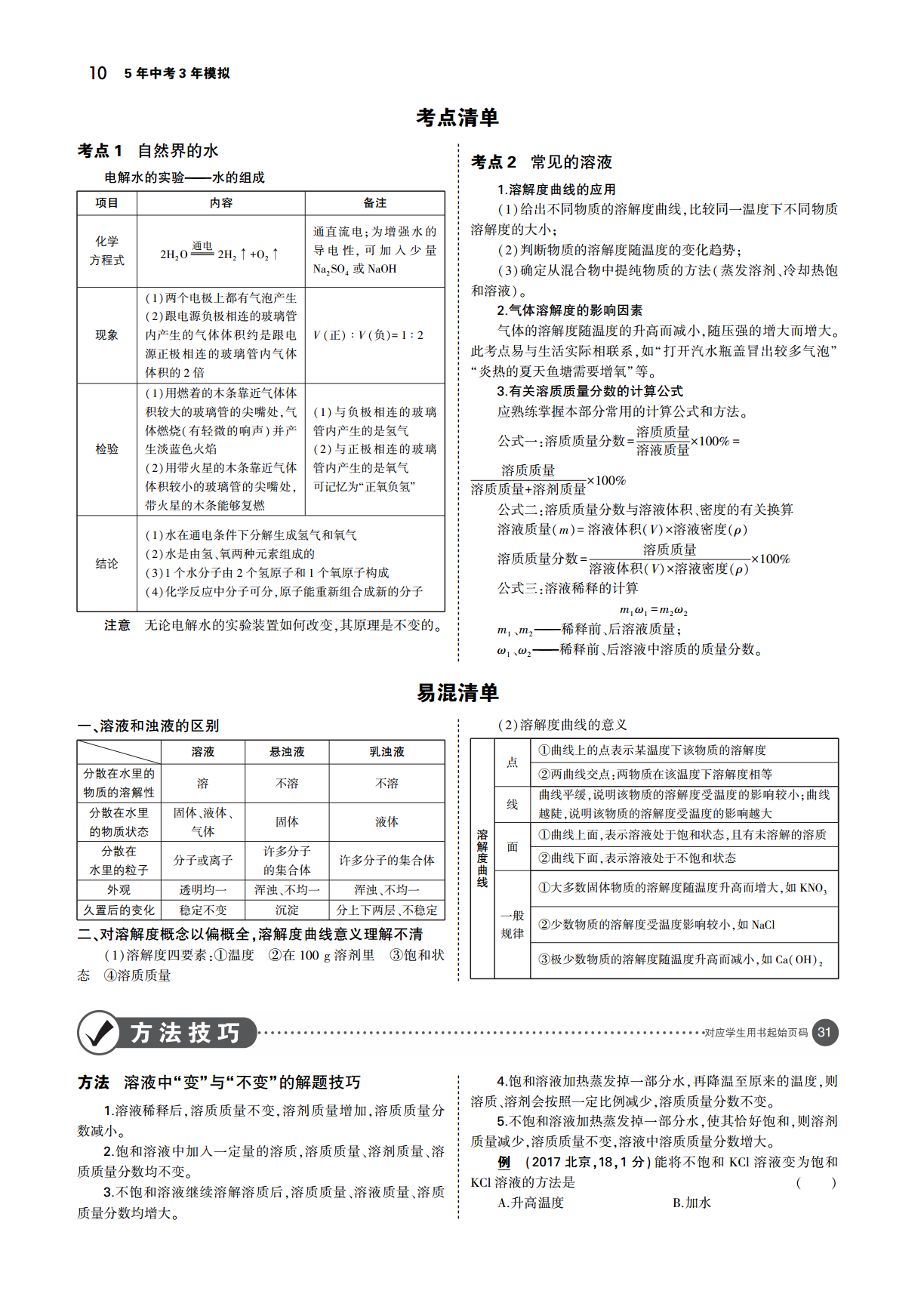
专题三水与常见的溶液9专题三水与常见的溶液29知识结构定义一种或几种物质分散到另一种物质里形成均一的稳定的混合物ì1.:,、ï溶质固体液体气体ï组成(、、)2.{溶剂液体一般为水ï(,)ï均一性各处的性质相同性质:ï3.{稳定性外界条件不变时溶液长时间放置不会分层也不会析出固体物质溶ï:,,í吸热如液ï(①NH4NO3)溶解时的热现象温度不变如ï4.{(②NaCl)ï放热如(③NaOH)ïì定义在一定温度下向一定量溶剂里加入某种溶质当溶质不能继续溶解时所得ïï:,,,ï溶液叫饱和溶液还能继续溶解的溶液叫做不饱和溶液îï分类饱和溶液与不饱和溶液í;,5.:增加溶质降温恒温蒸发ï④ï转化措施不饱和溶液、⑤、⑥饱和溶液一般情况下î:增加溶剂升温()⑦、⑧定义在一定温度下某固态物质在溶剂里达到饱和状态时所溶解的质量ïì:,100g内因溶质溶剂的性质ïïì:、ïïT一般Sï影响因素í↗,↗ï外因温度TTS变化不大如ïï:(){↗,(NaCl)ïîTS如熟石灰固体溶解度í↗,↘()ì1.读出某温度下的溶解度读出某溶解度对应的温度ïïïì()溶ïïï比较某温度下不同物质的溶解度ï溶解度ï解ïïí交点的意义表示该温度下两物质的溶解度相同íï曲线ï:⑨度S受T影响大用降温结晶的方法如中含少量ï3ïï物质提纯:(KNONaCl)Sïîî{S受T影响小用蒸发溶剂的方法如中含少量()ï:(NaClKNO3)ïTTSî气体溶解度影响因素(↗,↘)2.:{ppS(↗,↗)溶溶质质量定义溶质质量分数质ïì1.:=溶液质量×100%质ïì溶质质量分数íï量ïï实验步骤计算称量量取溶解装瓶ï:→、→→分îï溶液的配制仪器托盘天平烧杯玻璃棒药匙胶头滴管量筒计算í{:、、、、、数2.ï影响实验结果的原因ï溶液的稀释mωmωï(11=22)î溶质质量分数应用到化学方程式的计算与不纯物质的计算类似()105年中考3年模拟考点清单考点1自然界的水考点2常见的溶液电解水的实验———水的组成1溶解度曲线的应用项目内容备注.给出不同物质的溶解度曲线比较同一温度下不同物质(1),通直流电为增强水的溶解度的大小化学;;通电导电性可加入少量判断物质的溶解度随温度的变化趋势,方程式2H2O2H2↑+O2↑(2);或确定从混合物中提纯物质的方法蒸发溶剂冷却热饱Na2SO4NaOH(3)(、和溶液两个电极上都有气泡产生)。(1)2气体溶解度的影响因素跟电源负极相连的玻璃管.(2)气体的溶解度随温度的升高而减小随压强的增大而增大现象内产生的气体体积约是跟电V正V负,。()∶()=1∶2源正极相连的玻璃管内气体此考点易与生活实际相联系如打开汽水瓶盖冒出较多气泡,“”体积的倍炎热的夏天鱼塘需要增氧等2“”。用燃着的木条靠近气体体3有关溶质质量分数的计算公式(1).积较大的玻璃管的尖嘴处气与负极相连的玻璃应熟练掌握本部分常用的计算公式和方法,(1)。体燃烧有轻微的响声并产管内产生的是氢气溶质质量()公式一溶质质量分数检验生淡蓝色火焰与正极相连的玻璃:=溶液质量×100%=(2)用带火星的木条靠近气体管内产生的是氧气(2)溶质质量体积较小的玻璃管的尖嘴处可记忆为正氧负氢溶质质量溶剂质量×100%,“”+带火星的木条能够复燃公式二溶质质量分数与溶液体积密度的有关换算:、溶液质量溶液体积溶液密度mVρ水在通电条件下分解生成氢气和氧气()=()×()(1)溶质质量水是由氢氧两种元素组成的溶质质量分数结论(2)、=溶液体积V溶液密度ρ×100%个水分子由个氢原子和个氧原子构成(3)121()×()化学反应中分子可分原子能重新组合成新的分子公式三溶液稀释的计算(4),:mωmω11=22注意无论电解水的实验装置如何改变其原理是不变的mm稀释前后溶液质量,。1、2———、;ωω稀释前后溶液中溶质的质量分数1、2———、。易混清单一、溶液和浊液的区别溶解度曲线的意义(2)曲线上的点表示某温度下该物质的溶解度溶液悬浊液乳浊液点①分散在水里的两曲线交点两物质在该温度下溶解度相等溶不溶不溶②:物质的溶解性曲线平缓说明该物质的溶解度受温度的影响较小曲线线,;分散在水里固体液体越陡说明该物质的溶解度受温度的影响越大、、固体液体,的物质状态气体溶曲线上面表示溶液处于饱和状态且

灵波****ng
 实名认证
实名认证
 内容提供者
内容提供者
最近下载
最新上传
2024年安徽省六安市金寨县二级建造师考试水利水电工程管理与实务考前冲刺试卷及答案.docx
2024年安徽省六安市金寨县二级建造师考试水利水电工程管理与实务考前冲刺试卷完整版.docx
2025年高考河南省化学真题试卷(网络收集版).pdf
2025年高考江苏卷物理真题(网络收集版).pdf
2025年高考山东地理真题(网络收集版).pdf
2025年高考山东卷物理真题(网络收集版).pdf
2025高考广西卷物理真题及答案(网络收集版).pdf
2025年高考安徽卷化学真题及答案(网络收集版).pdf
2025年黑吉辽蒙化学高考真题试卷及答案-黑龙江卷(网络收集版).pdf
2025年高考云南省物理真题及答案(网络收集版).pdf


















