



如果您无法下载资料,请参考说明:
1、部分资料下载需要金币,请确保您的账户上有足够的金币
2、已购买过的文档,再次下载不重复扣费
3、资料包下载后请先用软件解压,在使用对应软件打开
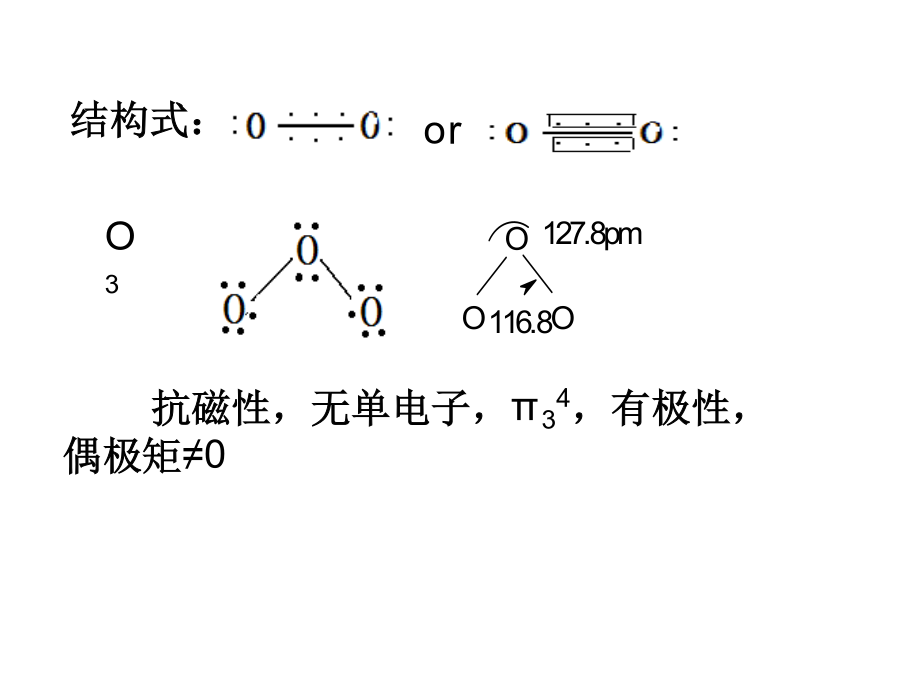
氧族元素N—N3,结构式:3.3.4氧化物As4O6两性PbO碱性As2O5酸性PbO2两性CrO(碱性)Cr2O3(两性)CrO3(酸性)3.3.5氧化物酸、碱性强弱的比较SO3(l)+H2O(l)=H2SO4(l)-70Cl2O7(g)+H2O(l)=2HClO4(l)-329 说明从Na2O到Al2O3碱性下降 1/3P2O5(s)+H2O(l)=2/3H3PO4(S)-59 SO3(l)+H2O(l)=H2SO4(l)-70Cl2O7(g)+H2O(l)=2HClO4(l)-329说明从P2O5—Cl2O7酸性升高3.3.5氧化物的制备3.3.5.1.3高价氧化物加热分解:3.3.6臭氧3.3.6.2制备3.4过氧化氢3.3.1.2制备+H23.3.2性质和用途不同点:—O—O—的断裂a,氧化剂b,还原剂c,自身氧化还原H2O2=H2O+1/2O2碱性Fe2+时反应剧烈 电极电势:φoFe3+/Fe2+=0.77v φoH2O2/H2O=1.77vφoO2/H2O2=0.683v 特殊反应 4H2O2+Cr2O72-+2H+=2CrO5↓+5H2O CrO5中Cr的氧化数为多少?O族元素:1,O的成键特征2,氧化物的制法3,O的电势图3.4硫及其化合物液态S在160oC时,S8开始断裂成长链,粘度增大,200oC时最粘,290时有S6生成444oC时沸腾,急冷后成为弹性硫H2SKa2=1.2×10-15Ka1=5.7×10-8要使H2S不从溶液中跑出,则:pH=pKa1-lgCa/Cb=7.2要使Al(OH)3不出现,则pH=?设[Al3+]=0.1mol∙L-1[OH-]=(10-35)1/3pH<2.3 一个要pH<2.3一个要pH>7.2,所以不可能,因此双水解 3.4.2.1硫化物和多硫化物3.4.2.1.2H2S体系储存:棕色瓶中2S2-+O2+2H2O=2S+4OH- 问题:Na2S溶液长期放于空气中,会产生什么变化? S2-+xS=SX+12- 如何计算Na2S和(NH4)2S的pH值。a,S2-+H2O=HS-+OH-c-xxxx=0.098828pH=13.00b,S2-+NH4+=HS-+NH311pH=pKa-lg1=9.24895 难溶硫化物的特点: 1,金属最难溶的盐一般为硫化物2,Ksp相差大。3.5含氧化合物H2SO4分子中,所有S–O键的键长和O–S–O键角不相等,而SO42-为对称性很高的Td群 水合能 HClHBrHNO3H2SO4 kJ·mol-1-74.9-85.1-33.3-878.6 所以硫酸溶解于水放热多3.5.2.3酸式盐3.5.2.3水合物和复盐M(III=Al3+Fe3+Cr3+V3+ HSO4-和SO42-之间互相转化 NaHSO4+NaOH=Na2SO4+H2O难溶盐 MSO4+H+=Mn2++HSO4-K=Ksp/Ka3.5.3硫代硫酸Na2S2O33.5.4其它酸练习次硫酸HO—S—OH+2价过硫酸 H—O—O—H3.6硫的其他化合物3.6.3卤磺酸因为SbF5为一种强的Lewis酸,由于Sb为第五主族元素,其配位数可以为6,它最外层价电子都成键,故为一种Lewis酸(电子受体),其它如:BF3、AlF3、GaF3而NH3、PH3、AsH3、Sb3H为Lewis碱H[SbF5(OSO2F)]+HOSO2F= H2SO3F++[SbF5(OSO2F)]- 3.7硒和碲3.8含氧酸的氧化还原性和酸的强弱规律2.同族,有亚周期性 如HBrO4>H5IO6>HClO4H2SeO4>H2TeO4>H2SO4HNO3>H3PO4>H3AsO4>Sb2O5>Bi2O5 实际上是Bi2O5最强,然后HNO3、H3AsO4、Sb2O5、H3PO4原因:第二,四,六周期的特殊性二,r小,无2d,内层电子少四,3d10屏蔽少于4p使原子核引力升高同一元素的不同氧化态,则氧化态越低,越易氧化HClO>HClO2>HClO3>HClO4(HClO2>HClO)HNO2>HNO3注:一些特殊,如一般S为最高+6而S2O82-为+7当然氧化力更强 目前认为:S2O82-为+6,同理还有CrO5 练习:比较HNO3H3PO4H3AsO4H2SO4H2SeO4H2TeO4的氧化性3.8.1.2影响含氧酸氧化能力的因素由于3d和4d、5d相比,1,无节点2,余尾效应小。3,能量受核电荷影响大,故d轨道和O原子成键的倾向,3d<4d<5d所以稳定性:ReO4->TeO4->MnO4-Pauli定律: 1,多元酸各级电离平衡常数有规律递减 pKan-pKan-1=5 如H3PO4、Ka1=7.52×10-3 Ka2=6.23×10-8Ka3=2.2×10-13 2,pKa1=7-5NN为非羟基氧的

王子****青蛙
 实名认证
实名认证
 内容提供者
内容提供者
最近下载


















