



如果您无法下载资料,请参考说明:
1、部分资料下载需要金币,请确保您的账户上有足够的金币
2、已购买过的文档,再次下载不重复扣费
3、资料包下载后请先用软件解压,在使用对应软件打开
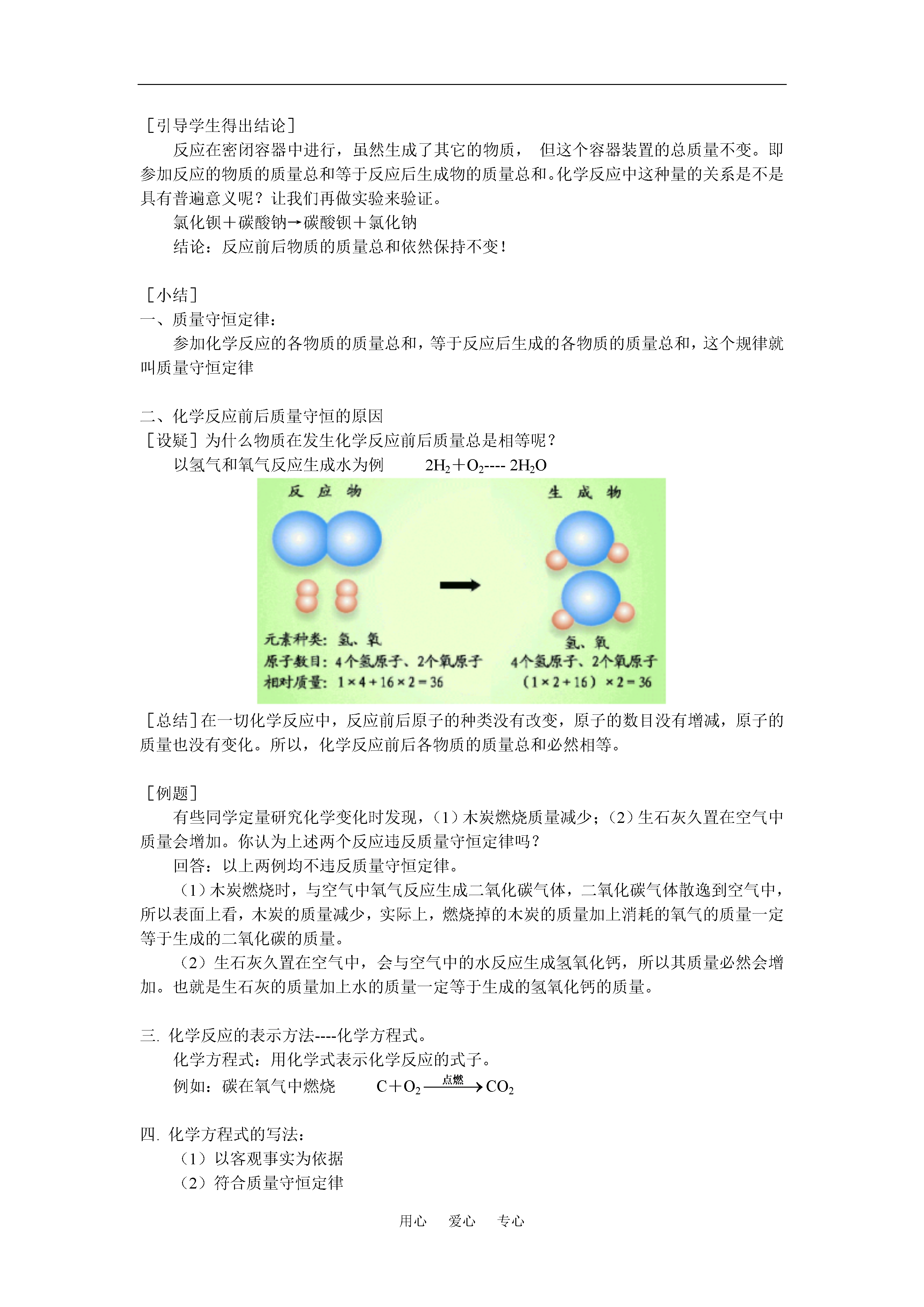
用心爱心专心九年级化学4.5化学方程式粤教版【本讲教育信息】一.教学内容:4.5化学方程式1.通过对化学反应中反应物及生成物的质量的实验测定,使学生理解质量守恒定律,培养学生的辨证唯物主义观点。2.学会化学方程式的规范书写3.学会利用化学方程式进行简单计算二.重点、难点:质量守恒定律、化学方程式及计算,既是重点,也是难点。4.5化学方程式[课前练习]用化学式表示下列化学变化的反应式:铁在氧气中燃烧;[引入新课]上述这些反应式反映出反应物在一定条件下转变为性质不同的新的生成物,从这些反应式里我们可以看到参加反应的是什么物质,生成的又是什么物质,反映了这些反应中质的变化。那么,物质的总质量在反应前后有没有变化呢?反应物和生成物之间的量是否有一定的关系呢?现在我们通过实验来研究这一关系。[实验现象](1)溶液中生成蓝色沉淀硫酸铜+氢氧化钠→氢氧化铜+硫酸钠(2)天平同反应前一样保持平衡。[实验结论]反应前后物质的总质量没有发生变化。[引导学生得出结论]反应在密闭容器中进行,虽然生成了其它的物质,但这个容器装置的总质量不变。即参加反应的物质的质量总和等于反应后生成物的质量总和。化学反应中这种量的关系是不是具有普遍意义呢?让我们再做实验来验证。氯化钡+碳酸钠→碳酸钡+氯化钠结论:反应前后物质的质量总和依然保持不变![小结]一、质量守恒定律:参加化学反应的各物质的质量总和,等于反应后生成的各物质的质量总和,这个规律就叫质量守恒定律二、化学反应前后质量守恒的原因[设疑]为什么物质在发生化学反应前后质量总是相等呢?以氢气和氧气反应生成水为例2H2+O2----2H2O[总结]在一切化学反应中,反应前后原子的种类没有改变,原子的数目没有增减,原子的质量也没有变化。所以,化学反应前后各物质的质量总和必然相等。[例题]有些同学定量研究化学变化时发现,(1)木炭燃烧质量减少;(2)生石灰久置在空气中质量会增加。你认为上述两个反应违反质量守恒定律吗?回答:以上两例均不违反质量守恒定律。(1)木炭燃烧时,与空气中氧气反应生成二氧化碳气体,二氧化碳气体散逸到空气中,所以表面上看,木炭的质量减少,实际上,燃烧掉的木炭的质量加上消耗的氧气的质量一定等于生成的二氧化碳的质量。(2)生石灰久置在空气中,会与空气中的水反应生成氢氧化钙,所以其质量必然会增加。也就是生石灰的质量加上水的质量一定等于生成的氢氧化钙的质量。三.化学反应的表示方法----化学方程式。化学方程式:用化学式表示化学反应的式子。例如:碳在氧气中燃烧C+O2CO2四.化学方程式的写法:(1)以客观事实为依据(2)符合质量守恒定律分三步(1)依据实验事实,把反应物的化学式写在左边,生成物的化学式写在右边,反应物与生成物之间用一条短线相连(2)根据质量守恒定律,化学方程式要配平(使反应前后每种原子的数目相等)。(3)要在化学方程式中注明反应发生的条件和生成物的状态。(用“↓”表示生成物中的沉淀,用“↑”表示生成物中的气体。)以“碳在氧气中燃烧”为例说明①C+O2----CO2②C+O2=CO2③C+O2CO2在上述三个书写步骤中,以化学方程式的配平最为关键。五.化学方程式的配平在反应物、生成物的化学式前填上适当的系数,使式子左、右两边的每一种元素的原子总数相等,这个过程叫化学方程式的配平。理论依据----质量守恒定律反映出:在化学反应前后原子的种类、数目和质量均不变。以磷在空气中燃烧生成五氧化二磷的反应为例,说明书写化学方程式的具体步骤。1.根据实验事实写出反应物及生成物的化学式P+O2─P2O52.配平化学方程式(最小公倍数法)先找出原子个数相差较多的原子进行配平。(有氧先配平氧原子!!)①P+O2─2P2O5②P+5O2─2P2O5③4P+5O2─2P2O5④4P+5O2=2P2O5(把短线改等号。)3.注明反应发生的条件和生成物的状态4P+5O22P2O5常见的反应条件有:点燃、加热(△)、高温、催化剂等。不能混用!!!生成物的状态是指:“↑”(气体)“↓”(沉淀)注意:①在反应物中无气体参加反应,则生成的气体物质注“↑”号,否则不标注“↑”。如:C+O2CO2;②在溶液中进行的化学反应,反应物无难溶性物质参加反应,则生成的难溶性固体要注“↓”号。〔小结〕书写化学方程式具体步骤(韵语)左边反应物,右边生成物,写好化学式,方程要配平短线改等号条件要注明生成气体或沉淀,上下箭头来分清。六.根据化学方程式计算例题1.在实验室中,将含有15.3g过氧化氢的溶液与少量二氧化锰混合,求过氧化氢完全分解后,生成的氧气质

是你****芹呀
 实名认证
实名认证
 内容提供者
内容提供者
最近下载
最新上传
2024年安徽省六安市金寨县二级建造师考试水利水电工程管理与实务考前冲刺试卷及答案.docx
2024年安徽省六安市金寨县二级建造师考试水利水电工程管理与实务考前冲刺试卷完整版.docx
2025年高考河南省化学真题试卷(网络收集版).pdf
2025年高考江苏卷物理真题(网络收集版).pdf
2025年高考山东地理真题(网络收集版).pdf
2025年高考山东卷物理真题(网络收集版).pdf
2025高考广西卷物理真题及答案(网络收集版).pdf
2025年高考安徽卷化学真题及答案(网络收集版).pdf
2025年黑吉辽蒙化学高考真题试卷及答案-黑龙江卷(网络收集版).pdf
2025年高考云南省物理真题及答案(网络收集版).pdf


















