课件-广东-2017_广东省2017年中考化学总复习 第五部分 专题突破 专题一 科学探究 第四节 化学工艺流程课件.ppt
 立即下载
立即下载




如果您无法下载资料,请参考说明:
1、部分资料下载需要金币,请确保您的账户上有足够的金币
2、已购买过的文档,再次下载不重复扣费
3、资料包下载后请先用软件解压,在使用对应软件打开
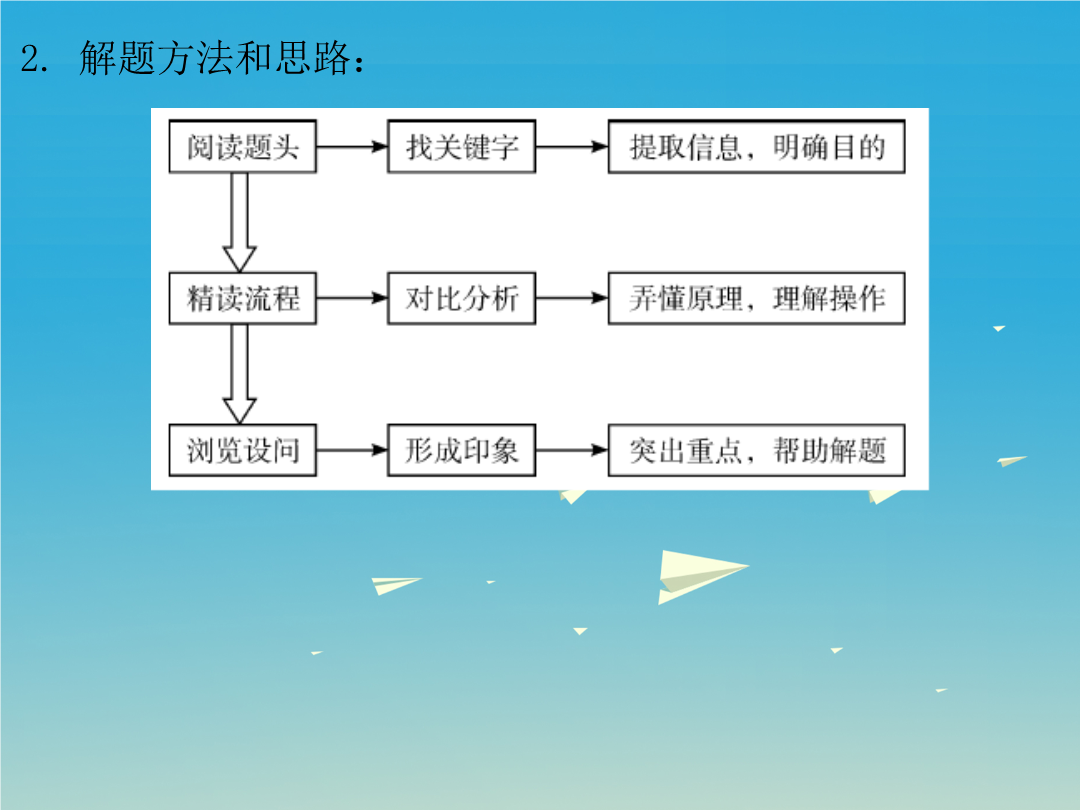
第五部分专题突破考情分析考点梳理2.解题方法和思路:二、几个常见的工业流程1.海水资源的开发和利用。2.金属冶炼和金属回收。3.石灰石工业。4.污水处理工业。5.金属回收工业。6.物质制备工业。(1)铜屑表面呈绿色的物质化学式是Cu2(OH)2CO3,俗称_______,操作①所用到的玻璃仪器有:烧杯、玻璃棒和__________。(2)溶液A的溶质有__________(只写一种);铁锈与稀硫酸反应的化学方程式为____________。(3)两种方法比较,符合绿色化学要求的是方法__________;方法Ⅱ的化学方程式为:2Cu+2H2SO4+_______====2CuSO4+___________,操作②实验步骤为:__________、降温结晶。解析:(1)碱式碳酸铜俗称铜绿,过滤中要用到的玻璃仪器有:烧杯、漏斗和玻璃棒。(2)铜绿和稀硫酸反应生成硫酸铜和水还有二氧化碳,氧化铁和稀硫酸反应生成硫酸铁和水,硫酸过量。(3)方法Ⅰ中产生二氧化硫,二氧化硫是有毒气体会污染空气;方法Ⅱ是铜、稀硫酸和氧气反应生成硫酸铜和水,比较环保;为了得到硫酸铜晶体,先浓缩得到饱和溶液再冷却饱和溶液即可。答案:(1)铜绿漏斗(2)硫酸铜(或硫酸亚铁或硫酸)Fe2O3+3H2SO4====Fe2(SO4)3+3H2O(3)ⅡO22H2O蒸发浓缩【例2】(2015佛山)现代循环经济要求综合考虑环境污染和经济效益。高纯氧化铁可作现代电子工业的材料,图5-1-4-2是以硫铁矿烧渣(主要成分为Fe2O3、Fe3O4、FeO、SiO2)为原料制备高纯氧化铁(Fe2O3)的生产流程示意图:[(NH4)2CO3溶液呈碱性,40℃以上时(NH4)2CO3分解](1)实验室中,操作Ⅰ、操作Ⅱ用到的玻璃仪器有玻璃棒、烧杯、_________等。(2)滤液Ⅰ中主要的阳离子是__________等。(3)加适量氨水的目的是_________________。(4)根据题中信息,加入(NH4)2CO3后,该反应必须控制的条件是:____________________________________。(5)滤液Ⅱ中回收的产品是____________________(写化学式)。(6)写出在空气中煅烧FeCO3的化学方程式:______________________________________。解析:(1)据图可以看出,经过操作Ⅰ、操作Ⅱ得到的是滤液和固体,故是过滤操作,用到的玻璃仪器有玻璃棒、烧杯、漏斗。(2)一氧化碳能将氧化铁还原为铁,将氧化亚铁还原为铁,故硫铁矿高温通入一氧化碳得到的固体中主要含有的是铁,稀硫酸能与铁反应生成硫酸亚铁和氢气,故含有亚铁离子,由于硫酸过量,故含有氢离子。(3)由于硫酸过量,溶液呈酸性,氨水呈碱性,加适量氨水能将溶液调节为中性。(4)根据题中信息,40℃以上时(NH4)2CO3分解,故加入(NH4)2CO3后,该反应必须控制温度低于40℃。(5)碳酸铵能与硫酸亚铁反应生成碳酸亚铁和硫酸铵,故滤液Ⅱ中可回收的产品是硫酸铵。(6)在空气中煅烧FeCO3生成氧化铁和二氧化碳。答案:(1)漏斗(2)Fe2+、H+(3)调节溶液的酸碱性(4)温度低于40℃(5)(NH4)2SO4(6)考题再现1.(2016广州)保险粉(化学式为Na2S2O4)在工农业生产中有广泛的用途,Na2S2O4在碱性溶液中稳定,在中性和酸性溶液中极不稳定,在NaCl存在下,Na2S2O4在水中溶解度显著下降。制备流程如图5-1-4-3:(1)反应Ⅰ的原理为Zn+2SO2====ZnS2O4,该反应类型为____________。(2)反应Ⅱ为复分解反应,该反应的化学方程式为_______________________________________。(3)操作a的名称为________。(4)滤液中含有Na2S2O4,为使Na2S2O4结晶析出还需要加入少量NaOH的原因是________________________________________,加入NaCl的原因是_____________________________________________________________________________。(5)198gZn(OH)2理论上能得到Zn的质量为______g。2.(2016梅州)工业上以粗盐(含少量MgCl2、CaCl2杂质)为原料,利用电解饱和食盐水的方法制备NaOH,其简要工艺流程如下:(1)步骤①中发生反应的基本反应类型是__________反应。(2)步骤③中加入适量稀盐酸的目的是________________________________。(3)验证步骤②中Ca

森林****io
 实名认证
实名认证
 内容提供者
内容提供者
最近下载
一种胃肠道超声检查助显剂及其制备方法.pdf
201651206021+莫武林+浅析在互联网时代下酒店的营销策略——以湛江民大喜来登酒店为例.doc
201651206021+莫武林+浅析在互联网时代下酒店的营销策略——以湛江民大喜来登酒店为例.doc
用于空间热电转换的耐高温涡轮发电机转子及其装配方法.pdf
用于空间热电转换的耐高温涡轮发电机转子及其装配方法.pdf
用于空间热电转换的耐高温涡轮发电机转子及其装配方法.pdf
用于空间热电转换的耐高温涡轮发电机转子及其装配方法.pdf
用于空间热电转换的耐高温涡轮发电机转子及其装配方法.pdf
用于空间热电转换的耐高温涡轮发电机转子及其装配方法.pdf
论《离骚》诠释史中的“香草”意蕴.docx


















