


如果您无法下载资料,请参考说明:
1、部分资料下载需要金币,请确保您的账户上有足够的金币
2、已购买过的文档,再次下载不重复扣费
3、资料包下载后请先用软件解压,在使用对应软件打开
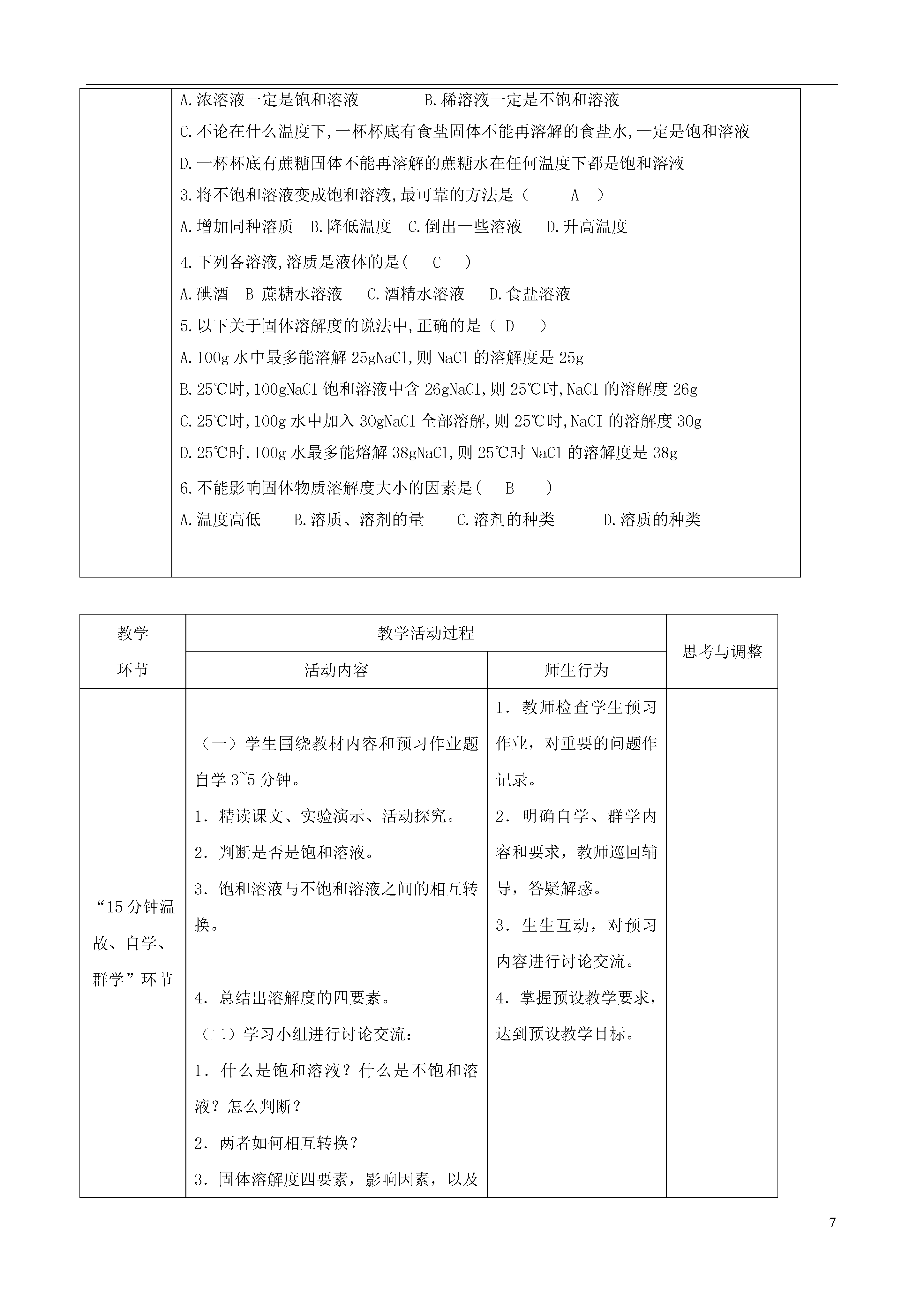
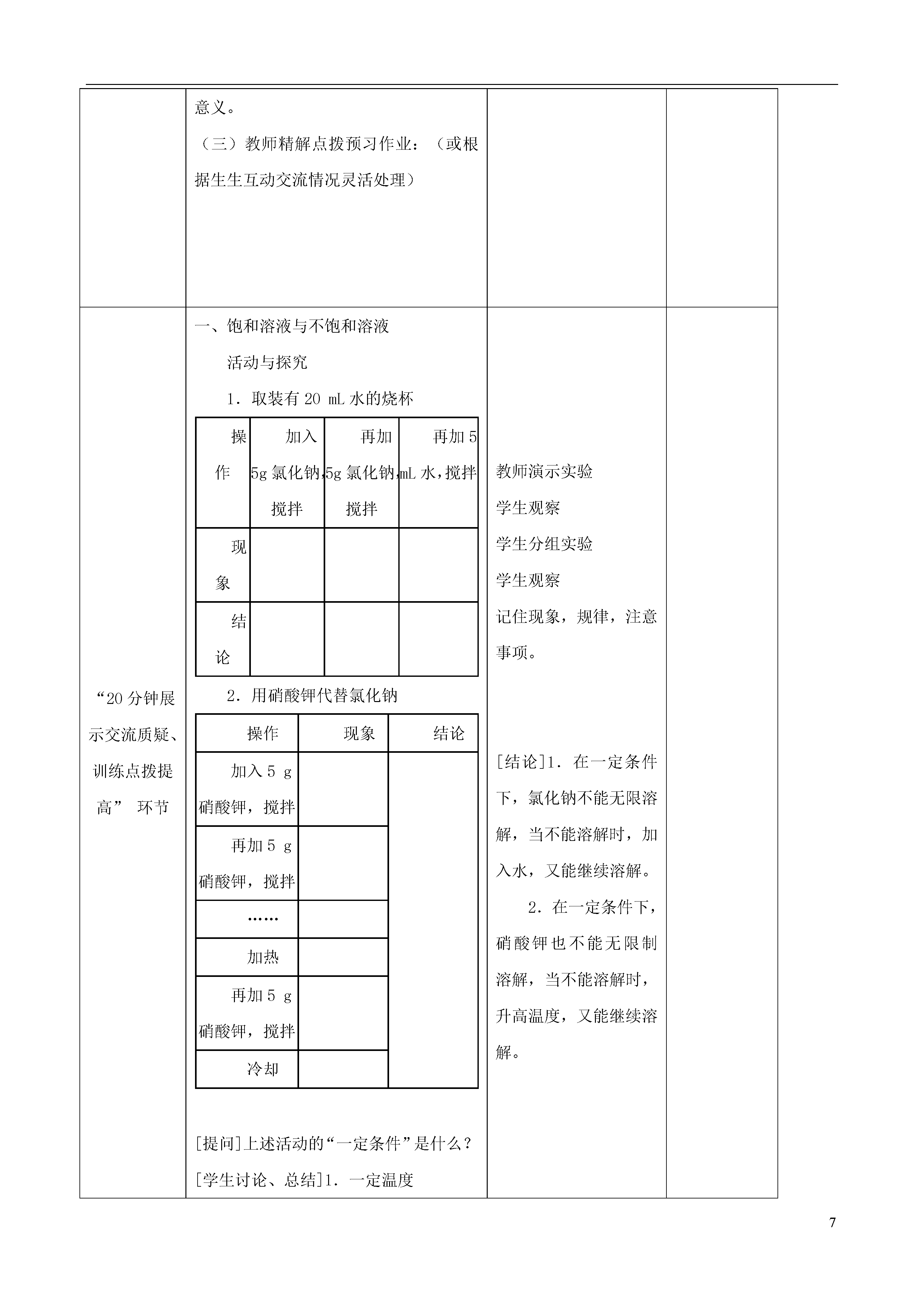
7第九单元课题2溶解度第1课时总第个教案教学三维目标知识与技能(1)理解饱和溶液的涵义。(2)了解溶解度涵义,过程与方法(1)学习观察、分析实验现象,并能归纳出相应的概念。(2)学习通过实验解决问题情感态度价值观(1)认识矛盾的双方在一定条件下可以相互转化的辩证唯物主义思想。(2)树立做任何事情都要实事求是的观点。教学重点理解饱和溶液和溶解度的概念教学难点1.理解饱和溶液和溶解度的概念。2.正确理解固体物质溶解度的概念。教具学具仪器:烧杯、玻璃棒、酒精灯、蒸发皿、药匙、天平、砝码、量筒、石棉网、铁架台、药品:氯化钠、硝酸钾教学设计:本节课预习作业题一、填空题1.在一定温度下,在一定量溶剂里,还能继续溶解某种溶质的溶液叫做这种溶质的不饱和溶液,不能继续溶解某种溶质的溶液叫做这种溶质的饱和溶液。2.接近饱和的硝酸钾溶液变为饱和溶液的方法有降温、增加溶质、增发溶剂。3.溶解度表示在一定温度下,某固态物质在100g溶剂里达到饱和状态时所溶解的质量。4·氯化纳在20oC时的溶解度为36g,这说明20摄氏度时,100克水中溶解36克氯化钠达到饱和状态。二、选择题1在一定温度下,某物质的饱和溶液一定是(B)A.含溶质量多的溶液B.不能再溶解该物质的溶液C.含溶质量少的溶液D.还能再溶解该物质的溶液2.下列说法正确的是(C)A.浓溶液一定是饱和溶液B.稀溶液一定是不饱和溶液C.不论在什么温度下,一杯杯底有食盐固体不能再溶解的食盐水,一定是饱和溶液D.一杯杯底有蔗糖固体不能再溶解的蔗糖水在任何温度下都是饱和溶液3.将不饱和溶液变成饱和溶液,最可靠的方法是(A)A.增加同种溶质B.降低温度C.倒出一些溶液D.升高温度4.下列各溶液,溶质是液体的是(C)A.碘酒B蔗糖水溶液C.酒精水溶液D.食盐溶液5.以下关于固体溶解度的说法中,正确的是(D)A.100g水中最多能溶解25gNaCl,则NaCl的溶解度是25gB.25℃时,100gNaCl饱和溶液中含26gNaCl,则25℃时,NaCl的溶解度26gC.25℃时,100g水中加入3OgNaCl全部溶解,则25℃时,NaCI的溶解度3OgD.25℃时,100g水最多能熔解38gNaCl,则25℃时NaCl的溶解度是38g6.不能影响固体物质溶解度大小的因素是(B)A.温度高低B.溶质、溶剂的量C.溶剂的种类D.溶质的种类教学环节教学活动过程思考与调整活动内容师生行为“15分钟温故、自学、群学”环节(一)学生围绕教材内容和预习作业题自学3~5分钟。1.精读课文、实验演示、活动探究。2.判断是否是饱和溶液。3.饱和溶液与不饱和溶液之间的相互转换。4.总结出溶解度的四要素。(二)学习小组进行讨论交流:1.什么是饱和溶液?什么是不饱和溶液?怎么判断?2.两者如何相互转换?3.固体溶解度四要素,影响因素,以及意义。(三)教师精解点拨预习作业:(或根据生生互动交流情况灵活处理)1.教师检查学生预习作业,对重要的问题作记录。2.明确自学、群学内容和要求,教师巡回辅导,答疑解惑。3.生生互动,对预习内容进行讨论交流。4.掌握预设教学要求,达到预设教学目标。“20分钟展示交流质疑、训练点拨提高”环节一、饱和溶液与不饱和溶液活动与探究1.取装有20mL水的烧杯操作加入5g氯化钠,搅拌再加5g氯化钠,搅拌再加5mL水,搅拌现象结论2.用硝酸钾代替氯化钠操作现象结论加入5g硝酸钾,搅拌再加5g硝酸钾,搅拌……加热再加5g硝酸钾,搅拌冷却[提问]上述活动的“一定条件”是什么?[学生讨论、总结]1.一定温度2.一定量的溶剂[追问]如果不指明这两个条件,能否说某物质的溶解量是有限的?[学生讨论、回答]不能。因为我们可以改变温度、改变溶剂的量,使溶质无限制地溶解。[引导]我们把一定条件下不能继续溶解溶质的溶液叫饱和溶液,相反,还能继续溶解溶质的溶液叫不饱和溶液。[思考]请大家根据刚才的分析,总结饱和溶液与不饱和溶液的科学概念。[提问]1.通过活动与探究可看出饱和溶液与不饱和溶液的根本区别是什么?2.如何判断某一溶液是否饱和?[提问]回想课上的活动与探究,试分析如何将一瓶已经饱和的硝酸钾溶液转化成不饱和溶液。调动学生的逆向思维,思考:如何将接近饱和的溶液转化为饱和溶液?3.饱和溶液与不饱和溶液的相互转化:一般情况下:二、固体溶解度⒈溶解度在一定温度下,某固态物质在100g溶剂里达到饱和状态时所溶解的质量,叫做这种物质溶解在这种溶剂里的溶解度。理解溶解度概念时应注意哪些问题?2思考:影响固体溶解度的因素有哪些⒊溶解性与溶
Ta的资源

2025年龙里县二级建造师考试水利水电工程管理与实务深度预测试题含解析

2025年龙里县人力资源管理师四级理论知识高分冲刺试题(附答案及解析)

2025年龙胜各族自治县人力资源管理师四级理论知识预测试题完整版

2025年龙川县二级建造师考试水利水电工程管理与实务考前冲刺试题(附答案及解析)

2025年龙岩市漳平市人力资源管理师四级理论知识深度预测试卷完整版

2025年齐齐哈尔市碾子山区人力资源管理师二级理论知识全真模拟试卷(附答案及解析)

2025年齐齐哈尔市建华区人力资源管理师四级理论知识全真模拟试题完整版

2025年齐齐哈尔市富拉尔基区人力资源管理师四级理论知识深度预测试题完整版

2025年齐齐哈尔市克山县人力资源管理师四级理论知识预测试卷含解析

2025年齐齐哈尔市人力资源管理师二级理论知识高分冲刺试题(附答案及解析)

邻家****mk
 实名认证
实名认证
 内容提供者
内容提供者
最近下载
最新上传
2025年龙门县人力资源管理师四级理论知识高分通关卷及答案.docx
2025年龙门县人力资源管理师四级理论知识高分冲刺试题及答案.docx
2025年龙门县人力资源管理师四级理论知识高分冲刺试卷及答案.docx
2025年龙门县人力资源管理师四级理论知识预测试卷及答案.docx
2025年龙门县人力资源管理师四级理论知识预测试题及答案.docx
2025年龙门县人力资源管理师四级理论知识预测密卷及答案.docx
2025年龙门县人力资源管理师四级理论知识考前冲刺预测试卷及答案.docx
2025年龙门县人力资源管理师四级理论知识考前冲刺试题及答案.docx
2025年龙门县人力资源管理师四级理论知识点睛提分卷及答案.docx
2025年龙门县人力资源管理师四级理论知识深度预测试题及答案.docx








