


如果您无法下载资料,请参考说明:
1、部分资料下载需要金币,请确保您的账户上有足够的金币
2、已购买过的文档,再次下载不重复扣费
3、资料包下载后请先用软件解压,在使用对应软件打开
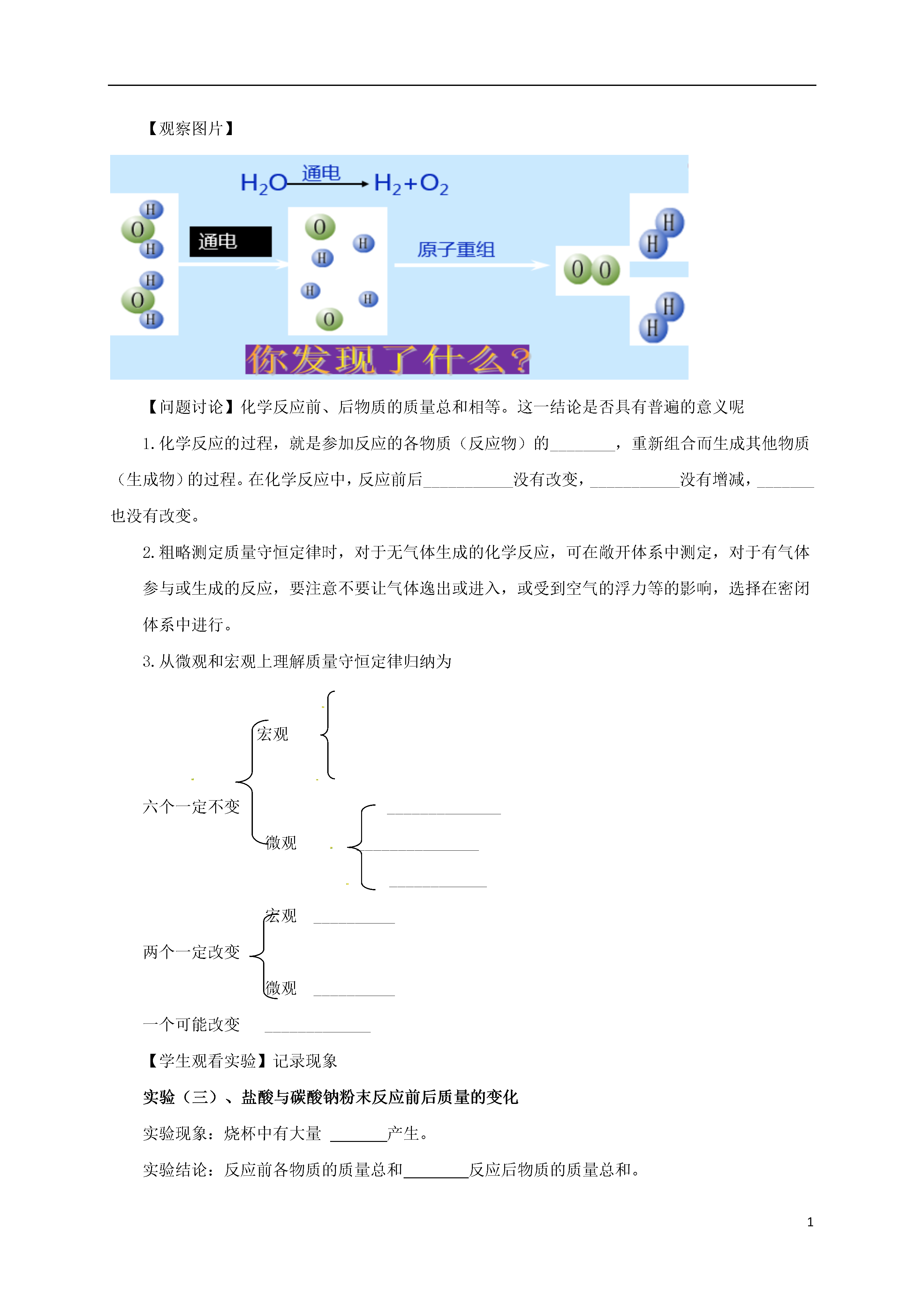
17.1.1质量守恒定律教学目标1、通过实验测定,记住质量守恒定律,并用分子、原子的观点解释该定律。2、初步学会应用实验方法来定量研究问题和分析问题。3、质量守恒定律的简单应用。重点和难点:1、通过实验测定,记住质量守恒定律,并用分子、原子的观点解释该定律。2、质量守恒定律的简单应用。教学方法:自学、讨论、实验、讲解教学设计一、情境引入:铁丝燃烧后,质量会变大,所以化学反应质量是变大的,木材燃烧完后,只剩下会,所以化学反应质量是变小的,你说对吗?这是我们今天要学习的内容?二、预习检测:1、给水通电时,水分子分解成了和,然后这些原子进行重新组合,生成了和,大量的分子聚集在一起,分别生成了和。在这个过程中,氢、氧原子的种类、数目、质量(有或没有)发生变化。因此,被分解水的质量(等于或不等于)生成的氢气与氧气的质量和。2、叫做质量守恒定律。3、在化学反应前后,原子的没有改变,原子的没有增减,原子的也没有改变,因此化学反应遵循质量守恒定律。三、新知新解:实验(一)白磷燃烧前后质量的测定【学生观看实验】作好记录实验现象:白磷燃烧,产生大量的,放出大量的,玻璃管上得气球先变后变。实验结论:天平,反应前后物质的总质量。反应表达式:。思考问题:红热玻璃棒的作用是白磷,说明白磷的燃点,锥形瓶底放入少量的沙的作用是:防止溅落物炸裂瓶底。实验(二)、铁钉与硫酸铜溶液反应前后质量的测定实验现象:铁钉表面,溶液由蓝色变为。实验结论:反应前后物质的总质量。反应表达式:。【思考问题】:经过实验证明:的各物质的质量总和,反应后的各物质质量,这个规律叫。分析比较两个方案的实验结果,能得到什么结论?【小结】参加化学反应的各物质的质量总和,等于反应后生成的各物质的质量总和。【问题讨论】1.质量守恒定律适用于所有___________。2.质量守恒定律的“守恒”指的是_________守恒,其它方面如_______等不一定守恒。3.守恒的范围是“_______化学反应的各物质”,没有参加反应的物质,不能计算在内。4.“参加化学反应的各物质的质量总和”,应当包括各种物质,如________等。5.“生成的各物质的质量总和”,应当包括生成的各种物质,如_______、_______等。【观察图片】【问题讨论】化学反应前、后物质的质量总和相等。这一结论是否具有普遍的意义呢化学反应的过程,就是参加反应的各物质(反应物)的________,重新组合而生成其他物质(生成物)的过程。在化学反应中,反应前后___________没有改变,___________没有增减,_______也没有改变。2.粗略测定质量守恒定律时,对于无气体生成的化学反应,可在敞开体系中测定,对于有气体参与或生成的反应,要注意不要让气体逸出或进入,或受到空气的浮力等的影响,选择在密闭体系中进行。3.从微观和宏观上理解质量守恒定律归纳为宏观六个一定不变______________微观___________________________宏观__________两个一定改变微观__________一个可能改变_____________【学生观看实验】记录现象实验(三)、盐酸与碳酸钠粉末反应前后质量的变化实验现象:烧杯中有大量产生。实验结论:反应前各物质的质量总和反应后物质的质量总和。结论分析:反应是有大量的逸出,如果把气体收集起来,反应前后各物质的总质量仍然。反应表达式:。实验(四)、镁带燃烧前后质量的测定实验现象:燃烧,发出光,生成。实验结论:反应前各物质的质量总和反应后各物质的质量。结论分析:由于有参加反应,所以生成的的质量大于镁带的质量。【思考】1、按照“质量守恒定律”概念的理解,一切化学反应都要遵守质量守恒定律,为什么在实验(三)、实验(四)中看不到?2、为什么物质在发生化学反应前后,各物质的质量总和相等?【教师】理解质量守恒定律的定义时要注意1.质量守恒定律适用于所有化学反应。2.质量守恒定律的“守恒”指的是质量守恒,其它方面如体积等不一定守恒。四、随堂练习:1.氢气和氧气的混合气体共20克,在点燃的条件下,让它们充分反应后,生成9克水,则原混合气体中含有氢气的质量可能是()A.8克B.12克C.11克D.无法确定2.已知化学方程式:R+2O2CO2+2H2O,则关于R组成的叙述正确的是()A.只含有碳元素B.只含碳、氢元素C.一定含碳、氢、氧元素D.一定含碳、氢元素,可能含氧元素3.煤燃烧时会排放出二氧化硫、二氧化氮等污染物.在一定条件下,二氧化硫与二氧化氮能发生反应:SO2+NO2=SO3+X,其中X的化学式为()A.N2B.NOC.

是浩****32
 实名认证
实名认证
 内容提供者
内容提供者
最近下载


















