

如果您无法下载资料,请参考说明:
1、部分资料下载需要金币,请确保您的账户上有足够的金币
2、已购买过的文档,再次下载不重复扣费
3、资料包下载后请先用软件解压,在使用对应软件打开
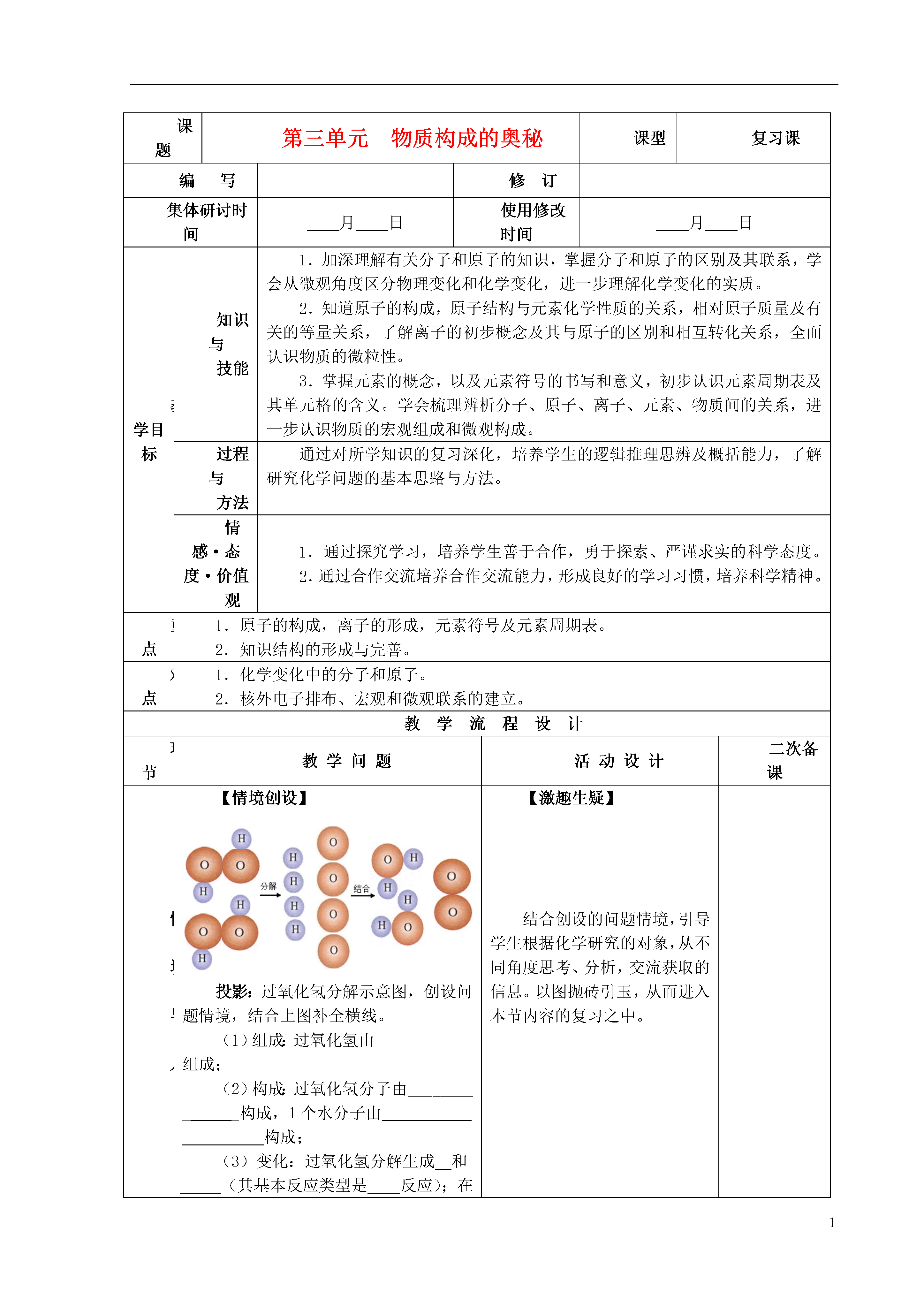
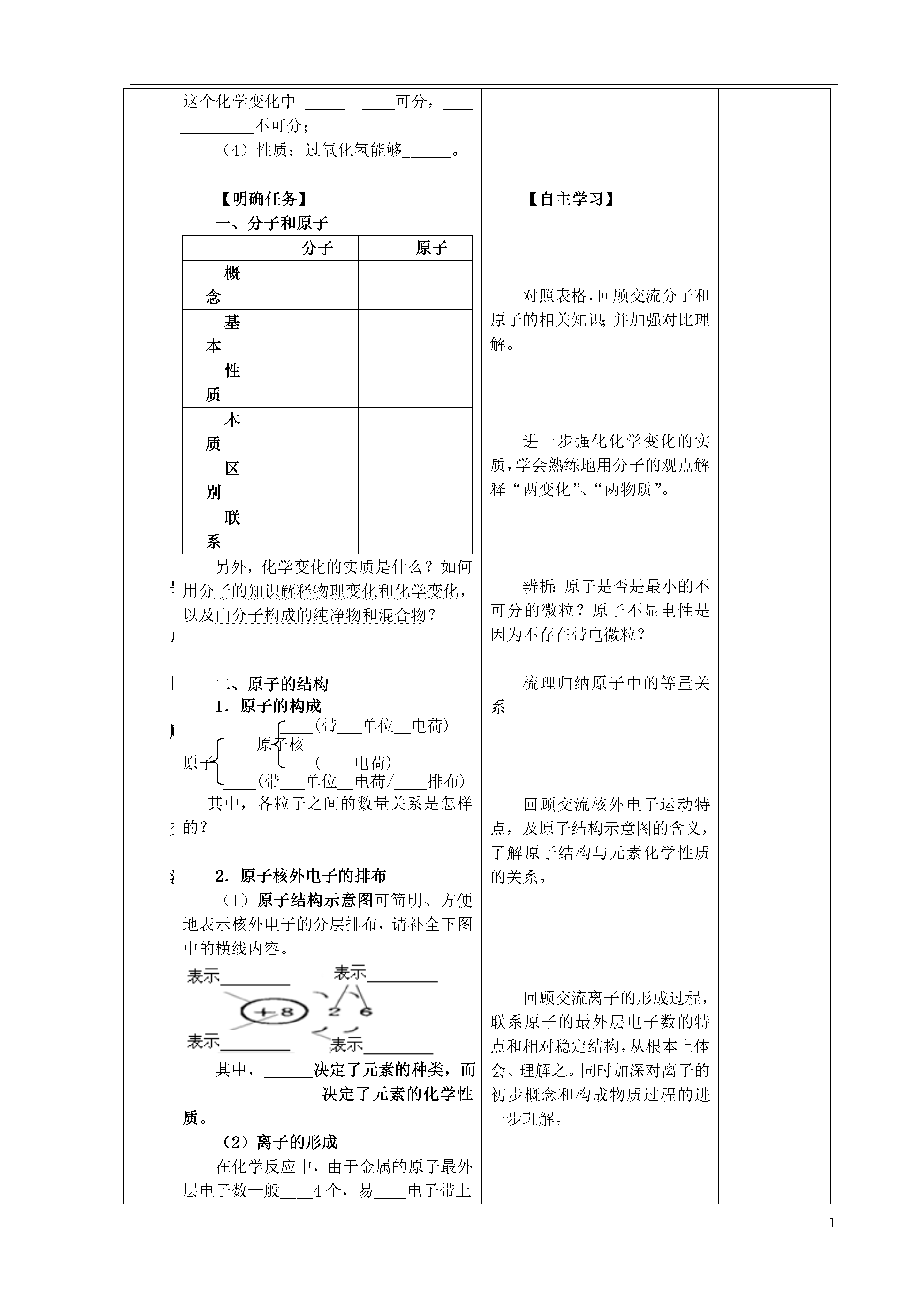
1课题第三单元物质构成的奥秘课型复习课编写修订集体研讨时间月日使用修改时间月日教学目标知识与技能1.加深理解有关分子和原子的知识,掌握分子和原子的区别及其联系,学会从微观角度区分物理变化和化学变化,进一步理解化学变化的实质。2.知道原子的构成,原子结构与元素化学性质的关系,相对原子质量及有关的等量关系,了解离子的初步概念及其与原子的区别和相互转化关系,全面认识物质的微粒性。3.掌握元素的概念,以及元素符号的书写和意义,初步认识元素周期表及其单元格的含义。学会梳理辨析分子、原子、离子、元素、物质间的关系,进一步认识物质的宏观组成和微观构成。过程与方法通过对所学知识的复习深化,培养学生的逻辑推理思辨及概括能力,了解研究化学问题的基本思路与方法。情感·态度·价值观1.通过探究学习,培养学生善于合作,勇于探索、严谨求实的科学态度。2.通过合作交流培养合作交流能力,形成良好的学习习惯,培养科学精神。重点1.原子的构成,离子的形成,元素符号及元素周期表。2.知识结构的形成与完善。难点1.化学变化中的分子和原子。2.核外电子排布、宏观和微观联系的建立。教学流程设计环节教学问题活动设计二次备课情境导入【情境创设】投影:过氧化氢分解示意图,创设问题情境,结合上图补全横线。(1)组成:过氧化氢由____________组成;(2)构成:过氧化氢分子由____________构成,1个水分子由构成;(3)变化:过氧化氢分解生成和(其基本反应类型是反应);在这个化学变化中______可分,不可分;(4)性质:过氧化氢能够______。【激趣生疑】结合创设的问题情境,引导学生根据化学研究的对象,从不同角度思考、分析,交流获取的信息。以图抛砖引玉,从而进入本节内容的复习之中。要点回顾与交流要点回顾与交流【明确任务】一、分子和原子分子原子概念基本性质本质区别联系另外,化学变化的实质是什么?如何用分子的知识解释物理变化和化学变化,以及由分子构成的纯净物和混合物?二、原子的结构1.原子的构成(带单位电荷)原子核原子(电荷)(带单位电荷/排布)其中,各粒子之间的数量关系是怎样的?2.原子核外电子的排布(1)原子结构示意图可简明、方便地表示核外电子的分层排布,请补全下图中的横线内容。其中,决定了元素的种类,而决定了元素的化学性质。(2)离子的形成在化学反应中,由于金属的原子最外层电子数一般____4个,易____电子带上电荷,形成离子(填“阳或阴”,下同);而非金属原子的最外层一般____4个,易______电子带上电荷,形成离子;都趋于达到相对稳定结构。这样两种带相反电荷的离子相互作用就构成了物质。可见,离子就是的原子,它也是构成物质的一种粒子。3.相对原子质量(1)概念是什么?(2)它的近似值是哪两个数之和?三、元素及元素周期表1.什么是元素?它在化学变化会不会发生改变?2.元素与原子、分子、离子的区别和联系是什么?3.元素周期表的编排依据是什么?其结构是怎样的?每一个单元格都包含哪些内容?【自主学习】对照表格,回顾交流分子和原子的相关知识;并加强对比理解。进一步强化化学变化的实质,学会熟练地用分子的观点解释“两变化”、“两物质”。辨析:原子是否是最小的不可分的微粒?原子不显电性是因为不存在带电微粒?梳理归纳原子中的等量关系回顾交流核外电子运动特点,及原子结构示意图的含义,了解原子结构与元素化学性质的关系。回顾交流离子的形成过程,联系原子的最外层电子数的特点和相对稳定结构,从根本上体会、理解之。同时加深对离子的初步概念和构成物质过程的进一步理解。回顾相对原子质量的概念,定义式,及近似计算回顾元素定义及其在化学变化的表现。教师指导辨析元素、分子、原子、离子之间的关系,以及应用范围的不同,强化记忆地壳及生物体内元素之最。查阅元素周期表,交流从中获得的信息。教师引导学生尝试总结其中周期性的一些规律。定位提升通过本课的学习,你有哪些收获?通过投影、板书展现这些知识间的关系知能应用知能应用例1:关于氧气和铁的构成,下列说法正确的是()A.分别由氧元素、铁元素构成B.分别由氧分子、铁原子构成C.分别由氧原子、铁原子构成D.分别由氧分子、铁分子的构成【强化训练一】完善学案上的学习过程中的导学提纲

白凡****12
 实名认证
实名认证
 内容提供者
内容提供者
最近下载
一种胃肠道超声检查助显剂及其制备方法.pdf
201651206021+莫武林+浅析在互联网时代下酒店的营销策略——以湛江民大喜来登酒店为例.doc
201651206021+莫武林+浅析在互联网时代下酒店的营销策略——以湛江民大喜来登酒店为例.doc
用于空间热电转换的耐高温涡轮发电机转子及其装配方法.pdf
用于空间热电转换的耐高温涡轮发电机转子及其装配方法.pdf
用于空间热电转换的耐高温涡轮发电机转子及其装配方法.pdf
用于空间热电转换的耐高温涡轮发电机转子及其装配方法.pdf
用于空间热电转换的耐高温涡轮发电机转子及其装配方法.pdf
用于空间热电转换的耐高温涡轮发电机转子及其装配方法.pdf
论《离骚》诠释史中的“香草”意蕴.docx


















