教案-全国-2016_北大绿卡九年级化学上册 第四单元 课题4 化学式与化合价(第2课时)教案 (新版)新人教版.doc
 立即下载
立即下载



如果您无法下载资料,请参考说明:
1、部分资料下载需要金币,请确保您的账户上有足够的金币
2、已购买过的文档,再次下载不重复扣费
3、资料包下载后请先用软件解压,在使用对应软件打开
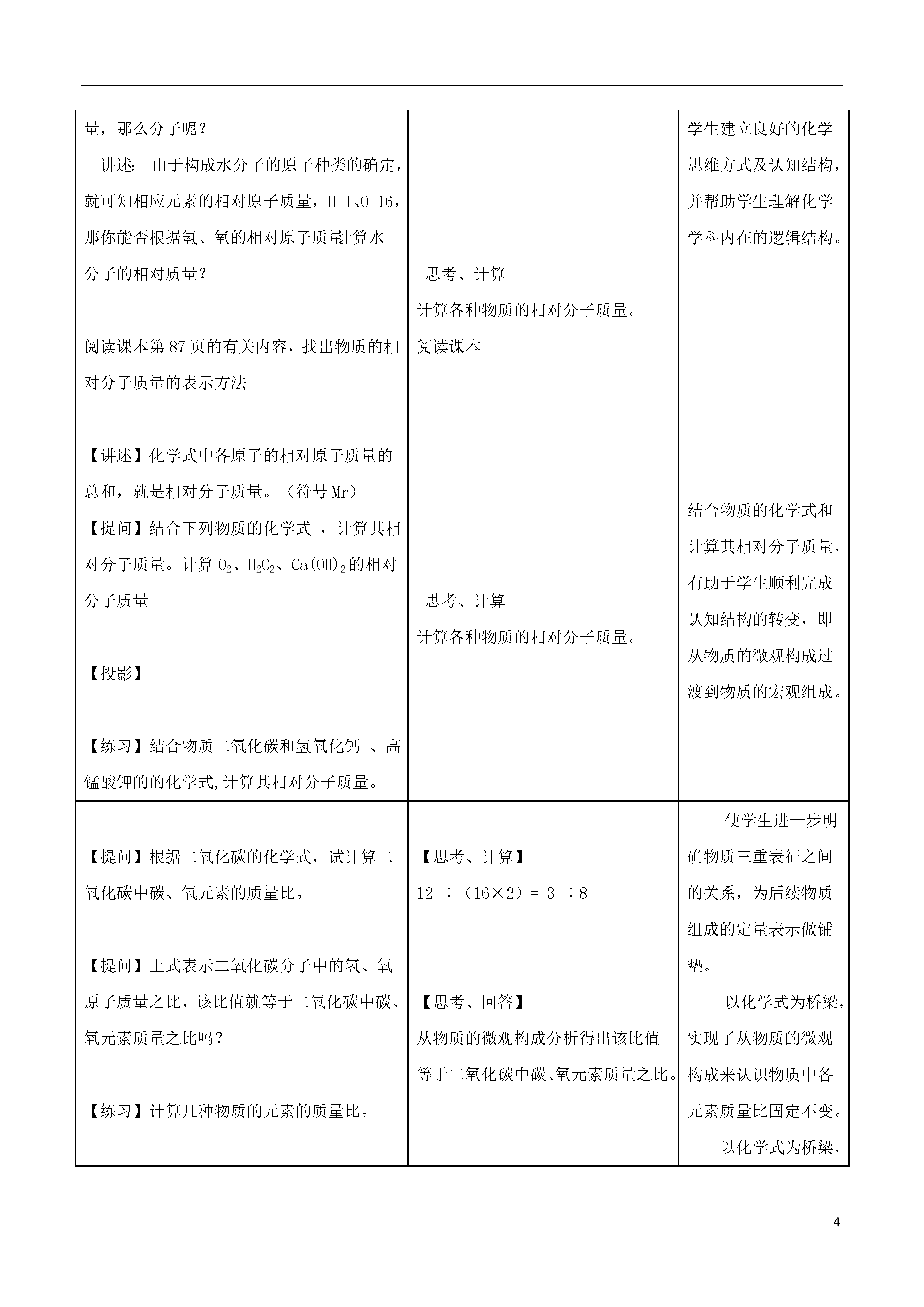
4化学式与化合价一、教学目标:知识与技能(1)理解相对分子质量的涵义,能利用相对原子质量和相对分子质量计算物质的组成。(2)能看懂某些商品标签或说明书上、标示的物质成分和含量,并会进行相关计算。过程与方法(1)通过解密物质的相对分子质量,自主构建相对分子质量的定义。(2)通过探寻物质中元素质量大小,在积极思考、解决问题的过程中,初步学会用化学的思维解决化学问题。情感态度与价值观(1)通过识别生活中各种商品标签、说明书,了解各种成分及含量,感受化学就在我们身边,增强对化学的热爱之情。(2)通过解决标签中的问题,体会化学的学科价值,树立化学源于生活服务于生活的理念。二、教学重点、难点:重点:根据化学式进行相对分子质量、元素质量比及元素质量分数的计算。难点:能根据化学式相关计算解决商品标签中的问题。三、教学过程:教师活动学生活动教学意图出示水的化学式“H2O”,提问1、水有质量吗?2、水由什么构成的?3、水分子有质量吗?4、水分子由什么构成的?化学式就像一座桥梁将宏观的物质与物质的微观构成紧紧的联系在了一起。如水(H2O)的化学式从宏观而言可表示水及其元素组成,微观表示一个水分子和一个水分子中的原子构成。提问:原子的质量很小,分子的质量也很小,原子可以用相对原子质量来表示它的质量,那么分子呢?讲述:由于构成水分子的原子种类的确定,就可知相应元素的相对原子质量,H-1、O-16,那你能否根据氢、氧的相对原子质量计算水分子的相对质量?阅读课本的有关内容,找出物质的相对分子质量的表示方法【讲述】化学式中各原子的相对原子质量的总和,就是相对分子质量。(符号Mr)【提问】结合下列物质的化学式,计算其相对分子质量。计算O2、H2O2、Ca(OH)2的相对分子质量【投影】【练习】结合物质二氧化碳和氢氧化钙、高锰酸钾的的化学式,计算其相对分子质量。思考,回忆上节课学习的内容思考、聆听在头脑中逐步建立起宏观、微观、符号三者之间的联系。思考、计算计算各种物质的相对分子质量。阅读课本思考、计算计算各种物质的相对分子质量。复习化学学习中学生对物质进行的宏观表征、微观表征和符号表征以及建立三者间的联系是化学学科不同于其他科学最典型的思维方式,来促进学生建立良好的化学思维方式及认知结构,并帮助学生理解化学学科内在的逻辑结构。结合物质的化学式和计算其相对分子质量,有助于学生顺利完成认知结构的转变,即从物质的微观构成过渡到物质的宏观组成。【提问】根据二氧化碳的化学式,试计算二氧化碳中碳、氧元素的质量比。【提问】上式表示二氧化碳分子中的氢、氧原子质量之比,该比值就等于二氧化碳中碳、氧元素质量之比吗?【练习】计算几种物质的元素的质量比。【提问】根据水(H2O)的化学式,计算水中氢元素的质量分数。【讲述】物质中某元素的质量分数,就是该元素的质量与组成物质的元素总质量之比。例题3:计算硝酸铵中氮元素的质量分数对比物质中各元素质量比和某元素的质量分数。【思考、计算】12︰(16×2)=3︰8【思考、回答】从物质的微观构成分析得出该比值等于二氧化碳中碳、氧元素质量之比。【思考、计算】1×2/18×100%=11.1%明确物质中各元素质量比和物质中某元素的质量分数两者的区别。使学生进一步明确物质三重表征之间的关系,为后续物质组成的定量表示做铺垫。以化学式为桥梁,实现了从物质的微观构成来认识物质中各元素质量比固定不变。以化学式为桥梁,实现了从物质的微观构成来认识物质中某元素质量分数固定不变。运用对比法,有利于充分显示事物的矛盾,突出被表现事物的本质特征。有关相对分子计算的应用:【计算】100千克的硝酸铵中有多少氮元素?【计算】多少吨的硝酸铵中含有100吨的氮元素?【小结】【课题小结】【思考、计算】对本课题的知识体系有一个整体的认识,并把握其重点。知识迁移就是“一种学习对另一种学习的影响”。这种原有的知识结构对新的学习的影响就形成了知识的迁移。知识掌握是知识运用的前提,知识应用是知识掌握的归宿。课堂小结可以帮助学生理清所学知识的层次结构,掌握其外在的形式和内在联系,形成知识体系及一定的结构框架。板书设计有关相对分子质量的计算计算相对分子质量:计算元素的质量比:计算元素的质量分数:计算物质中元素的质量:

雅云****彩妍
 实名认证
实名认证
 内容提供者
内容提供者
最近下载


















