课件-全国-2018_(泰安专版)2018中考化学总复习 第二部分 专题复习 高分保障 专题1 曲线、表格、流程图题课件.ppt
 立即下载
立即下载




如果您无法下载资料,请参考说明:
1、部分资料下载需要金币,请确保您的账户上有足够的金币
2、已购买过的文档,再次下载不重复扣费
3、资料包下载后请先用软件解压,在使用对应软件打开
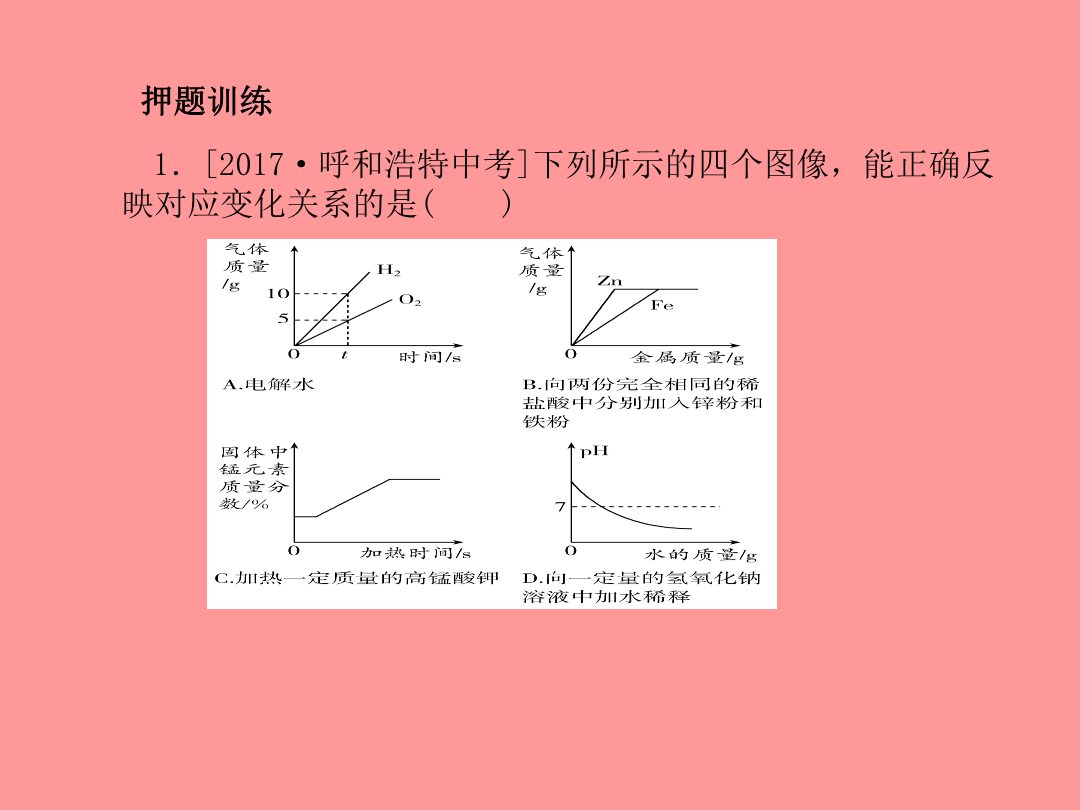
第二部分专题复习高分保障重点类型突破【思路点拨】向一定质量的AgNO3溶液中滴加NaCl溶液生成氯化银沉淀的质量开始不断增加,至AgNO3完全反应完后沉淀的质量就不会再增加了;向一定量的过氧化氢溶液中加入少量二氧化锰,能够快速地生成氧气,但是二氧化锰只能改变反应的速度,而不能改变产物的质量;恒温条件下饱和的KNO3溶液蒸发适量水,溶液中溶质的质量分数不变;氢氧化钠溶液中加水时碱性减弱,pH会减小,但不会因为加水而导致溶液显酸性。押题训练C电解水生成氢气和氧气的体积比是2∶1,而不是质量比,故A错误;由化学方程式:Zn+2HCl===ZnCl2+H2↑,Fe+2HCl===FeCl2+H2↑,可知生成相同质量的氢气需要的锌的质量大于铁,故B错误;高锰酸钾加热一段时间才分解,随着生成氧气质量的增加,固体质量在不断减少,但是锰元素的质量不变,所以固体中锰元素的质量分数变大;反应结束后,固体质量不再减少,则固体中锰元素的质量分数也不再改变,故C正确;氢氧化钠是一种碱,无论加入多少水稀释,溶液仍显碱性,pH始终大于7,故D错误。D由图可知,b点所示溶液的pH<7;d点所示溶液的pH>7,所以b、d点对应溶液的pH:b<d,故A错误;由化学方程式可知:NaOH+HCl===NaCl+H2O4036.5由于题干中没有提及两种溶液的密度,所以无法确定所需氢氧化钠溶液的溶质质量分数,故B错误;由图可知,b点所示溶液的pH<7,溶液显酸性,滴加紫色石蕊溶液变红色,故C错误;d点所示溶液的pH>7,所示溶液的溶质既有酸碱中和生成的氯化钠,还有过量的氢氧化钠,故D正确。【例2】现实生活中,氨气多用作制冷剂及农用化肥,其实它还是一种清洁能源,在纯氧中可以完全燃烧,只生成水和氮气。最近,科学家用一种含钼的化合物作催化剂,在常温下就能完成氨的合成,从而大大降低了生产成本,使得液氨有望取代液氢成为新一代绿色能源。(1),该反应属于基本反应类型的化合反应。(2)请你根据下表信息分析用NH3取代H2作为能源的优点:①由于NH3比H2沸点高,所以更易液化,便于储存和运输。②NH3泄漏时易发现是因为有刺激性气味,同时它易溶于水,便于处理。押题训练B根据质量守恒定律可得X=(18+1+2+32)-(26+2+12)=13,A说法正确;在反应过程中乙的质量由1g增加到26g,乙应是生成物,B说法错误;反应中乙、丁的质量比为(26g-1g)∶(32g-12g)=5∶4,C说法正确;物质丙在反应过程中质量没有变化,可能是催化剂,也可能不参加反应,D说法正确。4.[2017·枣庄中考]在一定条件下,一密闭容器内发生某反应,测得反应前后各物质的质量如下表所示。下列说法错误的是()A.a一定是反应物B.x+y=20C.x的取值范围一定是0≤x≤30D.反应生成c与d的质量比为2∶1C反应后质量增加的物质是生成物,质量减少的物质是反应物,差值是生成的质量或参加反应的质量。c质量增加20g-10g=10g,故c是生成物,d质量增加20g-15g=5g,故d是生成物,两种物质增加的质量之和是15g,而b只有5g,a肯定是反应物;如果b是反应物,则(30-x)+(5-y)=10+5,变形得:x+y=20,如果b是生成物,30-x=10+5+(y-5),变形得:x+y=20,B正确;由于0≤y≤20,则x的取值范围是0≤x≤20,C错误;反应生成c与d的质量比为10g∶5g=2∶1,D正确。【例3】合成氨是人类科学技术上的一项重大突破,对社会发展与进步做出了巨大贡献。合成氨的工艺流程图如下:(1)合成氨需要的氮气来自空气,空气中氮气的体积分数约为78%(或4/5)。(2)制取氢气的反应过程为C+H2OCO+H2,CO+H2OCO2+H2。上述两个化学方程式中表现氧化性的物质是H2O(填化学式)。(3)原料中N2、H2中常含有CO2和水蒸气,反应前要净化,净化的过程是先把原混合气体通过氢氧化钠溶液,再通过浓硫酸(或碱石灰等干燥剂)(合理即可)。(4)写出N2、H2反应生成NH3的化学方程式:N2+3H22NH3。(5)将沸点不同的气体分离开来,常采用液化分离法。如控制温度在-183℃时,可将空气中N2与O2分离。根据下表中物质的沸点判断,要将产物NH3与N2、H2分离开来,最适宜的温度应该控制在-33.5℃。【思路点拨】(1)空气中氮气的体积分数约为78%(或4/5)。(2)制取氢气的两个反应中提供氧元素的反应物都是水,所以表现氧化性的物质是水,即H2O。(3)可利用CO2与碱溶液的反应除去CO2,即将混合气体通过NaOH溶液,然后再通过浓硫酸(或碱石灰等干燥剂)除去水蒸气。(4)N2与H2反应生成NH3,条件是高温、高压、催化剂。(5)N

一只****ng
 实名认证
实名认证
 内容提供者
内容提供者
最近下载


















