如果您无法下载资料,请参考说明:
1、部分资料下载需要金币,请确保您的账户上有足够的金币
2、已购买过的文档,再次下载不重复扣费
3、资料包下载后请先用软件解压,在使用对应软件打开
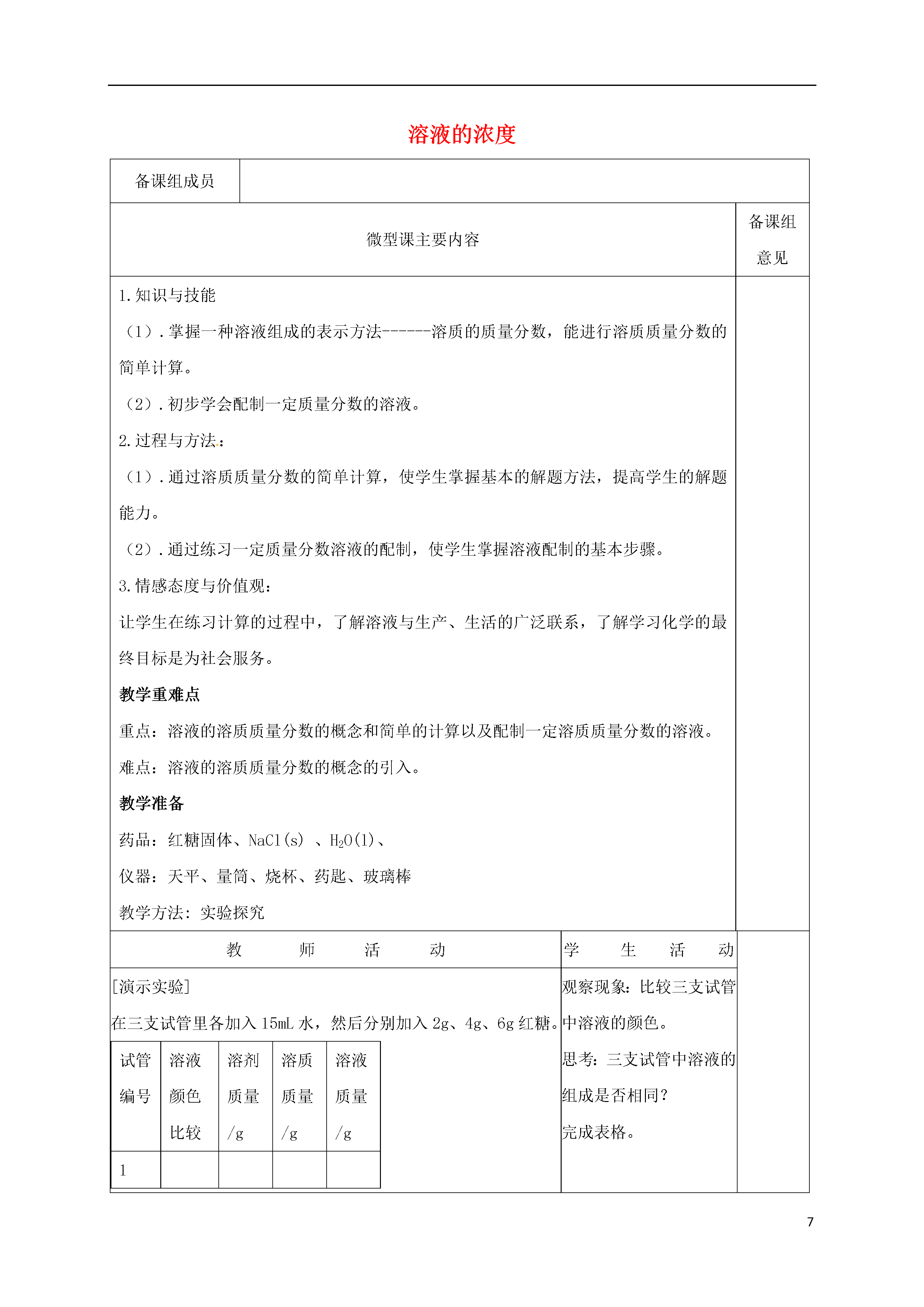
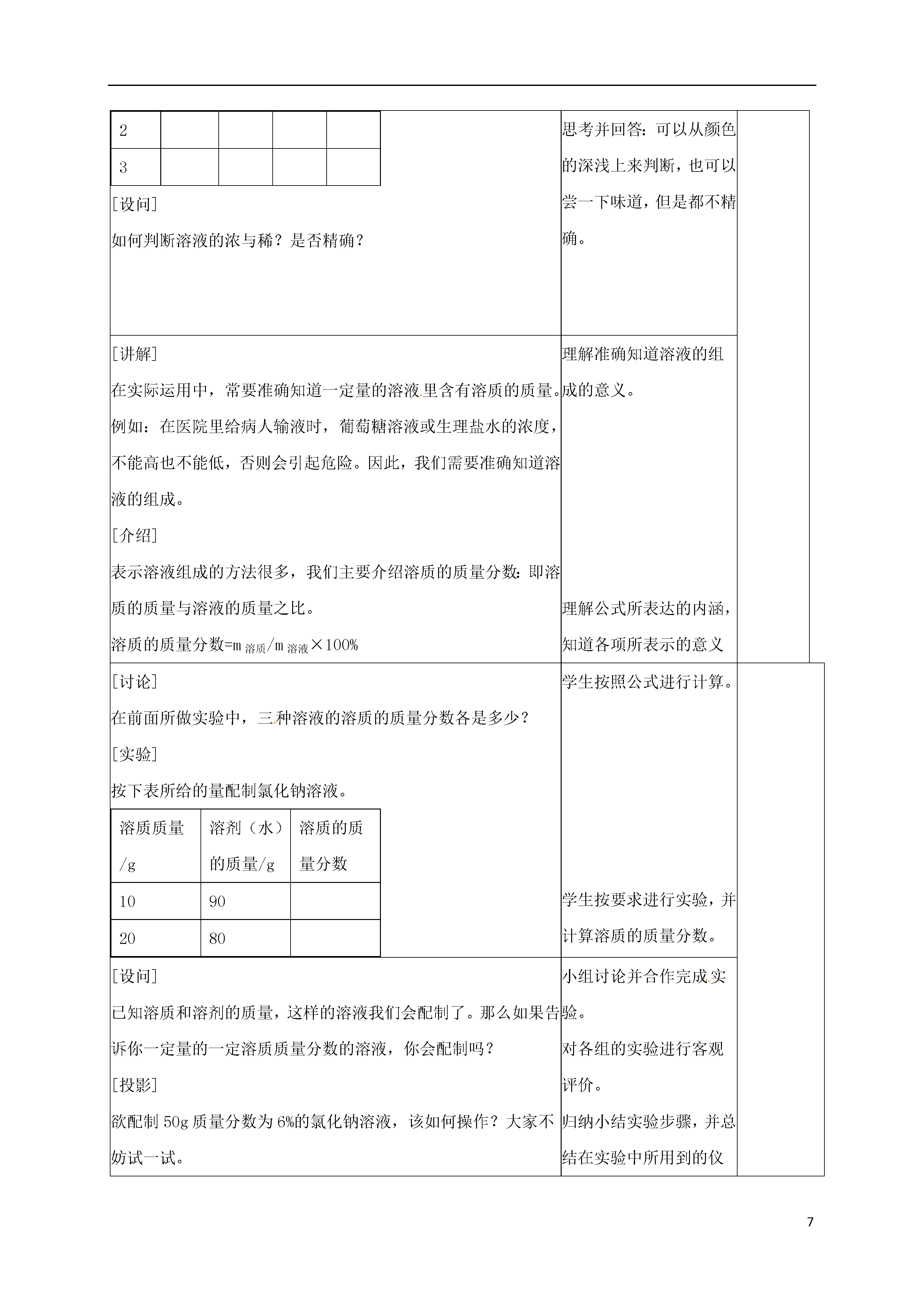
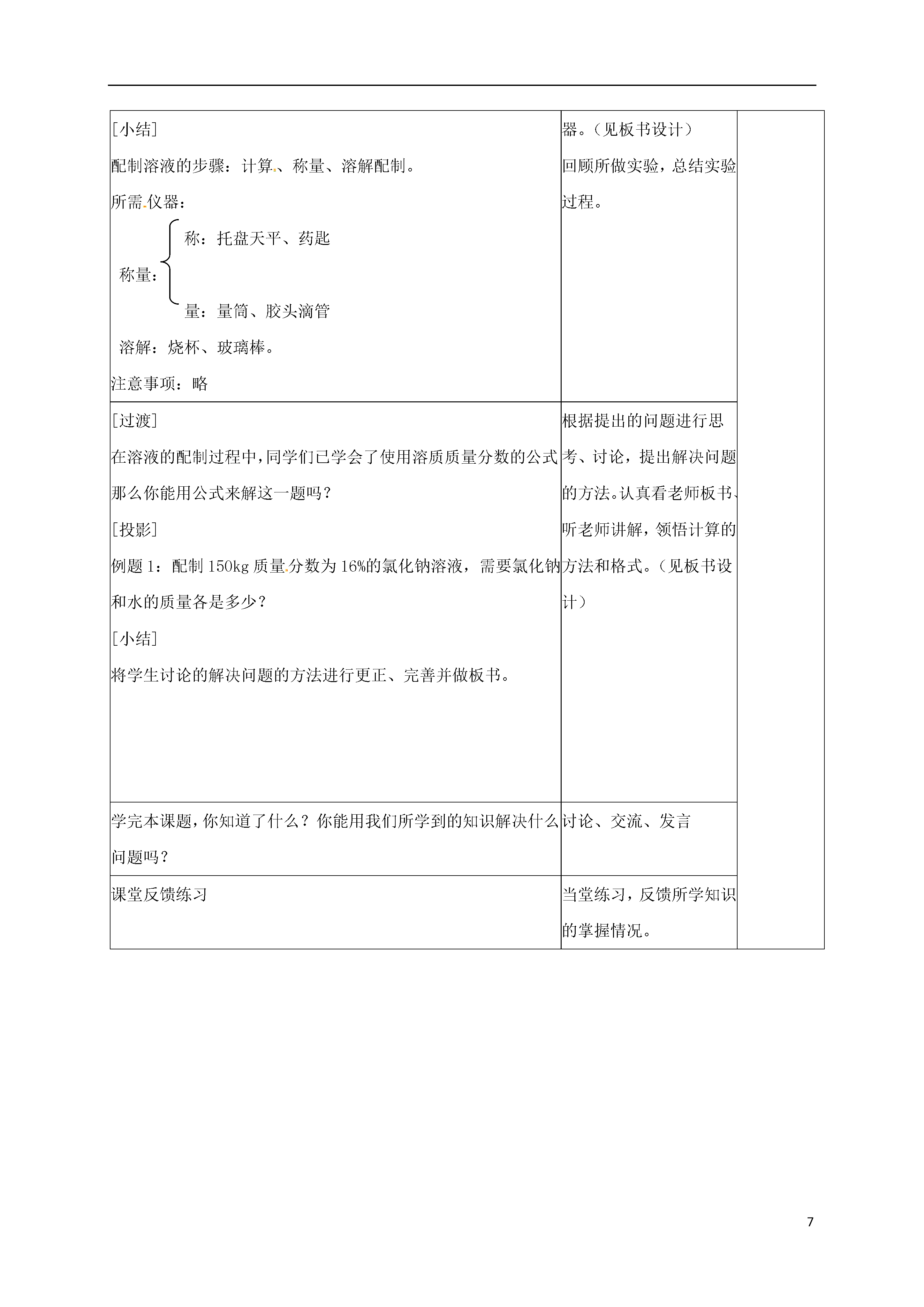
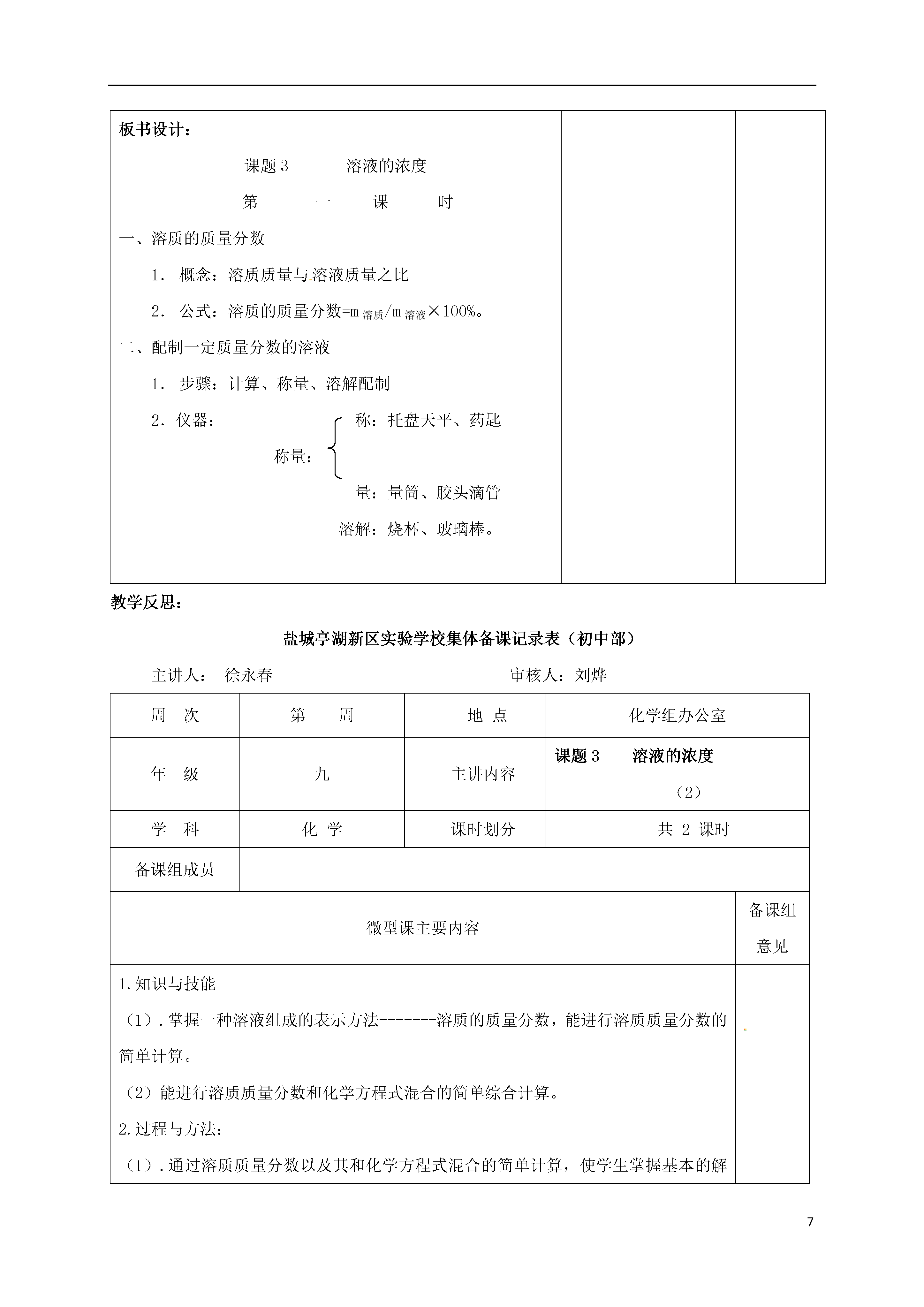
7溶液的浓度备课组成员微型课主要内容备课组意见1.知识与技能(1).掌握一种溶液组成的表示方法------溶质的质量分数,能进行溶质质量分数的简单计算。(2).初步学会配制一定质量分数的溶液。2.过程与方法:(1).通过溶质质量分数的简单计算,使学生掌握基本的解题方法,提高学生的解题能力。(2).通过练习一定质量分数溶液的配制,使学生掌握溶液配制的基本步骤。3.情感态度与价值观:让学生在练习计算的过程中,了解溶液与生产、生活的广泛联系,了解学习化学的最终目标是为社会服务。教学重难点重点:溶液的溶质质量分数的概念和简单的计算以及配制一定溶质质量分数的溶液。难点:溶液的溶质质量分数的概念的引入。教学准备药品:红糖固体、NaCl(s)、H2O(l)、仪器:天平、量筒、烧杯、药匙、玻璃棒教学方法:实验探究教师活动学生活动[演示实验]在三支试管里各加入15mL水,然后分别加入2g、4g、6g红糖。试管编号溶液颜色比较溶剂质量/g溶质质量/g溶液质量/g123[设问]如何判断溶液的浓与稀?是否精确?观察现象:比较三支试管中溶液的颜色。思考:三支试管中溶液的组成是否相同?完成表格。思考并回答:可以从颜色的深浅上来判断,也可以尝一下味道,但是都不精确。[讲解]在实际运用中,常要准确知道一定量的溶液里含有溶质的质量。例如:在医院里给病人输液时,葡萄糖溶液或生理盐水的浓度,不能高也不能低,否则会引起危险。因此,我们需要准确知道溶液的组成。[介绍]表示溶液组成的方法很多,我们主要介绍溶质的质量分数:即溶质的质量与溶液的质量之比。溶质的质量分数=m溶质/m溶液×100%理解准确知道溶液的组成的意义。理解公式所表达的内涵,知道各项所表示的意义[讨论]在前面所做实验中,三种溶液的溶质的质量分数各是多少?[实验]按下表所给的量配制氯化钠溶液。溶质质量/g溶剂(水)的质量/g溶质的质量分数10902080学生按照公式进行计算。学生按要求进行实验,并计算溶质的质量分数。[设问]已知溶质和溶剂的质量,这样的溶液我们会配制了。那么如果告诉你一定量的一定溶质质量分数的溶液,你会配制吗?[投影]欲配制50g质量分数为6%的氯化钠溶液,该如何操作?大家不妨试一试。小组讨论并合作完成实验。对各组的实验进行客观评价。归纳小结实验步骤,并总结在实验中所用到的仪器。(见板书设计)回顾所做实验,总结实验过程。[小结]配制溶液的步骤:计算、称量、溶解配制。所需仪器:称:托盘天平、药匙称量:量:量筒、胶头滴管溶解:烧杯、玻璃棒。注意事项:略[过渡]在溶液的配制过程中,同学们已学会了使用溶质质量分数的公式,那么你能用公式来解这一题吗?[投影]例题1:配制150kg质量分数为16%的氯化钠溶液,需要氯化钠和水的质量各是多少?[小结]将学生讨论的解决问题的方法进行更正、完善并做板书。根据提出的问题进行思考、讨论,提出解决问题的方法。认真看老师板书、听老师讲解,领悟计算的方法和格式。(见板书设计)学完本课题,你知道了什么?你能用我们所学到的知识解决什么问题吗?讨论、交流、发言课堂反馈练习当堂练习,反馈所学知识的掌握情况。板书设计:课题3溶液的浓度第一课时溶质的质量分数概念:溶质质量与溶液质量之比公式:溶质的质量分数=m溶质/m溶液×100%。配制一定质量分数的溶液步骤:计算、称量、溶解配制2.仪器:称:托盘天平、药匙称量:量:量筒、胶头滴管溶解:烧杯、玻璃棒。教学反思:盐城亭湖新区实验学校集体备课记录表(初中部)主讲人:徐永春审核人:刘烨周次第周地点化学组办公室年级九主讲内容课题3溶液的浓度(2)学科化学课时划分共2课时备课组成员微型课主要内容备课组意见1.知识与技能(1).掌握一种溶液组成的表示方法-------溶质的质量分数,能进行溶质质量分数的简单计算。(2)能进行溶质质量分数和化学方程式混合的简单综合计算。2.过程与方法:(1).通过溶质质量分数以及其和化学方程式混合的简单计算,使学生掌握基本的解题方法,提高学生的解题能力。3.情感态度与价值观:让学生在练习计算的过程中,了解溶液与生产、生活的广泛联系,了解学习化学的最终目标是为社会服务。教学重难点重点:溶液的溶质质量分数简单的计算以及溶质质量分数和化学方程式混合的综合计算。难点:溶液的溶质质量分数和化学方程式混合的综合计算。教学准备相关课件及其教学投影片教学方法:讲授法、合作学习法、讨论法教师活动学生活动[提问]什么是溶质的质量分数?它的计算公式是什么?如何配制一定量的溶质
Ta的资源

2025年黑龙江大庆市三站中学七年级数学上学期期末质量检测试题含解析

2025年湖南省永州零冷两区七校联考七年级数学上学期期末质量跟踪监视试题含解析

2025年重庆两江新区数学七上期末质量跟踪监视试题含解析

2025年重庆两江新区七年级数学上学期期末教学质量检测模拟试题含解析

2025年辽宁省大连市中学山区七年级上学期1月期末数学考试试题含解析

2025年贵州省都匀市第六中学数学七上期末学业水平测试试题含解析

2025年贵州省桐梓县联考七年级数学第一学期期中学业质量监测试题含解析

2025年海南省白沙县七年级数学第一学期期中综合测试模拟试题含解析

2025年贵州省都匀市第六中学七年级数学上学期期末达标检测试题含解析

2025年莆田市重点中学七年级上学期1月期末数学经典试题含解析

书生****aa
 实名认证
实名认证
 内容提供者
内容提供者
最近下载
最新上传
商务英语BEC考试高级阅读真题.docx
妈妈的礼物作文用户编辑原创.docx
商务英语BEC考试阅读辅导素材.docx
商务英语BEC考试网上报名流程.docx
2025年黑龙江省七台河市勃利县数学七上期末达标测试试题含解析.docx
2025年黑龙江省七台河市勃利县数学七上期末综合测试试题含解析.docx
2025年黑龙江省七台河市勃利县数学七上期末质量跟踪监视模拟试题含解析.docx
2025年黑龙江省七台河市勃利县数学七上期末联考试题含解析.docx
2025年黑龙江省七台河市勃利县数学七上期末检测模拟试题含解析.docx
2025年黑龙江省七台河市勃利县数学七上期末经典试题含解析.docx








