

如果您无法下载资料,请参考说明:
1、部分资料下载需要金币,请确保您的账户上有足够的金币
2、已购买过的文档,再次下载不重复扣费
3、资料包下载后请先用软件解压,在使用对应软件打开
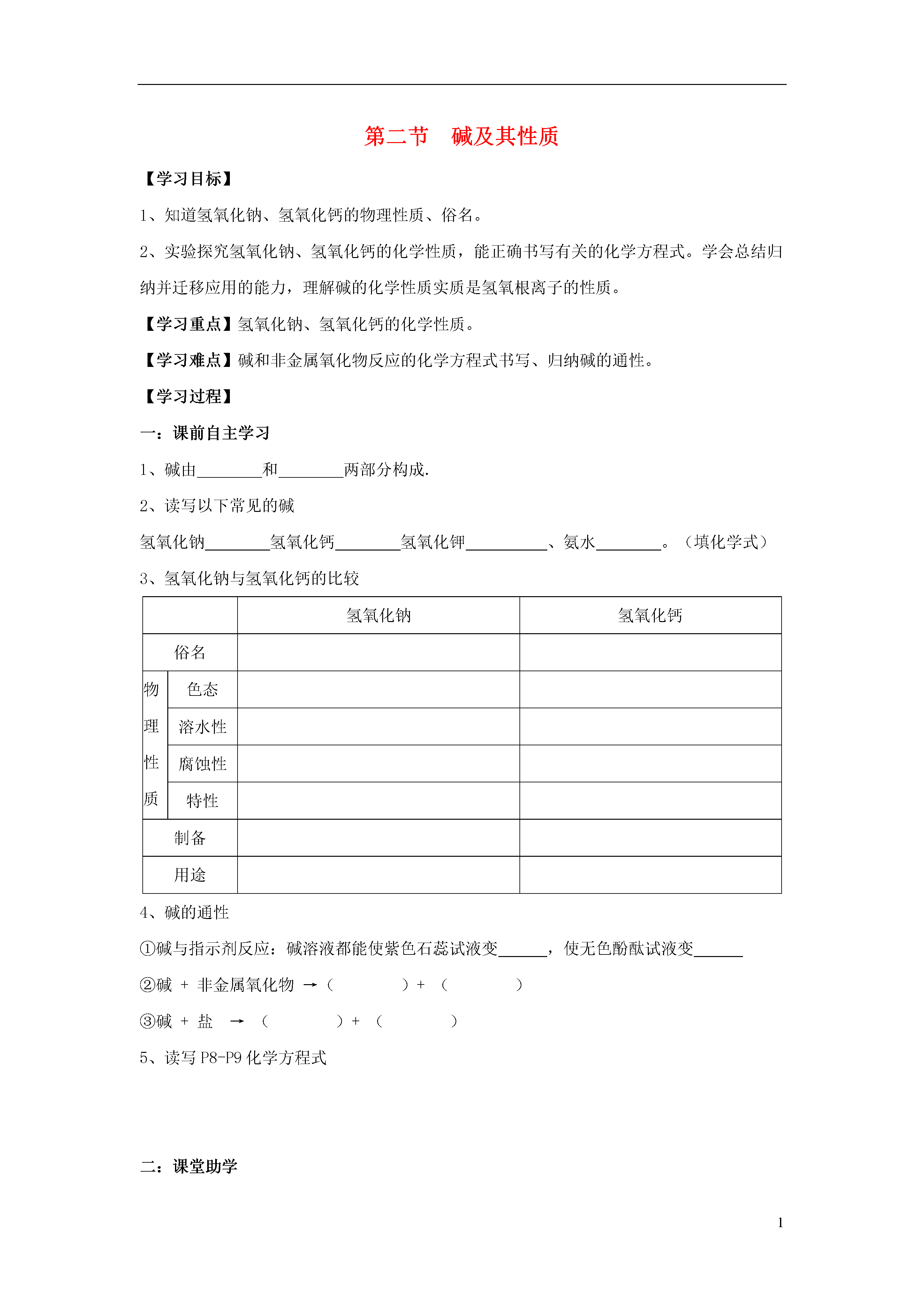
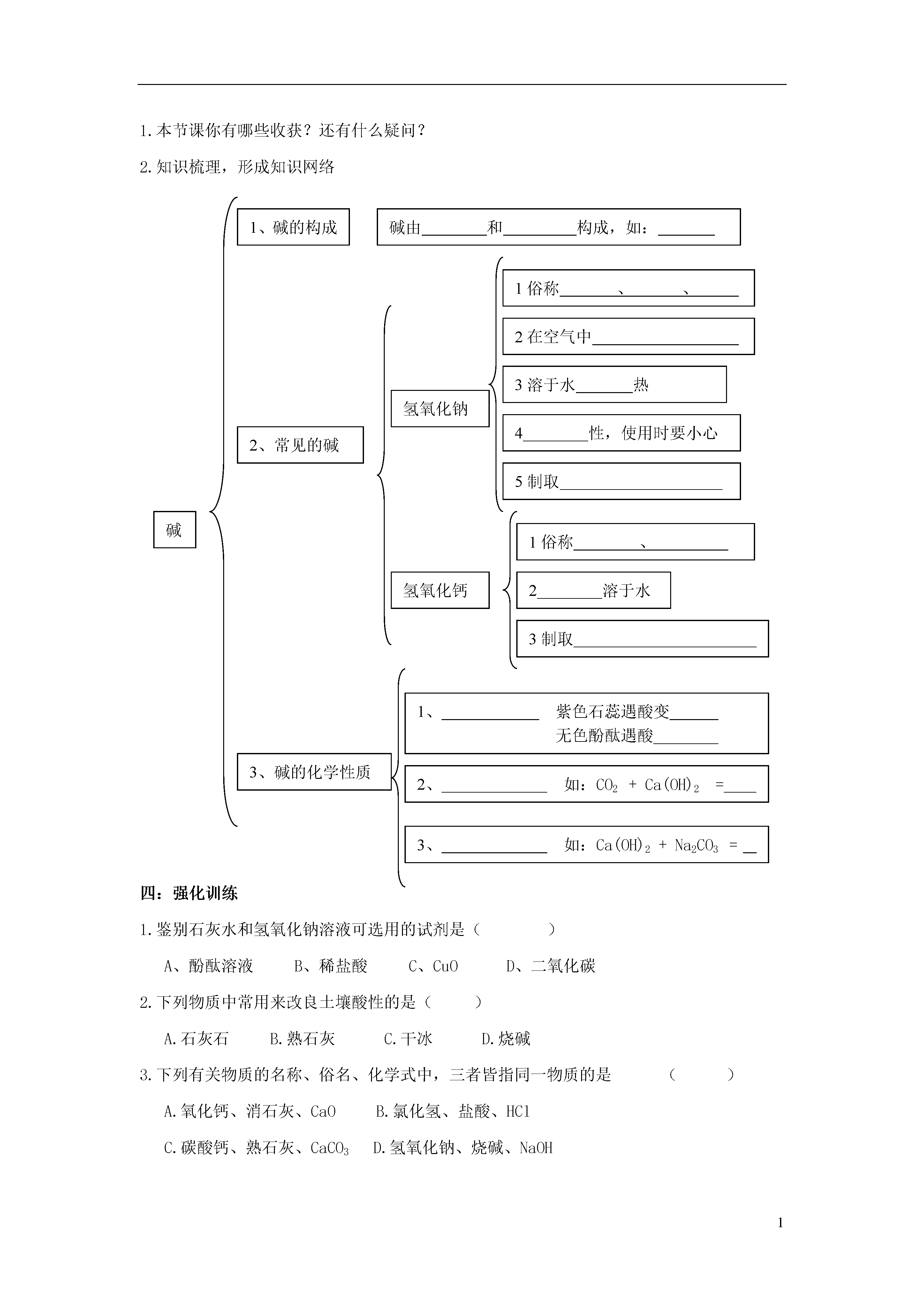
1第二节碱及其性质【学习目标】1、知道氢氧化钠、氢氧化钙的物理性质、俗名。2、实验探究氢氧化钠、氢氧化钙的化学性质,能正确书写有关的化学方程式。学会总结归纳并迁移应用的能力,理解碱的化学性质实质是氢氧根离子的性质。【学习重点】氢氧化钠、氢氧化钙的化学性质。【学习难点】碱和非金属氧化物反应的化学方程式书写、归纳碱的通性。【学习过程】一:课前自主学习1、碱由和两部分构成.2、读写以下常见的碱氢氧化钠氢氧化钙氢氧化钾、氨水。(填化学式)3、氢氧化钠与氢氧化钙的比较氢氧化钠氢氧化钙俗名物理性质色态溶水性腐蚀性特性制备用途4、碱的通性①碱与指示剂反应:碱溶液都能使紫色石蕊试液变,使无色酚酞试液变②碱+非金属氧化物→()+()③碱+盐→()+()5、读写P8-P9化学方程式二:课堂助学导入新课:上一节学习了一类重要的物质——酸,下面再分析氢氧化钠NaOH、氢氧化钙Ca(OH)2组成上有什么共性?本节学习另一类重要的化合物——碱学习活动:认识氢氧化钠、氢氧化钙的固体俗名、物理性质1、投影展示氢氧化钠、氢氧化钙的固体2、投影展示氢氧化钠、氢氧化钙的固体露置在空气中一段时间的变化3、投影展示氢氧化钠、氢氧化钙的固体在水中溶解情况4、投影展示头发(或鸡爪)在氢氧化钠溶液中的变化讨论交流1.如果将氢氧化钠不慎沾到皮肤上,应该怎样处理?2.氢氧化钠能不能露天放置?教师小结完善表格内容,重点记忆探究活动:根据教材P8—P9实验内容完成实验探究,填写有关现象讨论交流1、有的同学认为“实验4中发生的现象不足以证明二氧化碳和氢氧化钠或氢氧化钙溶液发生了化学反应,因为二氧化碳溶解在水中也会产生类似的现象。”你同意这种观点吗?你认为如何改进?2、观察下列实验设计,你能说出它们的设计原理及现象吗?3、氢氧化钠需要密封保存的原因是①②4、能不能用NaOH固体干燥二氧化硫、二氧化碳等气体?5、碱溶液具有相似的化学性质的原因是碱有哪些通性?学生活动:阅读课本了解常见碱的用途:三:课堂反思:1.本节课你有哪些收获?还有什么疑问?2.知识梳理,形成知识网络碱由和构成,如:1、碱的构成1俗称、、2在空气中氢氧化钠3溶于水热4性,使用时要小心2、常见的碱5制取碱1俗称、氢氧化钙2溶于水3制取1、紫色石蕊遇酸变无色酚酞遇酸3、碱的化学性质2、如:CO2+Ca(OH)2=3、如:Ca(OH)2+Na2CO3=四:强化训练1.鉴别石灰水和氢氧化钠溶液可选用的试剂是()A、酚酞溶液B、稀盐酸C、CuOD、二氧化碳2.下列物质中常用来改良土壤酸性的是()A.石灰石B.熟石灰C.干冰D.烧碱3.下列有关物质的名称、俗名、化学式中,三者皆指同一物质的是()A.氧化钙、消石灰、CaOB.氯化氢、盐酸、HClC.碳酸钙、熟石灰、CaCO3D.氢氧化钠、烧碱、NaOH4.下列气体可以用固体氢氧化钠干燥的是()A、氯化氢B、氢气C、二氧化碳D、二氧化硫5.下列质量增加的变化有一种与其它三种存在本质的区别,这种变化是()A.长期放置在空气中的氢氧化钠质量增加B.长期敞口放置的浓硫酸质量增加C.久置的生石灰质量增加D.久置的铁钉生锈质量增加6.如右图所示装置,向试管里的水中加入某种物质后,U形管右边支管的红墨水液面降低,左边支管的红墨水液面上升,则加入的物质可能是()A.氢氧化钠B.生石灰C.浓硫酸D.硝酸铵7.从石灰浆抹的墙壁上掉下的一块白色固体,为探究其成分,进行如下实验:实验步骤实验现象①将固体磨成粉末状,加水搅拌固体没有全部溶解②取上层清液,滴加酚酞试液溶液呈红色③取不溶物,滴加稀盐酸有气泡产生由此得出的结论正确的是()A.一定含有Ca(OH)2,可能有CaCO3B.一定含有CaCO3和Ca(OH)2C.一定没有CaCO3和Ca(OH)2D.一定有CaCO3,可能有Ca(OH)28.下列四种实验设计及操作,实验过程中其现象不足以说明CO2与NaOH溶液发生反应的是()9.纯净的氢氧化钠是一种___色固体,由于在空气里它不仅能吸收___而潮解,还能跟空气里的___起反应而变质。所以,氢氧化钠必须___保存。写出有关反应的化学方程式:。向变质的氢氧化钠中加入足量的盐酸,可观察到的现象是_____________,写出所发生反应的化学方程式:___________________。
Ta的资源

2025年重庆市江北区新区联盟七年级上学期1月期末数学复习检测模拟试题含解析

2025年贵州省都匀市第六中学七年级数学上学期期末调研试题含解析

2025年福建省福州市华伦中学七年级上学期1月期末数学学业质量监测模拟试题含解析

2025年黑龙江省七台河市勃利县七年级数学第一学期期中复习检测试题含解析

2025年湖南省涟源市七年级上学期1月期末数学考试模拟试题含解析

2025年湖北省荆州市洪湖市七年级数学第一学期期中经典模拟试题含解析

2025年辽宁省盘锦双台子区六校联考七年级数学上学期期末学业水平测试试题含解析

2025年辽宁省丹东33中学七年级数学上学期期末统考试题含解析

2025年贵州省桐梓县联考七年级数学第一学期期中综合测试模拟试题含解析

2025年福建省莆田市涵江区七年级上学期1月期末数学学业水平测试试题含解析

书生****专家
 实名认证
实名认证
 内容提供者
内容提供者
最近下载
最新上传
商务英语BEC考试高级阅读真题.docx
妈妈的礼物作文用户编辑原创.docx
商务英语BEC考试阅读辅导素材.docx
商务英语BEC考试网上报名流程.docx
2025年黑龙江省七台河市勃利县数学七上期末达标测试试题含解析.docx
2025年黑龙江省七台河市勃利县数学七上期末综合测试试题含解析.docx
2025年黑龙江省七台河市勃利县数学七上期末质量跟踪监视模拟试题含解析.docx
2025年黑龙江省七台河市勃利县数学七上期末联考试题含解析.docx
2025年黑龙江省七台河市勃利县数学七上期末检测模拟试题含解析.docx
2025年黑龙江省七台河市勃利县数学七上期末经典试题含解析.docx








