


如果您无法下载资料,请参考说明:
1、部分资料下载需要金币,请确保您的账户上有足够的金币
2、已购买过的文档,再次下载不重复扣费
3、资料包下载后请先用软件解压,在使用对应软件打开
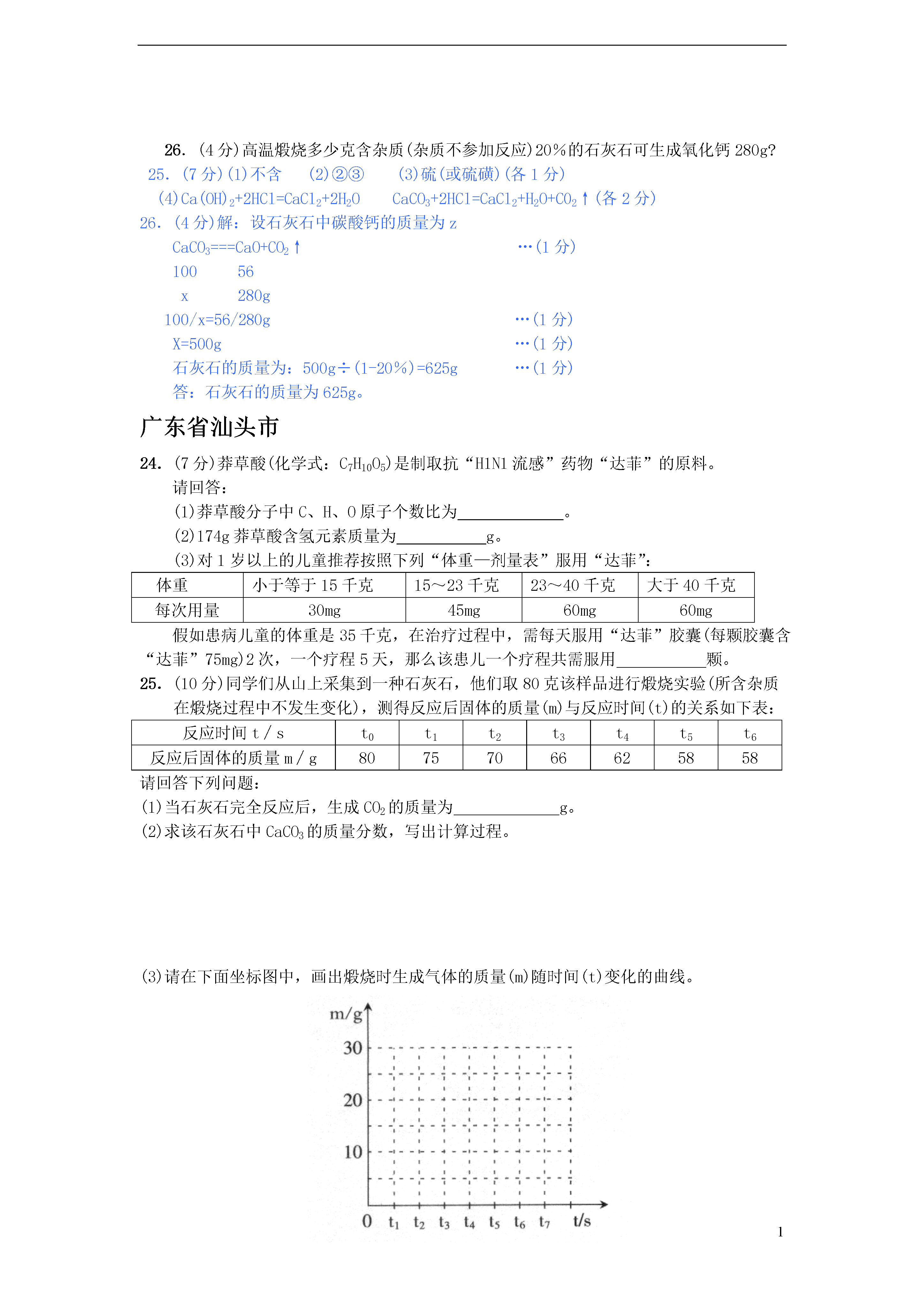
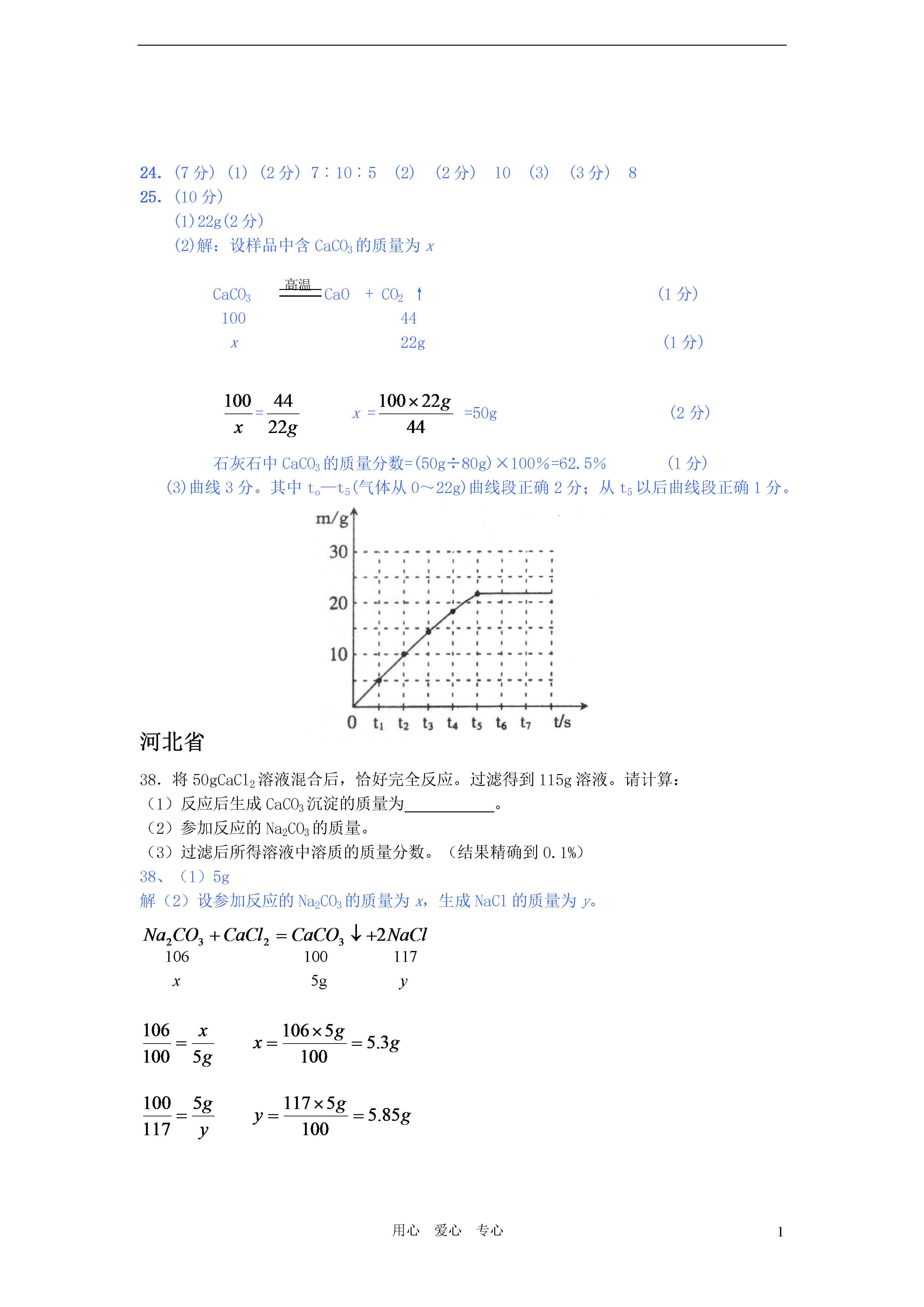
1用心爱心专心【2009年中考化学计算试题精讲精练】江西省29.(3分)2008年“毒奶事件”的起因是某些牛奶供应商为了提高利润而在牛奶中兑水,导致牛奶含氮量降低(牛奶主要成分是含氮的蛋白质),通常1Kg牛奶含有0.2Kg的氮才刚好合格,因此不法供应商就将含氮量较高的三聚氰胺(C3H8N6)掺入加水的牛奶中以通过检测。(1)三聚氰胺中氢、氮元素的质量比;(2)三聚氰胺中氮元素的质量分数为;(计算结果精确到0.1%)(3)现有某不法供应商将1Kg刚好合格的牛奶配成1.5Kg的“毒奶”,且顺利通过了测试,他至少在牛奶中加入了三聚氰胺Kg。30.(7分)(1)小强为了探究某炼铁厂赤铁矿石中氧化铁的质量分数,设计了如图所示的装置进行实验,测出赤铁矿中氧化铁的质量分数为80%。现炼铁厂利用该赤铁矿石5000t,理论上可炼出含铁98%的生铁的质量是多少?(结果保留整数)(2)在利用上图装置进行实验时,小强得到如下两组数据(杂质不参加反应)你认为他应该选用了(填“A”或“B”)组数据来就计算赤铁矿石中氧化铁的质量分数;结合装置图回答他不能选用另一组数据计算的原因是。肇庆市***牌口服液主要成分:葡萄糖酸锌化学式:C12H22O14Zn含锌:5.0mg/支质量:10.0g/支生产日期:······24.(5分)儿童缺锌会引起食欲不振、发育不良。右图为某种补锌口服液说明书的一部分,请回答:(1)该口服液中的锌属于(填:“常量”或“微量”)元素;葡萄糖酸锌分子中的碳、氢元素的质量比为。(2)每支口服液中锌的质量分数为(1g=1000mg)。(3)若儿童1kg体重每日需要0.5mg锌,每天从食物中只能摄入所需锌的一半;体重为20kg的儿童每天还须服该口服液支,才能满足身体的需要。△25.(7分)某同学为了检验家里购买的硫酸铵化肥是否合格,他称取27.5g化肥样品与足量浓烧碱溶液加热,产生的氨气用100.0g废硫酸吸收。测得吸收氨气的溶液总质量m与反应时间t的变化如右下图所示。所涉及的反应为:(NH4)2SO4+2NaOH===Na2SO4+2H2O+2NH3↑;2NH3+H2SO4==(NH4)2SO4。请计算:(1)完全反应后产生氨气g。(2)该化肥的含氮量为(精确到0.1%),则这种化肥属于(填:“合格”或“不合格”。合格硫酸铵含氮量为20%以上)产品。(3)请计算废硫酸中硫酸的质量分数(写出计算过程)。(4)若实验过程中氨气被完全吸收,但该实验测得硫酸铵化肥的含氮量高于实际值,其原因是。24.(5分)(1)(2分)微量(1分)72:11(1分)(2)(1分)0.05%(3)(2分)125.(7分)(1)(1分)6.8g(2)(2分)20.4%合格(3)解:设废硫酸中纯硫酸的质量为x。2NH3+H2SO4==(NH4)2SO4,34986.8gx..............................................................................................(1分)...............................................................................(1分)H2SO4%=(19.6g÷100.0g)×100%=19.6%.......................................................(1分)答:废硫酸中硫酸的质量分数为19.6%。(4)(1分)加热反应产生的水蒸汽被废硫酸吸收,导致所测吸收液质量比只吸收氨气大。常州市25.(7分)大龙在公园看到绿化工人往树干上涂抹具有杀菌杀虫作用的悬浊液,对其成份产生了好奇,于是他带回了一些样本进行研究。信息提示:许多金属或它们的化合物在灼烧时都会使火焰呈现特殊的颜色,这叫做焰色反应。如:钠——黄色;钙——砖红色;钾——紫色;钡——黄绿色Ⅰ猜想与假设:该制剂可能为波尔多液Ⅱ实验探究:序号实验步骤实验现象①取样,将其置于大试管中,加入一定量水,静置片刻上层有黄色固体漂浮,中层为无色液体,下层有较多白色固体②取少量中层液体滴加无色酚酞试液无色酚酞试液变红③另取少量中层液体进行焰色反应火焰呈现砖红色④取少量黄色固体灼烧燃烧,放热,产生淡蓝色火焰,有刺激性气味⑤向下层白色固体中滴加足量稀盐酸固体完全溶解,但仅产生少量气泡Ⅲ实验结论:(1)根据上述实验①,可以判断该悬浊液中▲(填“含”或“不含”)硫酸铜;(2)根据上述实验▲(填序号),可以判断该悬浊液中含有氢氧化钙;(
Ta的资源

2025年黑龙江大庆市三站中学七年级数学上学期期末联考模拟试题含解析

2025年辽宁省盘锦双台子区六校联考七年级数学上学期期末监测模拟试题含解析

2025年辽宁省大连市中学山区七年级上学期1月期末数学学业水平测试试题含解析

2025年贵州省凯里市华鑫实验学校七年级上学期1月期末数学复习检测模拟试题含解析

2025年浙江省宁波市名校七年级数学第一学期期中统考模拟试题含解析

2025年湖南省长沙青竹湖湘一外国语学校数学七上期末联考模拟试题含解析

2025年湖北省武汉市青山区数学七上期末考试模拟试题含解析

2025年湖北省武汉市求新联盟联考七年级数学第一学期期中检测模拟试题含解析

2025年湖北省荆州市洪湖市数学七上期末考试试题含解析

2025年河南省周口市扶沟县七年级上学期1月期末数学监测试题含解析

瀚玥****魔王
 实名认证
实名认证
 内容提供者
内容提供者
最近下载
最新上传
2025年黑龙江省七台河市勃利县数学七上期末达标测试试题含解析.docx
2025年黑龙江省七台河市勃利县数学七上期末综合测试试题含解析.docx
2025年黑龙江省七台河市勃利县数学七上期末质量跟踪监视模拟试题含解析.docx
2025年黑龙江省七台河市勃利县数学七上期末联考试题含解析.docx
2025年黑龙江省七台河市勃利县数学七上期末检测模拟试题含解析.docx
2025年黑龙江省七台河市勃利县数学七上期末经典试题含解析.docx
2025年黑龙江省七台河市勃利县数学七上期末学业质量监测模拟试题含解析.docx
2025年黑龙江省七台河市勃利县数学七上期末复习检测模拟试题含解析.docx
2025年黑龙江省七台河市勃利县七年级数学第一学期期中达标检测模拟试题含解析.docx
2025年黑龙江省七台河市勃利县七年级数学第一学期期中监测模拟试题含解析.docx








