

如果您无法下载资料,请参考说明:
1、部分资料下载需要金币,请确保您的账户上有足够的金币
2、已购买过的文档,再次下载不重复扣费
3、资料包下载后请先用软件解压,在使用对应软件打开
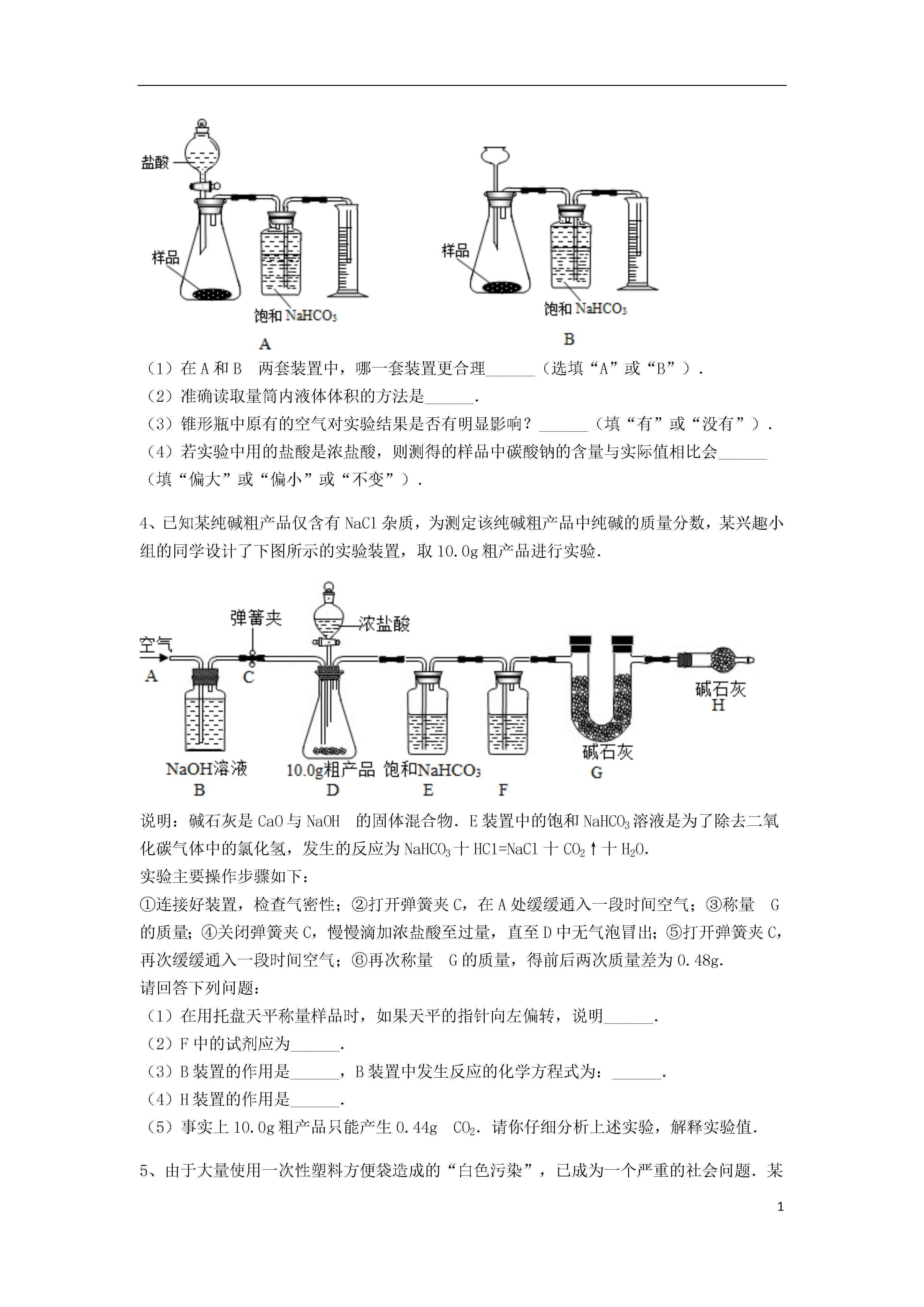
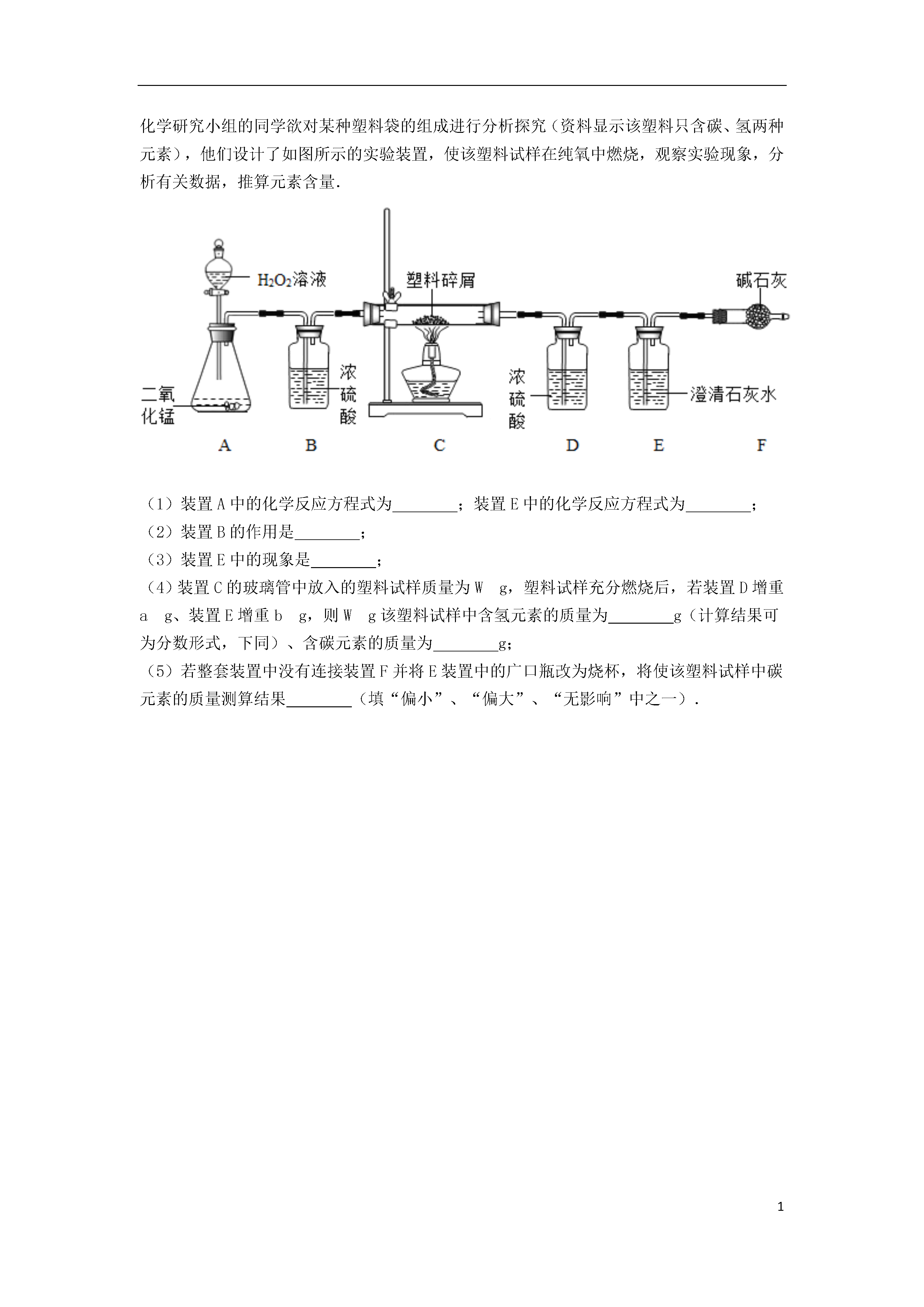
1实验数据处理或者误差分析的探究7实验室有一瓶久置部分变质的氢氧化钠固体,某化学兴趣小组采用如图所示装置测定样品中氢氧化钠的质量分数实验操作过程如下:把准确称量的10.0克样品装入B装置后,将装置B分别与装置A和C相连,打开开关K,从a处缓缓鼓入空气几分钟后,将开关K关闭,再将已称量过的干燥管D与装置C连接,然后将足量的稀硫酸缓缓注入B装置的瓶中.待反应完全后,再次打开开关K缓缓鼓入空气几分钟,最后称量干燥管D,增重了2.2克.请回答:(1)氢氧化钠固体久置变质的化学方程式是______.(2)为顺利完成实验探究,你认为上图的装置可选用下图中的______装置(填装置序号).(3)装置B中产生气体的化学方程式是______.(4)由干燥管D增加的质量,可推算出样品中氢氧化钠的质量分数为______.(5)装置C的作用是______.(6)装置A是为了吸收空气中的某气体,实验前第一次鼓入空气是为了驱赶装置中的该气体,则该气体是______(填物质的化学式).若反应后不鼓入空气,对测定结果的影响是______(填“偏大”或“偏小”).实验室制取氧气的实践与研究.(1)过氧化氢是一种无色透明的无毒液体,过氧化氢溶液俗称“双氧水”,具有强氧化性.贮运过氧化氢的试剂箱上最适合粘贴的一张标识是(从上图中选填字母序号).(2)过氧化氢溶液常用于实验室制取氧气.可供选择的仪器或装置如下图所示.①要收集干燥的氧气,整套装置的连接顺序为(由气体发生装置开始)(选填字母A~E);②加入药品通常采用“把过氧化氢溶液缓缓加入盛有少量MnO2的反应容器中”,优点是;③MnO2可以连续反应使用,理由是;④根据化学方程式计算获得的氧气理论值总是比实际实验操作收集到气体的数值大(若装置不漏气且实验操作正确),原因是.(3)生产火箭燃料的工业废水中含有少量偏二甲肼X,可用双氧水处理排污,反应的化学方程式为X+8H2O2=2CO2↑+N2↑+12H2O,则X的化学式为.(4)85g过氧化氢溶液加入wg二氧化锰反应完全后,留下混合物质量仍为85g,则过氧化氢溶液中溶质的质量分数为.青海湖地区素有“夏天晒盐,冬天捞碱”之说,其中捞出的碱主要是碳酸钠和少量氯化钠的混合物.小王同学以捞出的碱作为样品,并用以下一套装置对样品进行分析,根据量筒中收集到的液体的体积(相当于二氧化碳的体积)来计算样品中碳酸钠的含量.(已知:HCl+NaHCO3═NaCl+CO2↑+H2O;CO2在饱和NaHCO3溶液中溶解度很小)(1)在A和B两套装置中,哪一套装置更合理______(选填“A”或“B”).(2)准确读取量筒内液体体积的方法是______.(3)锥形瓶中原有的空气对实验结果是否有明显影响?______(填“有”或“没有”).(4)若实验中用的盐酸是浓盐酸,则测得的样品中碳酸钠的含量与实际值相比会______(填“偏大”或“偏小”或“不变”).已知某纯碱粗产品仅含有NaCl杂质,为测定该纯碱粗产品中纯碱的质量分数,某兴趣小组的同学设计了下图所示的实验装置,取10.0g粗产品进行实验.说明:碱石灰是CaO与NaOH的固体混合物.E装置中的饱和NaHCO3溶液是为了除去二氧化碳气体中的氯化氢,发生的反应为NaHCO3十HC1=NaCl十CO2↑十H2O.实验主要操作步骤如下:①连接好装置,检查气密性;②打开弹簧夹C,在A处缓缓通入一段时间空气;③称量G的质量;④关闭弹簧夹C,慢慢滴加浓盐酸至过量,直至D中无气泡冒出;⑤打开弹簧夹C,再次缓缓通入一段时间空气;⑥再次称量G的质量,得前后两次质量差为0.48g.请回答下列问题:(1)在用托盘天平称量样品时,如果天平的指针向左偏转,说明______.(2)F中的试剂应为______.(3)B装置的作用是______,B装置中发生反应的化学方程式为:______.(4)H装置的作用是______.(5)事实上10.0g粗产品只能产生0.44gCO2.请你仔细分析上述实验,解释实验值.由于大量使用一次性塑料方便袋造成的“白色污染”,已成为一个严重的社会问题.某化学研究小组的同学欲对某种塑料袋的组成进行分析探究(资料显示该塑料只含碳、氢两种元素),他们设计了如图所示的实验装置,使该塑料试样在纯氧中燃烧,观察实验现象,分析有关数据,推算元素含量.(1)装置A中的化学反应方程式为;装置E中的化学反应方程式为;(2)装置B的作用是;(3)装置E中的现象是;(4)装置C的玻璃管中放入的塑料试样质量为Wg,塑料试样充分燃烧后,若装置D增重ag、装置E增重bg,则Wg该塑料试样中含氢元素的质量为g(计算结果可为分数形式,下
Ta的资源

2024-2025学年内蒙古巴彦淖尔市第五中学数学七上期末联考试题含解析

2024-2025学年云南省曲靖市沾益县七年级数学上学期期末复习检测试题含解析

2024-2025学年云南省红河州七年级数学第一学期期中联考模拟试题含解析

2024-2025学年云南省曲靖市七年级数学第一学期期中统考模拟试题含解析

2024-2025学年云南省保山市名校七年级上学期1月期末数学学业水平测试试题含解析

2024-2025学年云南省大理州祥云县七年级数学上学期期末达标测试试题含解析

2024-2025学年上海市长宁区高级中学七年级数学上学期期末监测试题含解析

2024-2025学年上海市延安实验初级中学七年级上学期1月期末数学教学质量检测模拟试题含解析

2024-2025学年上海市延安实验初级中学七年级数学上学期期末调研模拟试题含解析

2024-2025学年上海市延安实验初级中学七年级上学期1月期末数学学业质量监测模拟试题含解析

朋兴****en
 实名认证
实名认证
 内容提供者
内容提供者
最近下载
最新上传
2024-2025学年内蒙古自治区呼伦贝尔市满洲里市七年级数学第一学期期中质量检测模拟试题含解析.docx
2024-2025学年内蒙古自治区呼伦贝尔市满洲里市七年级数学第一学期期中综合测试模拟试题含解析.docx
2024-2025学年内蒙古自治区呼伦贝尔市满洲里市七年级数学第一学期期中经典模拟试题含解析.docx
2024-2025学年内蒙古自治区呼伦贝尔市满洲里市七年级数学上学期期末预测试题含解析.docx
2024-2025学年内蒙古自治区呼伦贝尔市满洲里市七年级数学第一学期期中检测模拟试题含解析.docx
2024-2025学年内蒙古自治区呼伦贝尔市满洲里市七年级数学第一学期期中学业水平测试试题含解析.docx
2024-2025学年内蒙古自治区呼伦贝尔市满洲里市七年级数学上学期期末联考试题含解析.docx
2024-2025学年内蒙古自治区呼伦贝尔市满洲里市七年级数学上学期期末质量跟踪监视试题含解析.docx
2024-2025学年内蒙古自治区呼伦贝尔市满洲里市七年级数学上学期期末经典试题含解析.docx
2024-2025学年内蒙古自治区呼伦贝尔市满洲里市七年级数学上学期期末综合测试试题含解析.docx








